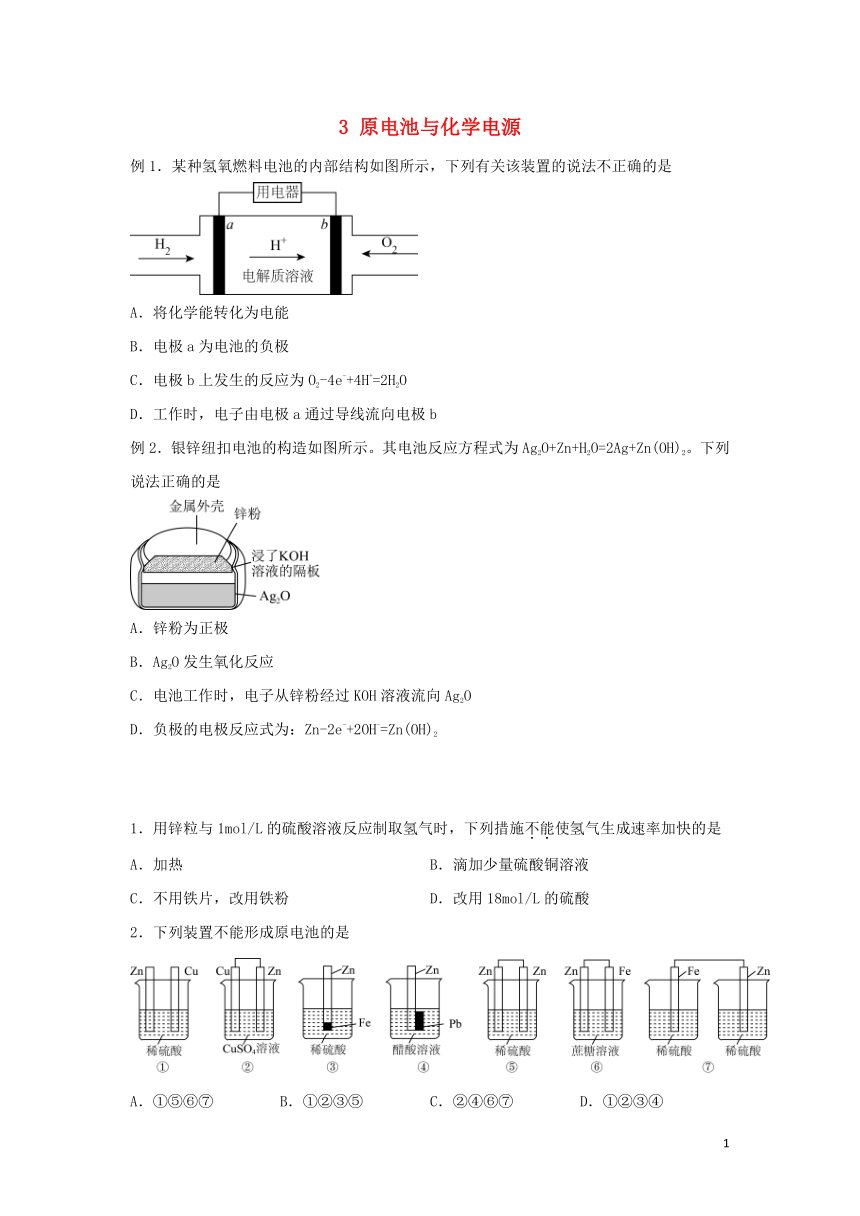
3 原电池与化学电源 例1.某种氢氧燃料电池的内部结构如图所示,下列有关该装置的说法不正确的是 A.将化学能转化为电能 B.电极a为电池的负极 C.电极b上发生的反应为O2-4e-+4H+=2H2O D.工作时,电子由电极a通过导线流向电极b 例2.银锌纽扣电池的构造如图所示。其电池反应方程式为Ag2O+Zn+H2O=2Ag+Zn(OH)2。下列说法正确的是 A.锌粉为正极 B.Ag2O发生氧化反应 C.电池工作时,电子从锌粉经过KOH溶液流向Ag2O D.负极的电极反应式为:Zn-2e-+2OH-=Zn(OH)2 1.用锌粒与1mol/L的硫酸溶液反应制取氢气时,下列措施不能使氢气生成速率加快的是 A.加热 B.滴加少量硫酸铜溶液 C.不用铁片,改用铁粉 D.改用18mol/L的硫酸 2.下列装置不能形成原电池的是 A.①⑤⑥⑦ B.①②③⑤ C.②④⑥⑦ D.①②③④ 3.科学研究发现,火星存在大量,有科学家提出设想:利用火星上设计电池,电池反应为。下列说法错误的是 A.钠在负极发生氧化反应 B.在正极上生成C C.放电时向正极迁移 D.参与反应时转移12mol电子 4.普通锌锰干电池的构造如图所示,其电池反应的方程式为:。下列说法正确的是 A.石墨作负极 B.锌发生还原反应 C.电池工作时,电子从石墨经导线流向锌 D.正极的电极反应为: 5.化学能与热能、电能等可相互转化。关于化学能与其他能量相互转化的说法正确的是 A.化学反应中能量变化的主要原因是物质状态的改变 B.铝与盐酸的反应中,反应物的总能量比生成物的总能量高 C.图I所示的装置能将化学能转变为电能 D.图II所示的反应为吸热反应 6.有A、B、C、D四种金属。将A与B用导线连接起来,浸入电解质溶液中,B为正极。将A、D分别投入等浓度盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化。如果把铜浸入C的盐溶液里,有金属C析出。据此判断它们的活泼性由强到弱的顺序是 A.D>A>B>C B.B>A>D>C C.D>B>A>C D.D>A>C>B 7.一种锂水电池以锂和钢板为电极,为电解质,使用时加入水即可放电,总反应为:。下列有关该电池的说法错误的是 A.锂极为负极 B.移向正极 C.为正极产物 D.电子由锂经导线流向钢板 8.将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计(装置如右图),若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为47g,则该过程中产生H2(标准状况下)的体积为 A.2.24L B.3.36L C.4.48L D.6.72L 9.利用微生物燃料电池原理,可以处理宇航员排出的粪便,同时得到电能。设计的方案是:用微生物中的芽孢杆菌来处理粪便产生氨气,氨气与氧气分别通入燃料电池两极,如图。下列说法错误的是 A.a电极是负极,b电极是正极 B.负极区发生的反应是2NH3 - 6e-=N2+6H+ C.正极区,每消耗标准状况下2.24 L O2,a向b电极转移0.4 mol电子 D.负极区,每消耗标准状况下2.24 LNH3,a向b电极转移0.6 mol电子 10.(双选)以铁片和铜片为电极,以稀硫酸为电解质溶液组成的原电池,当导线中通过电子时,下列叙述正确的是 A.铁片溶解1mol,铜片上析出1mol H2 B.两极上溶解和析出的物质的质量相等 C.铁片溶解2g,铜片上析出1g H2 D.铁片溶解1mol,硫酸消耗1mol 11.(双选)质量相同的铁棒、碳棒和足量CuCl2溶液组成的装置如图所示,下列说法正确的是 A.闭合K,电子通过CuCl2溶液移到碳棒上 B.闭合K,铁棒表面发生的电极反应为Cu2++2e-=Cu C.闭合K,转移电子0.2mol时,理论上碳棒与铁棒的质量差为12g D.打开K,与闭合K时发生的总反应相同 12.为探究Ag+与Fe3+氧化性的相关问题,某小组同学进行如下实验: 已知:相关物质的溶解度(20℃)AgCl:1.5×10-4 g ;Ag2SO4:0.796 g。 (1)甲同学的实验如下: 序号 操作 现象 实验Ⅰ 将2 ... ...
~~ 您好,已阅读到文档的结尾了 ~~

