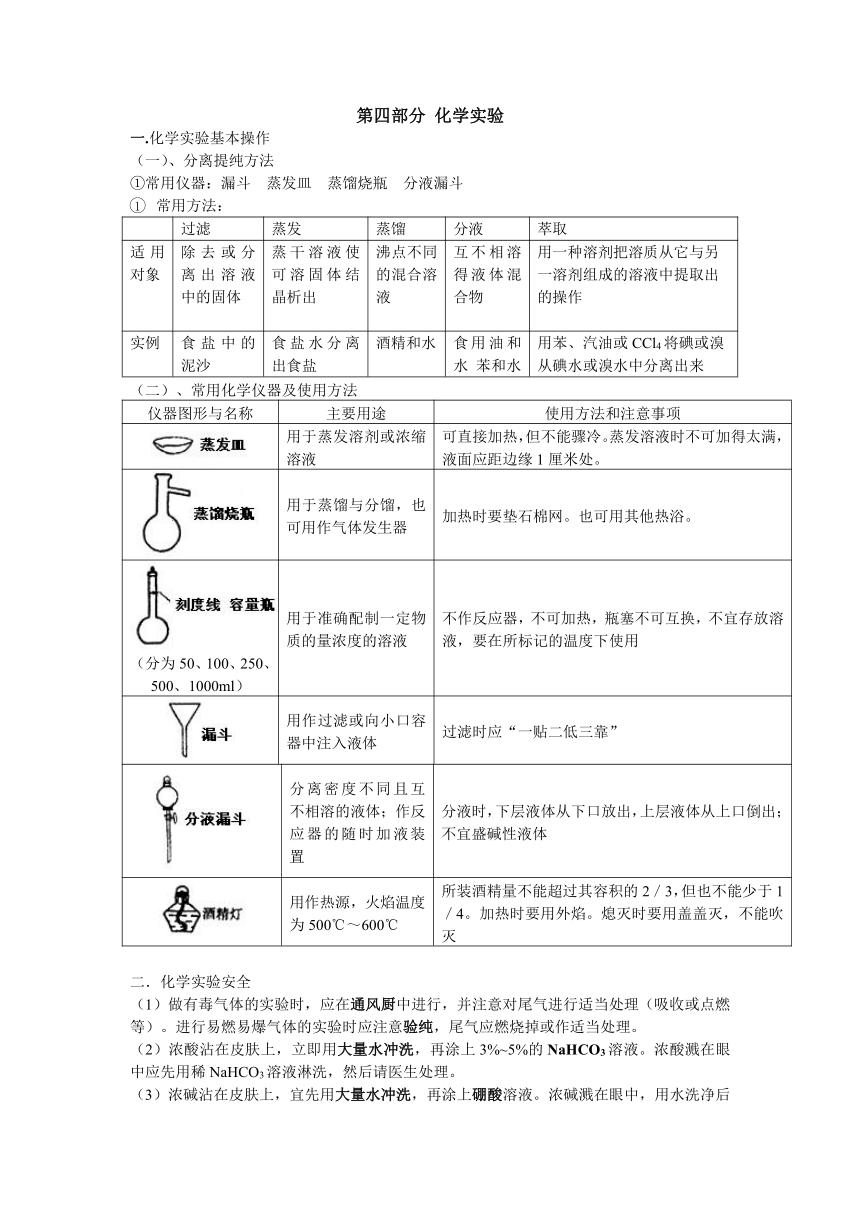
第四部分 化学实验 一.化学实验基本操作 (一)、分离提纯方法 ①常用仪器:漏斗 蒸发皿 蒸馏烧瓶 分液漏斗 常用方法: 过滤 蒸发 蒸馏 分液 萃取 适用对象 除去或分离出溶液中的固体 蒸干溶液使可溶固体结晶析出 沸点不同的混合溶液 互不相溶得液体混合物 用一种溶剂把溶质从它与另一溶剂组成的溶液中提取出的操作? 实例 食盐中的泥沙 食盐水分离出食盐 酒精和水 食用油和水 苯和水 用苯、汽油或CCl4将碘或溴从碘水或溴水中分离出来 (二)、常用化学仪器及使用方法 仪器图形与名称 主要用途 使用方法和注意事项 用于蒸发溶剂或浓缩溶液 可直接加热,但不能骤冷。蒸发溶液时不可加得太满,液面应距边缘1厘米处。 用于蒸馏与分馏,也可用作气体发生器 加热时要垫石棉网。也可用其他热浴。 (分为50、100、250、500、1000ml) 用于准确配制一定物质的量浓度的溶液 不作反应器,不可加热,瓶塞不可互换,不宜存放溶液,要在所标记的温度下使用 用作过滤或向小口容器中注入液体 过滤时应“一贴二低三靠” 分离密度不同且互不相溶的液体;作反应器的随时加液装置 分液时,下层液体从下口放出,上层液体从上口倒出;不宜盛碱性液体 用作热源,火焰温度为500℃~600℃ 所装酒精量不能超过其容积的2/3,但也不能少于1/4。加热时要用外焰。熄灭时要用盖盖灭,不能吹灭 二.化学实验安全 (1)做有毒气体的实验时,应在通风厨中进行,并注意对尾气进行适当处理(吸收或点燃等)。进行易燃易爆气体的实验时应注意验纯,尾气应燃烧掉或作适当处理。 (2)浓酸沾在皮肤上,立即用大量水冲洗,再涂上3%~5%的NaHCO3溶液。浓酸溅在眼中应先用稀NaHCO3溶液淋洗,然后请医生处理。 (3)浓碱沾在皮肤上,宜先用大量水冲洗,再涂上硼酸溶液。浓碱溅在眼中,用水洗净后再用硼酸溶液淋洗。 (4)钠、磷等失火宜用沙土扑盖。 (5)酒精及其他易燃有机物小面积失火,应迅速用湿抹布扑盖。 (6)若水银温度计破裂,应在汞珠上撒上硫粉 三.离子检验 Fe3+ 取待测物质加入 KSCN溶液 ,溶液变红色;或滴入NaOH溶液,产生红褐色沉淀,说明含有Fe3+ Fe2+ 取待测物质加入 KSCN溶液 ,无现象,再滴入新制氯水时,溶液呈红色;或滴入NaOH溶液,产生白色沉淀,白色沉淀迅速变成灰绿色,最后变成红褐色,说明含有Fe2+ CO32— 、HCO3— 待测物质中滴加 稀盐酸 ,产生能使澄清石灰水变浑浊的无色无味气体,则证明含有CO32— 或HCO3— NH4+ 取待测物质加 NaOH溶液,加热,如果有 能使湿润的红石蕊试纸变蓝的气体 产生,则证明含有铵根离子 SO42— 取待测物质加入 稀盐酸 无现象,再滴入 BaCl2溶液 ,有白色沉淀生成,则证明含有SO42—- Cl— 取待测物质加入 稀硝酸 无现象,再滴入 AgNO3溶液 ,有白色沉淀生成,,则证明含有Cl— 焰色反应 钠焰色:黄色;钾的焰色:紫色 (透过蓝色钴玻璃)。 四. 一定物质的量浓度的配制 (1) 1计算.2称量.3溶解.4转移.5洗涤.6定容.7摇匀8贮存溶液. (2)主要仪器:容量瓶,烧杯,玻璃棒,胶头滴管 (3)注意事项: A 选用与欲配制溶液体积相同的容量瓶. B 使用前必须检查是否漏水. C 不能在容量瓶内直接溶解. D 溶解完的溶液等冷却至室温时再转移. E 定容时,当液面离刻度线1―2cm时改用滴管,以平视法观察加水至液面最低处与刻度相切为止. 五. 氨气制备 原理:铵盐和碱共热产生氨气 方程式:2NH4Cl+Ca(OH)22NH3↑+2H2O+CaCl2 装置:和氧气的制备装置一样 收集:向下排空气法(不能用排水法,因为氨气极易溶于水) (注意:收集试管口有一团棉花,防止空气对流,减缓排气速度,收集较纯净氨气) 验证氨气是否收集满:用湿润的红色石蕊试纸靠近试管口,若试纸变蓝说明收集满 干燥:碱石灰(CaO和NaOH的混合物) ... ...
~~ 您好,已阅读到文档的结尾了 ~~