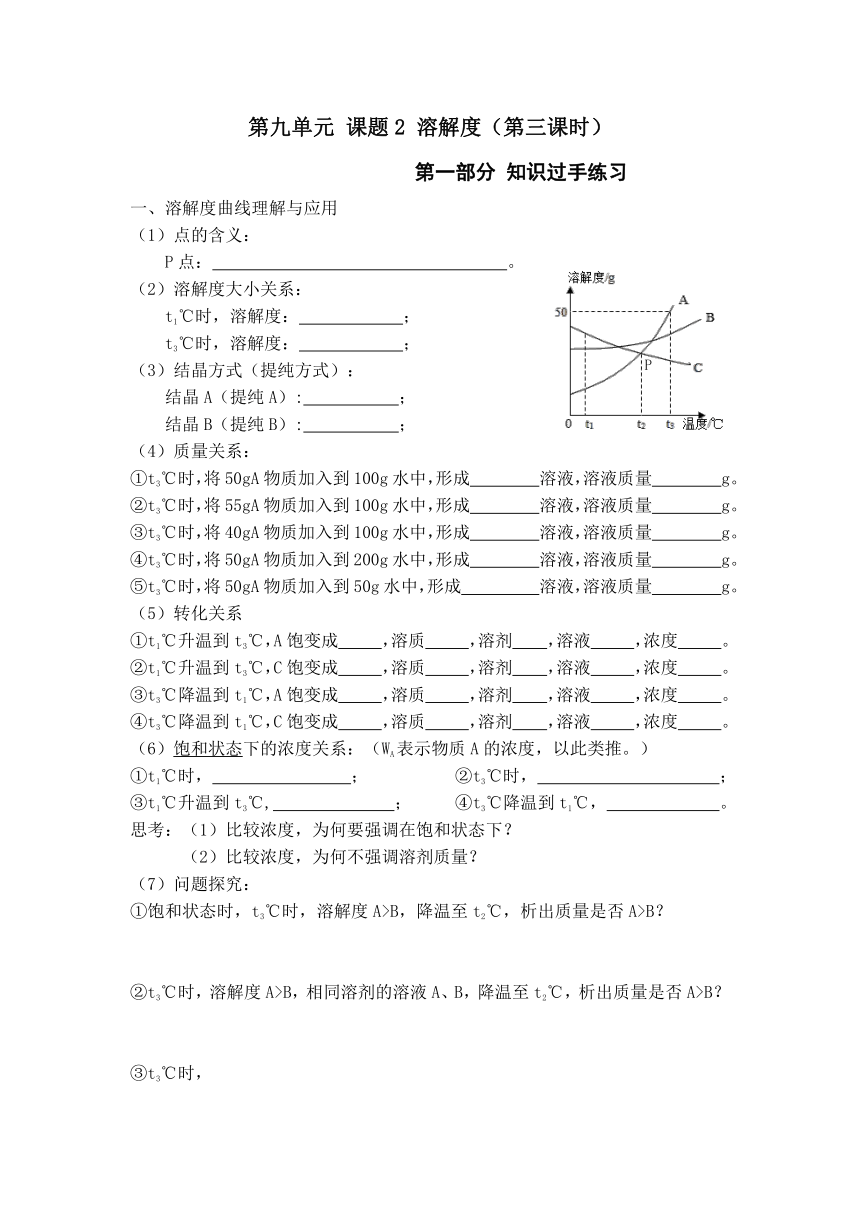
第九单元 课题2 溶解度(第三课时) 第一部分 知识过手练习 一、溶解度曲线理解与应用 (1)点的含义: P点: 。 (2)溶解度大小关系: t1℃时,溶解度: ; t3℃时,溶解度: ; (3)结晶方式(提纯方式): 结晶A(提纯A): ; 结晶B(提纯B): ; (4)质量关系: ①t3℃时,将50gA物质加入到100g水中,形成 溶液,溶液质量 g。 ②t3℃时,将55gA物质加入到100g水中,形成 溶液,溶液质量 g。 ③t3℃时,将40gA物质加入到100g水中,形成 溶液,溶液质量 g。 ④t3℃时,将50gA物质加入到200g水中,形成 溶液,溶液质量 g。 ⑤t3℃时,将50gA物质加入到50g水中,形成 溶液,溶液质量 g。 (5)转化关系 ①t1℃升温到t3℃,A饱变成 ,溶质 ,溶剂 ,溶液 ,浓度 。 ②t1℃升温到t3℃,C饱变成 ,溶质 ,溶剂 ,溶液 ,浓度 。 ③t3℃降温到t1℃,A饱变成 ,溶质 ,溶剂 ,溶液 ,浓度 。 ④t3℃降温到t1℃,C饱变成 ,溶质 ,溶剂 ,溶液 ,浓度 。 (6)饱和状态下的浓度关系:(WA表示物质A的浓度,以此类推。) ①t1℃时, ; ②t3℃时, ; ③t1℃升温到t3℃, ; ④t3℃降温到t1℃, 。 思考:(1)比较浓度,为何要强调在饱和状态下? (2)比较浓度,为何不强调溶剂质量? (7)问题探究: ①饱和状态时,t3℃时,溶解度A>B,降温至t2℃,析出质量是否A>B? ②t3℃时,溶解度A>B,相同溶剂的溶液A、B,降温至t2℃,析出质量是否A>B? ③t3℃时, 三种物质的饱和溶液各100g,其中溶质大小关系?溶剂大小关系?若将温度降为t1℃,溶剂关系是否会发生变化? 第二部分 当堂作业练习 (在课后消化、巩固知识) 1.如图是三种物质的溶解度曲线,回答下列问题: (1)P点的含义: 。 (2)t3℃时,溶解度由大到小的顺序: 。 (3)t2℃时,将50gA物质加入到200g水中,充分溶解,所得溶液中溶质与溶液质量比为 。 (4)B中混有少量A,提纯B的方法为 。 (5)分别将t3℃时A、B饱和溶液降温到t2℃,析出晶体的质量大小关系为 。 ①A>B ②Ab>c 4.如图所示,室温下将120 g NaOH固体加入100 g水中,搅拌后固体全部溶解,放置一段时间恢复至室温后,析出10g固体。(忽略实验过程中水的损失) (1)丙中溶液为 (填“饱和”或“不饱和”)溶液。 (2)该实验说明NaOH溶于水会 (“放热”或“吸热”)。 (3)上述实验说明NaOH的溶解度曲线与图中的 (填“a”或“b”)相似。 (4)最终需要再加入 g水,才能使丙中剩余固体全部刚好溶解形成室温下的饱和溶液。 ... ...
~~ 您好,已阅读到文档的结尾了 ~~