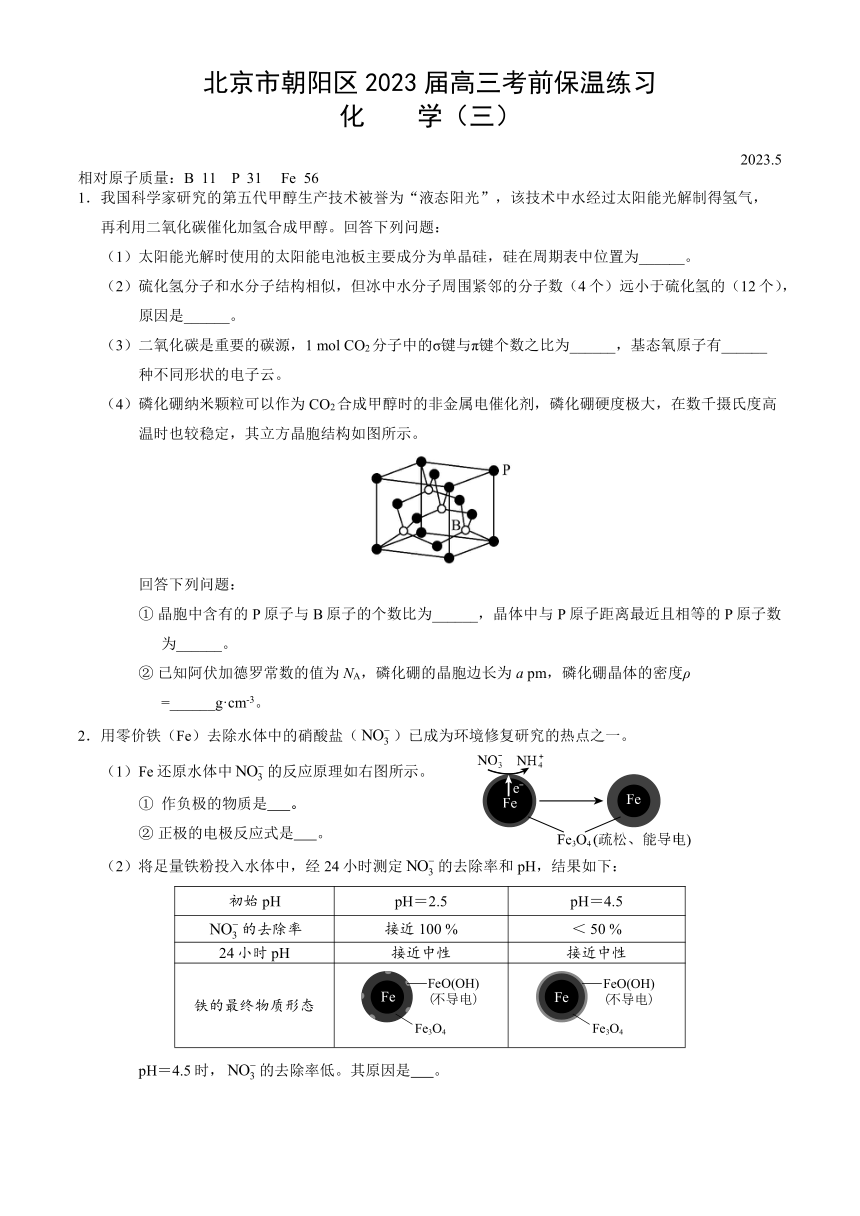
北京市朝阳区2023届高三考前保温练习 化 学(三) 2023.5 相对原子质量:B 11 P 31 Fe 56 1.我国科学家研究的第五代甲醇生产技术被誉为“液态阳光”,该技术中水经过太阳能光解制得氢气,再利用二氧化碳催化加氢合成甲醇。回答下列问题: (1)太阳能光解时使用的太阳能电池板主要成分为单晶硅,硅在周期表中位置为_____。 (2)硫化氢分子和水分子结构相似,但冰中水分子周围紧邻的分子数(4个)远小于硫化氢的(12个),原因是_____。 (3)二氧化碳是重要的碳源,1 mol CO2分子中的σ键与π键个数之比为_____,基态氧原子有_____种不同形状的电子云。 (4)磷化硼纳米颗粒可以作为CO2合成甲醇时的非金属电催化剂,磷化硼硬度极大,在数千摄氏度高温时也较稳定,其立方晶胞结构如图所示。 回答下列问题: ① 晶胞中含有的P原子与B原子的个数比为_____,晶体中与P原子距离最近且相等的P原子数为_____。 ② 已知阿伏加德罗常数的值为NA,磷化硼的晶胞边长为a pm,磷化硼晶体的密度ρ =_____g·cm-3。 2.用零价铁(Fe)去除水体中的硝酸盐()已成为环境修复研究的热点之一。 (1)Fe还原水体中的反应原理如右图所示。 ① 作负极的物质是 。 ② 正极的电极反应式是 。 (2)将足量铁粉投入水体中,经24小时测定的去除率和pH,结果如下: 初始pH pH=2.5 pH=4.5 的去除率 接近100 % < 50 % 24小时pH 接近中性 接近中性 铁的最终物质形态 pH=4.5时,的去除率低。其原因是 。 (3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高的去除率。对Fe2+的作用提出两种假设: Ⅰ.直接还原; Ⅱ.破坏FeO(OH)氧化层。 ① 做对比实验,结果如右图所示。可得到的结论是 。 ② 同位素示踪法证实能与FeO(OH)反应生成Fe3O4。结合该反应的离子方程式,解释加入提高去除率的原因: 。 (4)其他条件与(2)相同,经1小时测定的去除率和pH,结果如下: 初始pH pH=2.5 pH=4.5 的去除率 约10 % 约3 % 1小时pH 接近中性 接近中性 与(2)中数据对比,解释(2)中初始pH不同时,去除率和铁的最终物质形态不同的原因: 。 3.化合物K是制备药物那可汀的重要中间体,合成路线如下。 已知:ⅰ. ⅱ. 回答下列问题: (1)化合物A中的官能团名称为_____。 (2)A→B的化学方程式是_____。 (3)试剂a的结构简式为_____。 (4)从官能团转化的角度分析,先进行A→B,再进行B→C→D的原因是_____。 (5)下列关于有机物E的说法不正确的是(填序号)_____。 a.存在手性碳原子 b.存在含酚羟基的环状酯类同分异构体 c.可以发生加成、取代、聚合等反应 d.可用酸性高锰酸钾鉴别有机物E和F (6)化合物K的一种同分异构体同时满足下列条件,写出其结构简式:_____。 ① 分子中含有硝基且直接连在苯环上; ② 核磁共振氢谱中只有3组峰。 (7)化合物G经三步反应合成K,依次写出G、中间产物1的结构简式和无机试剂b的化学式_____、_____、_____。 4.Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下: 回答下列问题: (1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的浸出率为70%时,所采用的实验条件为_____。 (2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式_____。 (3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示: 分析40 ℃时TiO2·xH2O转化率最高的原因_____。 (4)若“滤液②”中c(Mg2+)=0.02 mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全,此时是否有Mg3(PO4)2沉淀生成? (列式计算)。FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-2 ... ...
~~ 您好,已阅读到文档的结尾了 ~~

