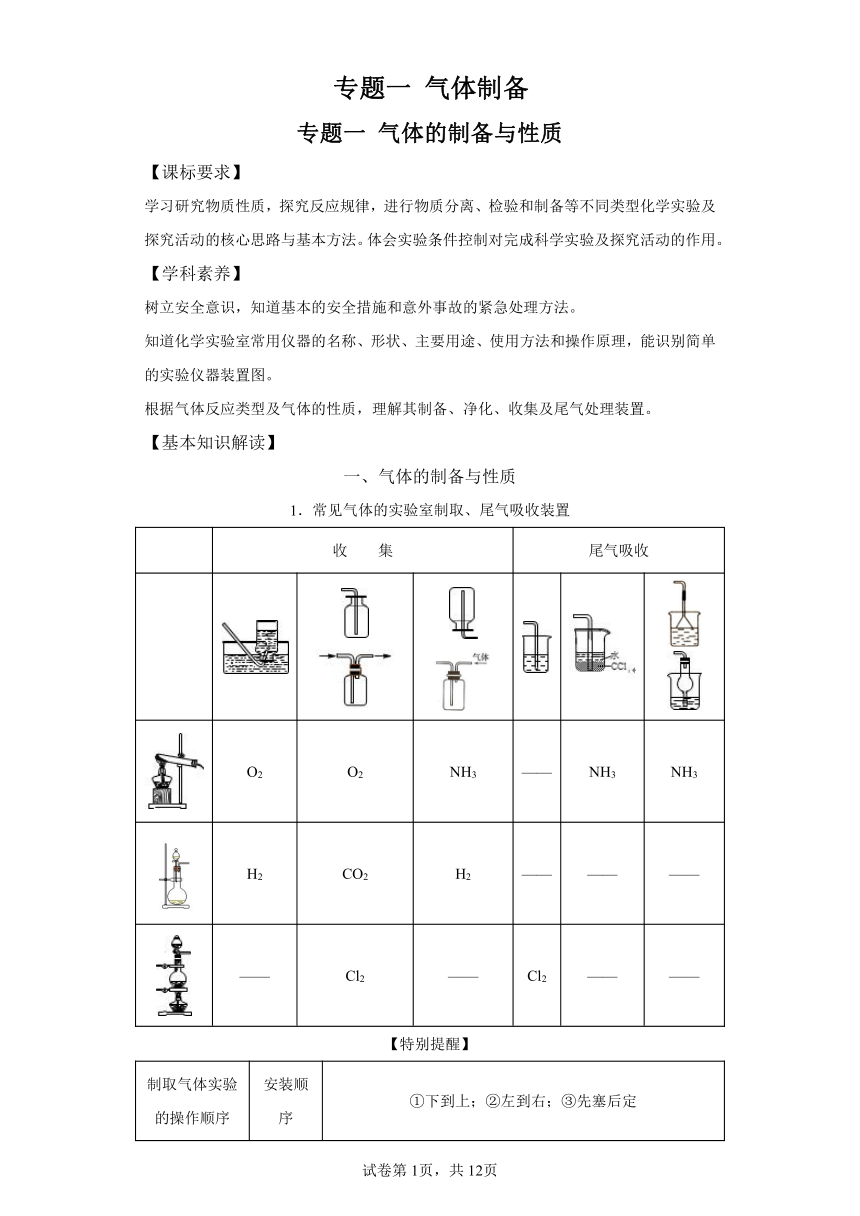
专题一 气体制备 专题一 气体的制备与性质 【课标要求】 学习研究物质性质,探究反应规律,进行物质分离、检验和制备等不同类型化学实验及探究活动的核心思路与基本方法。体会实验条件控制对完成科学实验及探究活动的作用。 【学科素养】 树立安全意识,知道基本的安全措施和意外事故的紧急处理方法。 知道化学实验室常用仪器的名称、形状、主要用途、使用方法和操作原理,能识别简单的实验仪器装置图。 根据气体反应类型及气体的性质,理解其制备、净化、收集及尾气处理装置。 【基本知识解读】 一、气体的制备与性质 1.常见气体的实验室制取、尾气吸收装置 收 集 尾气吸收 O2 O2 NH3 ——— NH3 NH3 H2 CO2 H2 ——— ——— ——— ——— Cl2 ——— Cl2 ——— ——— 【特别提醒】 制取气体实验的操作顺序 安装顺序 ①下到上;②左到右;③先塞后定 加试剂顺序 先固后液 其它操作顺序 先查气密性,后装药品(便于在装置漏气时进行调整和更换仪器),最后点酒精灯(所有装备工作完毕后). 实验装置 四部分 发生装置→净化装置→收集装置→尾气处理 2.物质的干燥 气体的干燥 ①浓硫酸:可干燥酸性气体、中性气体(如SO2、Cl2、H2、O2等),不能干燥碱性气体和还原性气体(如NH3、H2S等) ②碱石灰:可干燥碱性气体、中性气体(如NH3、H2、O2等),不能干燥酸性气体(如HCl) ③CaCl2:酸性、碱性、中性气体都可以干燥,但不能干燥NH3(CaCl2与NH3反应生成CaCl2·8NH3) 3.化学实验安全操作的“六防” 防爆炸 ①点燃可燃性气体(如H2、CO、CH4、C2H4)或用CO、H2还原Fe2O3、CuO之前,要验气体纯度②用H2或CO还原CuO时,应先通入H2或CO,在装置尾部收集气体并检验纯度,若尾部气体已纯净,说明装置中的空气已排尽,可对装置加热 防暴沸 配制硫酸的水溶液或硫酸的酒精溶液时,要将密度大的浓硫酸缓慢倒入水或酒精中;加热液体混合物时要加沸石或碎瓷片 防倒吸 用试管加热固体时,试管底部要略高于管口,如实验室制O2、NH3等;加热液体时试管口要向上倾斜;加热法制取并用排水法收集气体或吸收溶解度较大的气体时,要注意撤导管和熄灯顺序或加装安全瓶 防失火 ①可燃性物质如钾、钠、白磷等强还原剂要妥善保存,与强氧化剂要分开存放②使用易挥发性可燃物,如乙醇、乙醚、汽油等应防止蒸气逸出,添加易燃品一定要远离火源 防中毒 制取有毒气体(如Cl2、CO、SO2、H2S、NO2、NO)时,应在通风橱中进行,且进行尾气处理 防污染 用胶头滴管滴加液体时,不伸入瓶内,不接触试管壁(向FeSO4溶液中加NaOH溶液除外);取用试剂时试剂瓶盖倒放于桌面上;药匙和胶头滴管尽可能专用(或洗净、擦干后再取其他试剂);废液及时处理;凡有污染性气体(如Cl2、SO2、CO、NOx等)产生的均需对尾气进行吸收或处理 4.装置气密性的检查 方法 微热法 液差法 气压法 原理 升高装置中气体的温度,使气体体积膨胀 缩小装置中气体的体积,增大压强 封闭气体,压强增大,使液滴不能滴下 图示 具体操作 塞紧橡胶塞,将导气管末端伸入盛水的烧杯中,用手捂热(或用酒精灯微热)烧瓶 塞紧橡胶塞,用止水夹夹住导气管的橡胶管部分,从长颈漏斗向试管中注水 塞紧橡胶塞,用止水夹夹住导气管的橡胶管部分,打开分液漏斗活塞,向烧瓶中加水 现象说明 烧杯中有气泡产生,将手拿开(或停止微热),冷却后导气管末端形成一段水柱,且保持一段时间不下降 停止加水后,长颈漏斗中的液面高于试管中的液面,且一段时间内液面差不变 一段时间后,液滴不能滴下 【核心考点例题】 高频考点一 气体的制备与性质 (2022·西藏·高二统考学业考试) 1.下列关于氨气的说法中,不正确的是 A.实验室可用浓氨水和生石灰制取氨气 B.氨气可用浓硫酸干燥 C.氨气能使湿润的红色石蕊试纸变蓝 D.氨常用作制冷 ... ...
~~ 您好,已阅读到文档的结尾了 ~~