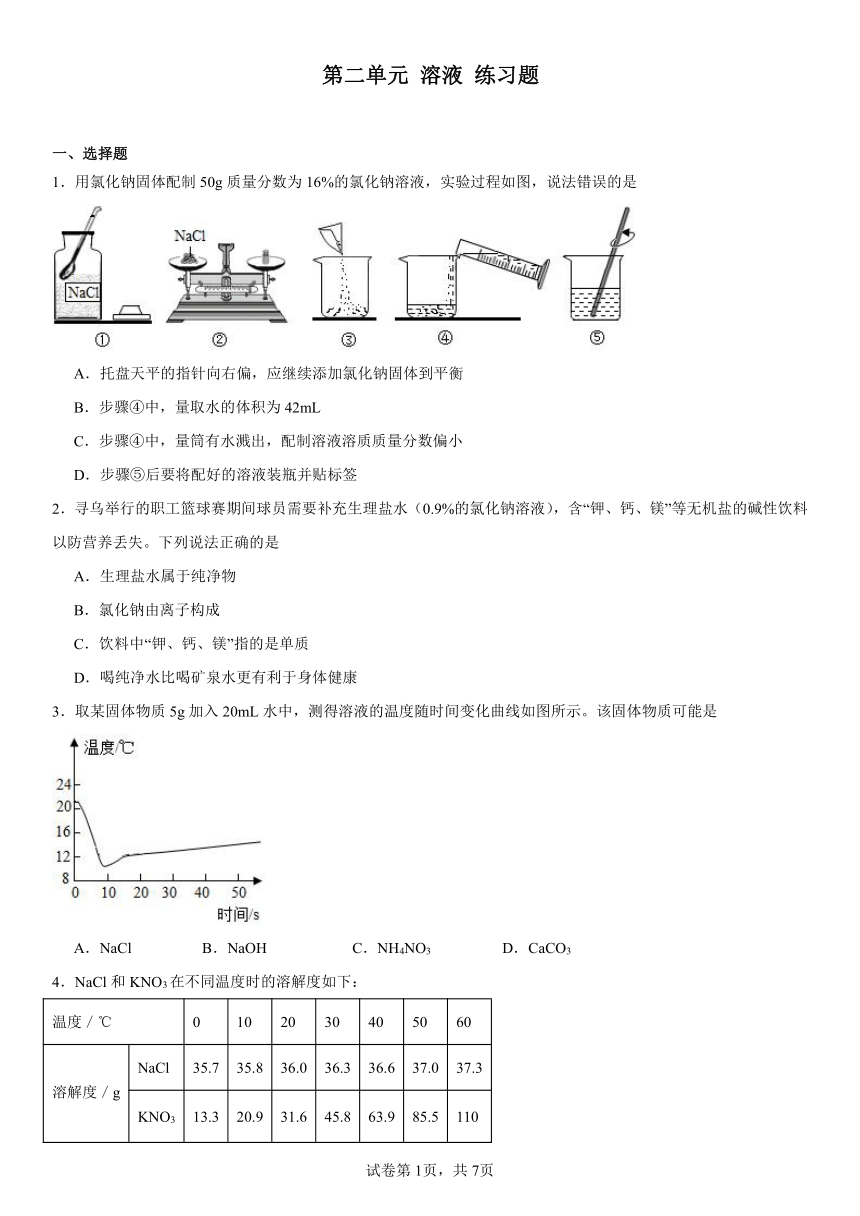
第二单元 溶液 练习题 一、选择题 1.用氯化钠固体配制50g质量分数为16%的氯化钠溶液,实验过程如图,说法错误的是 A.托盘天平的指针向右偏,应继续添加氯化钠固体到平衡 B.步骤④中,量取水的体积为42mL C.步骤④中,量筒有水溅出,配制溶液溶质质量分数偏小 D.步骤⑤后要将配好的溶液装瓶并贴标签 2.寻乌举行的职工篮球赛期间球员需要补充生理盐水(0.9%的氯化钠溶液),含“钾、钙、镁”等无机盐的碱性饮料以防营养丢失。下列说法正确的是 A.生理盐水属于纯净物 B.氯化钠由离子构成 C.饮料中“钾、钙、镁”指的是单质 D.喝纯净水比喝矿泉水更有利于身体健康 3.取某固体物质5g加入20mL水中,测得溶液的温度随时间变化曲线如图所示。该固体物质可能是 A.NaCl B.NaOH C.NH4NO3 D.CaCO3 4.NaCl和KNO3在不同温度时的溶解度如下: 温度/℃ 0 10 20 30 40 50 60 溶解度/g NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 下列说法正确的是 A.10℃时,将40g NaCl固体加入l00g水中,可得到l40gNaCl溶液 B.KNO3和NaCl的溶解度受温度的影响都很大 C.将30℃的KNO3饱和溶液升温至60℃,会变成不饱和溶液 D.20℃时,NaCl饱和溶液的溶质质量分数为36% 5.将质量分数为60%的乙醇溶液(密度小于1)与等体积的水混合后,则所得溶液的质量分数为: A.等于30% B.大于30% C.小于30% D.等于35% 6.NaCl 与 KNO3 在不同温度时的溶解度如下表,下列说法正确的是( ) 物质/溶解度g/温度℃ 0 20 40 60 80 100 NaCl 35.7 36.0 36.6 37.3 38.4 39.8 KNO3 13.3 31.6 63.9 110 169 246 A.时,NaCl的溶解度为 B.中混有少量NaCl,可用蒸发结晶的方法提纯 C.在 时,可以配制出溶质质量分数相等的NaCl和的饱和溶液 D.时,用等质量的NaCl和配制饱和溶液,所得溶液质量大于NaCl 7.如图是A、B、C三种物质的溶解度随温度的变化趋势。则下列说法正确的是( ) A.t1℃时ABC三种物质的溶解度由大到小的顺序是A>C>B B.t1℃时30g A物质加入50g水中不断搅拌,形成的溶液质量是80g C.A、B两种物质的混合溶液可通过蒸发结晶的方式提纯A D.将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数的大小关系是B>C>A 8.甲、乙两种物质的溶解度曲线如图所示,下列有关叙述正确的是 A.t1℃时,甲、乙溶液的溶质质量分数相等 B.t1℃时,甲的饱和溶液中含50g溶质 C.t1℃时,甲的饱和溶液升高温度后,其溶解度变大, 溶质质量分数不变 D.甲物质的溶解度大于乙物质的溶解度 9.以下关于溶液的叙述,不正确的是( ) A.溶液是均匀、稳定的混合物 B.溶液不一定是无色液体 C.正在配制的蔗糖溶液下面更甜,说明溶液总是下面更浓 D.如果水不蒸发,温度不变,糖水放再长时间,蔗糖也不会分离 10.将接近饱和的石灰水变成饱和溶液,不可行的方法是( ) A.加入CaO B.加入 C.升高温度 D.加入CaCO3 11.溶液在我们生活中有着广泛的应用,下列物质不属于溶液的是( ) A.矿泉水 B.冰水 C.碘酒 D.白醋 12.20℃时50克水中最多可溶解5克A物质,20℃时100克水中最多可溶解10克B物质,则20℃时A和B的溶解度相比 A. B. C. D.无法比较 13.甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法正确的是 A.甲、乙、丙的溶解度都随温度的升高而增大 B.t1℃时,甲、丙饱和溶液的溶质质量分数相等 C.将t2℃时乙的饱和溶液降低温度至t1℃有晶体析出 D.将t2℃时乙、丙两种物质的饱和溶液升温至t3℃,溶质质量分数不变的是丙溶液 14.60℃时,100g硝酸钾的饱和溶液,恒温下蒸发部分溶剂,然后再将溶液逐渐冷却到40℃。能表示此过程溶质质量分数a%与时间t关系的示意图是 ... ...
~~ 您好,已阅读到文档的结尾了 ~~

