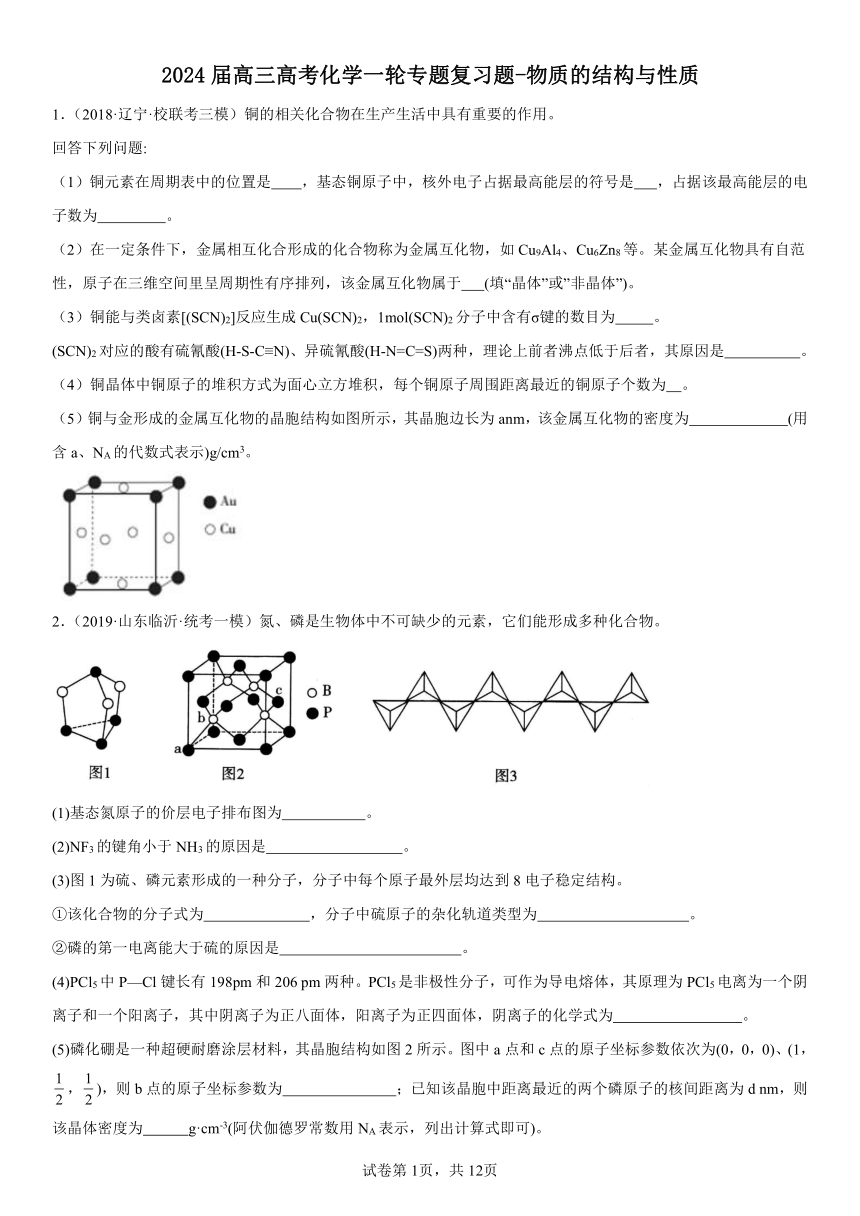
2024届高三高考化学一轮专题复习题-物质的结构与性质 1.(2018·辽宁·校联考三模)铜的相关化合物在生产生活中具有重要的作用。 回答下列问题: (1)铜元素在周期表中的位置是 ,基态铜原子中,核外电子占据最高能层的符号是 ,占据该最高能层的电子数为 。 (2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu6Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于 (填“晶体”或”非晶体”)。 (3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为 。 (SCN)2对应的酸有硫氰酸(H-S-C≡N)、异硫氰酸(H-N=C=S)两种,理论上前者沸点低于后者,其原因是 。 (4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为 。 (5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为anm,该金属互化物的密度为 (用含a、NA的代数式表示)g/cm3。 2.(2019·山东临沂·统考一模)氮、磷是生物体中不可缺少的元素,它们能形成多种化合物。 (1)基态氮原子的价层电子排布图为 。 (2)NF3的键角小于NH3的原因是 。 (3)图1为硫、磷元素形成的一种分子,分子中每个原子最外层均达到8电子稳定结构。 ①该化合物的分子式为 ,分子中硫原子的杂化轨道类型为 。 ②磷的第一电离能大于硫的原因是 。 (4)PCl5中P—Cl键长有198pm和206 pm两种。PCl5是非极性分子,可作为导电熔体,其原理为PCl5电离为一个阴离子和一个阳离子,其中阴离子为正八面体,阳离子为正四面体,阴离子的化学式为 。 (5)磷化硼是一种超硬耐磨涂层材料,其晶胞结构如图2所示。图中a点和c点的原子坐标参数依次为(0,0,0)、(1,,),则b点的原子坐标参数为 ;已知该晶胞中距离最近的两个磷原子的核间距离为d nm,则该晶体密度为 g·cm-3(阿伏伽德罗常数用NA表示,列出计算式即可)。 (6)某直链多磷酸钠的阴离子呈如图3所示的无限单链状结构,其中磷氧四面体通过共用顶角氧原子相连。则该多磷酸钠的化学式为 。 3.(2019上·湖北·高三校联考期中)氢原子是最轻的原子,人们曾预言它可能是所有元素之母。学习物质结构与性质,回答下列问题: (1)太阳中的主要化学元素是氢和 。 (2)氢负离子H-基态电子排布式为 。 (3)下列变化:H-(g)=H(g)+e-吸收的能量为73kJ/mol,H(g)=H+(g)+e-吸收的能量为1311kJ/mol,则氢负离子H-的第一电离能为 。 (4)几种碱金属氢化物的部分性质如下表所示: 氢化物 LiH NaH KH 密度/g/cm3 0.78 1.43 分解温度/℃ 850 425 400 从化学结构的角度回答说明,分解温度LiH>NaH>KH 。 (5)水溶液中有H3O+、H5O2+、H9O4+等微粒的形式。H3O+中,中心原子的杂化类型是 ,请画出H5O2+的结构式: 。当用高能射线照射液态水时,水分子便以一种新的方式电离,如图所示写出高能射线照射水的总反应的离子方程式 。 (6)氢化铝钠(NaAlH4)等复合氢化物是重要的有机还原剂。NaAlH4晶胞结构如图所示,NaAlH4晶体中,与Na+紧邻且等距的A1H4-有 个,设阿伏加 德罗常数为NA,则晶体的密度为 g·cm-3。 (7)在立方晶胞中与晶胞体对角线垂直的面在晶体学中称为(1,1,1)晶面。如图则该立方晶胞体中(1,1,1)晶面共有 个。 4.(2022上·广东东莞·高二东莞实验中学校考期中)前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B原子s能级的电子总数比p能级的多1;基态C原子中成对电子数均是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小;元素E是第四周期中未成对电子数最多的元素,回答下列问题: (1)基态E原子的价层电子轨道表示式为 。 (2)写出A与C原子个数比为1:1的化合物的电子式: ,该化合 ... ...
~~ 您好,已阅读到文档的结尾了 ~~

