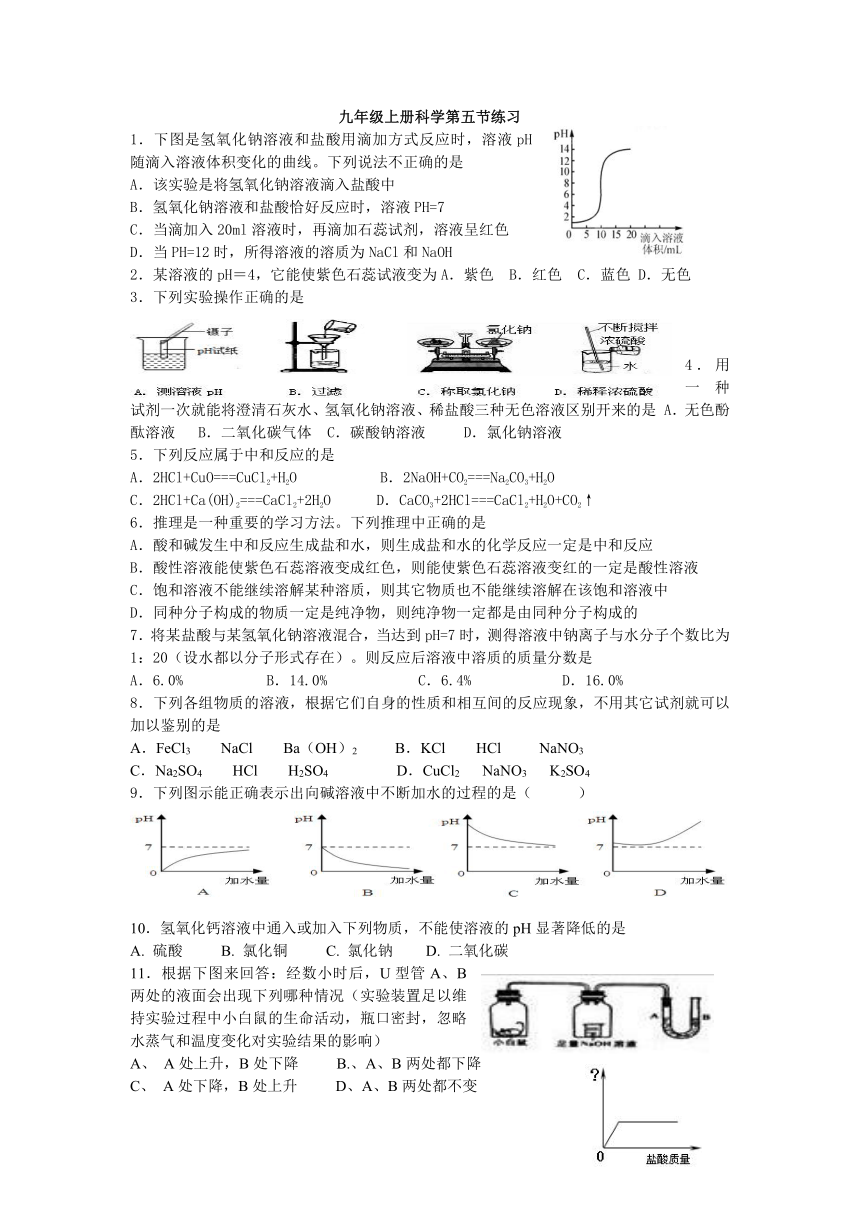
九年级上册科学第五节练习 1.下图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。下列说法不正确的是 A.该实验是将氢氧化钠溶液滴入盐酸中 B.氢氧化钠溶液和盐酸恰好反应时,溶液PH=7 C.当滴加入20ml溶液时,再滴加石蕊试剂,溶液呈红色 D.当PH=12时,所得溶液的溶质为NaCl和NaOH 2.某溶液的pH=4,它能使紫色石蕊试液变为A.紫色 B.红色 C.蓝色 D.无色 3.下列实验操作正确的是 4.用一种试剂一次就能将澄清石灰水、氢氧 出卷网化钠溶液、稀盐酸三种无色溶液区别开来的是 A.无色酚酞溶液 B.二氧化碳气体 C.碳酸钠溶液 D.氯化钠溶液 5.下列反应属于中和反应的是 A.2HCl+CuO===CuCl2+H2O B.2NaOH+CO2===Na2CO3+H2O C.2HCl+Ca(OH)2===CaCl2+2H2O D.CaCO3+2HCl===CaCl2+H2O+CO2↑ 6.推理是一种重要的学习方法。下列推理中正确的是 A.酸和碱发生中和反应生成盐和水,则生成盐和水的化学反应一定是中和反应 B.酸性溶液能使紫色石蕊溶液变成红色,则能使紫色石蕊溶液变红的一定是酸性溶液 C.饱和溶液不能继续溶解某种溶质,则其它物质也不能继续溶解在该饱和溶液中 D.同种分子构成的物质一定是纯净物,则纯净物一定都是由同种分子构成的 7.将某盐酸与某氢氧化钠溶液混合,当达到p 出卷网H=7时,测得溶液中钠离子与水分子个数比为1:20(设水都以分子形式存在)。则反应后溶液中溶质的质量分数是 A.6.0% B.14.0% C.6.4% D.16.0% 8.下列各组物质的溶液,根据它们自身的性质和相互间的反应现象,不用其它试剂就可以加以鉴别的是 A.FeCl3 NaCl Ba(OH)2 B.KCl HCl NaNO3 C.Na2SO4 HCl H2SO4 D.CuCl2 NaNO3 K2SO4 9.下列图示能正确表示出向碱溶液中不断加水的过程的是( ) 10.氢氧化钙溶液中通入或加入下列物质,不能使溶液的pH显著降低的是 A. 硫酸 B. 氯化铜 C. 氯化钠 D. 二氧化碳 11.根据下图来回答:经数小时后,U型管A 出卷网、B两处的液面会出现下列哪种情况(实验装置足以维持实验过程中小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响) A、 A处上升,B处下降 B.、A、B两处都下降 C、 A处下降,B处上升 D、A、B两处都不变 12.下图是在一定量氢氧化钠溶液中不断加入盐酸的曲线图。纵坐标能表示的意义是 A.溶液温度变化 B.生成氯化钠的质量 C.溶液中水的质量 D.溶液中氯化氢的质量 13.为测定一瓶氢氧化钠溶 出卷网液的质量分数,小张同学进行了以下实验:如图1所示,在烧杯中加入5g氢氧化钠溶液,滴入几滴酚酞溶液,用滴管慢慢滴入1% 的稀盐酸,并不断搅拌,至溶液颜色恰好变为无色为止。请回答: (1)酚酞溶液的作用是 。 (2)当溶液颜色恰好变为无色时,共用去稀盐酸7.3g,则该氢氧化钠溶液中溶质的质量分数为 。 (3)在以上实验操作中,如继续滴加1% 出卷网稀盐酸,并不断搅拌,则整个实验过程中溶液pH的变化曲线如图2所示。①a点表示的含义是 ; ②b点溶液中含有的阳离子有 (填离子符号)。 (4)下图是盐酸滴入氢氧化钠溶液中有关粒子之间反应的示意图。由此可看出,盐酸与氢氧化钠能发生反应的原因是 。 14.某化学兴趣小组用下图所示装置进行实验(装置的气密性良好)。 (1)如图1所示,让瓶内充满二氧化 出卷网碳气体,先向广口瓶中加入A的溶液,振荡广口瓶,气球膨胀;再向广口瓶中滴加B中的溶液,振荡广口瓶,气球又缩小,如此重复操作,气球可以反复膨胀和缩小。则:①分液漏斗A中可能是____溶液, 反应的化学方程式是 。②分液漏斗B中可能是_____溶液。 (2)如图2所示,将滴管甲中的液体 出卷网挤出,气球明显鼓起,一段时间后恢复原状;再将滴管乙中的液体挤出,气球有明显鼓起且不恢复原状。则滴管甲、乙和烧杯①、 ... ...
~~ 您好,已阅读到文档的结尾了 ~~