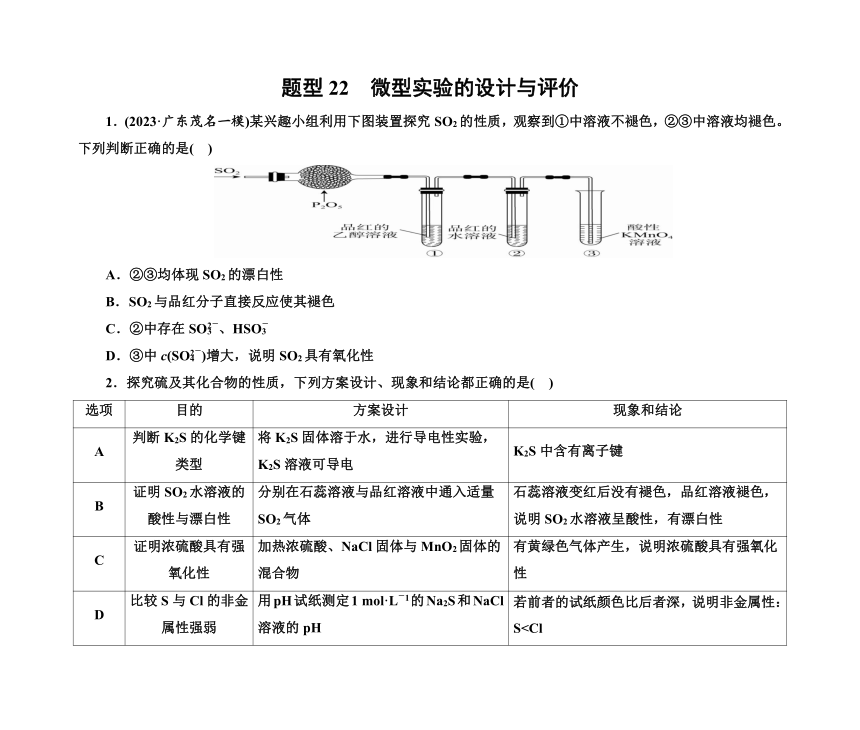
题型22 微型实验的设计与评价 1.(2023·广东茂名一模)某兴趣小组利用下图装置探究SO2的性质,观察到①中溶液不褪色,②③中溶液均褪色。下列判断正确的是( ) A.②③均体现SO2的漂白性 B.SO2与品红分子直接反应使其褪色 C.②中存在SO、HSO D.③中c(SO)增大,说明SO2具有氧化性 2.探究硫及其化合物的性质,下列方案设计、现象和结论都正确的是( ) 选项 目的 方案设计 现象和结论 A 判断K2S的化学键类型 将K2S固体溶于水,进行导电性实验,K2S溶液可导电 K2S中含有离子键 B 证明SO2水溶液的酸性与漂白性 分别在石蕊溶液与品红溶液中通入适量SO2气体 石蕊溶液变红后没有褪色,品红溶液褪色,说明SO2水溶液呈酸性,有漂白性 C 证明浓硫酸具有强氧化性 加热浓硫酸、NaCl固体与MnO2固体的混合物 有黄绿色气体产生,说明浓硫酸具有强氧化性 D 比较S与Cl的非金属性强弱 用pH试纸测定1 mol·L-1的Na2S和NaCl溶液的pH 若前者的试纸颜色比后者深,说明非金属性:SKa(HClO) D 在I2的CCl4溶液中加入浓KI溶液,振荡 四氯化碳层紫红色变浅 I2在四氯化碳中的溶解度小于在KI溶液中的溶解度 4.(2023·江苏扬州统考一模)根据下列实验操作和现象得出的结论不正确的是( ) 选项 实验操作和现象 实验结论 A 向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀 X具有强氧化性 B 向0.1 mol·L-1 FeCl3溶液中滴加KI-淀粉溶液,溶液变蓝 氧化性:Fe3+>I2 C 向NaHCO3溶液中加入等浓度、等体积的NaAlO2溶液,出现白色沉淀 AlO比CO更容易结合H+ D 将溴乙烷、乙醇和烧碱的混合物加热,产生的气体经水洗后,再通入酸性KMnO4溶液中,溶液褪色 溴乙烷发生了消去反应 5.根据实验目的,下列实验及现象、结论都正确的是( ) 选项 实验目的 实验及现象 结论 A 探究有机物中官能团之间的影响 分别向丙烯酸乙酯和α 氰基丙烯酸乙酯中滴入水,前者无明显现象,后者快速固化 氰基活化双键,使其更易发生加聚反应 B 比较KMnO4、Cl2和Fe3+的氧化性 向酸性KMnO4溶液中滴入FeCl2溶液,紫红色溶液变浅并伴有黄绿色气体产生 氧化性:KMnO4>Cl2>Fe3+ C 纤维素水解实验 将脱脂棉放入试管中,滴入90%硫酸捣成糊状,30 s后用NaOH溶液调至碱性,加入新制的Cu(OH)2悬浊液,无砖红色沉淀产生 纤维素未发生水解 D 探究不同价态硫元素之间的转化 向Na2SO3和Na2S混合溶液中加入浓硫酸,溶液中出现黄色沉淀 +4价和-2价硫可归中为0价 6.(2023·山东淄博一模)根据下列操作及现象,所得结论正确的是( ) 选项 操作及现象 结论 A 向溶有SO2的BaCl2溶液中加入Fe(NO3)3溶液,有白色沉淀生成 说明NO具有强氧化性 B 向2 mL浓度均为0.1 mol·L-1的NaBr与Na2S混合溶液中滴加2滴0.1 mol·L-1的AgNO3溶液,只有黑色沉淀生成 说明Ag2S比AgBr更难溶 C 取4 mL乙醇,加入12 mL浓硫酸及少量沸石,迅速升温至170 ℃,将产生的气体通入2 mL溴水中,溴水褪色 说明乙醇消去反应的产物为乙烯 D 向丙烯醛中加入足量新制的氢氧化铜悬浊液,加热至不再生成砖红色沉淀,静置,向上层清液滴加溴水,溴水褪色 说明丙烯醛中含有碳碳双键 7.将铜丝插入浓硝酸中进行如图所示的实验,下列说法正确的是( ) A.装置a中出现红棕色气体,只体现HNO3的酸性 B.一段时间后抽出铜丝,向装置b注入水,b中气体红棕色变浅 C.注入水后装置b中铜片表面产生气泡,说明Cu与硝酸反应可生成H2 D.装置c用NaOH吸收尾气,说明NO和NO2均 ... ...
~~ 您好,已阅读到文档的结尾了 ~~