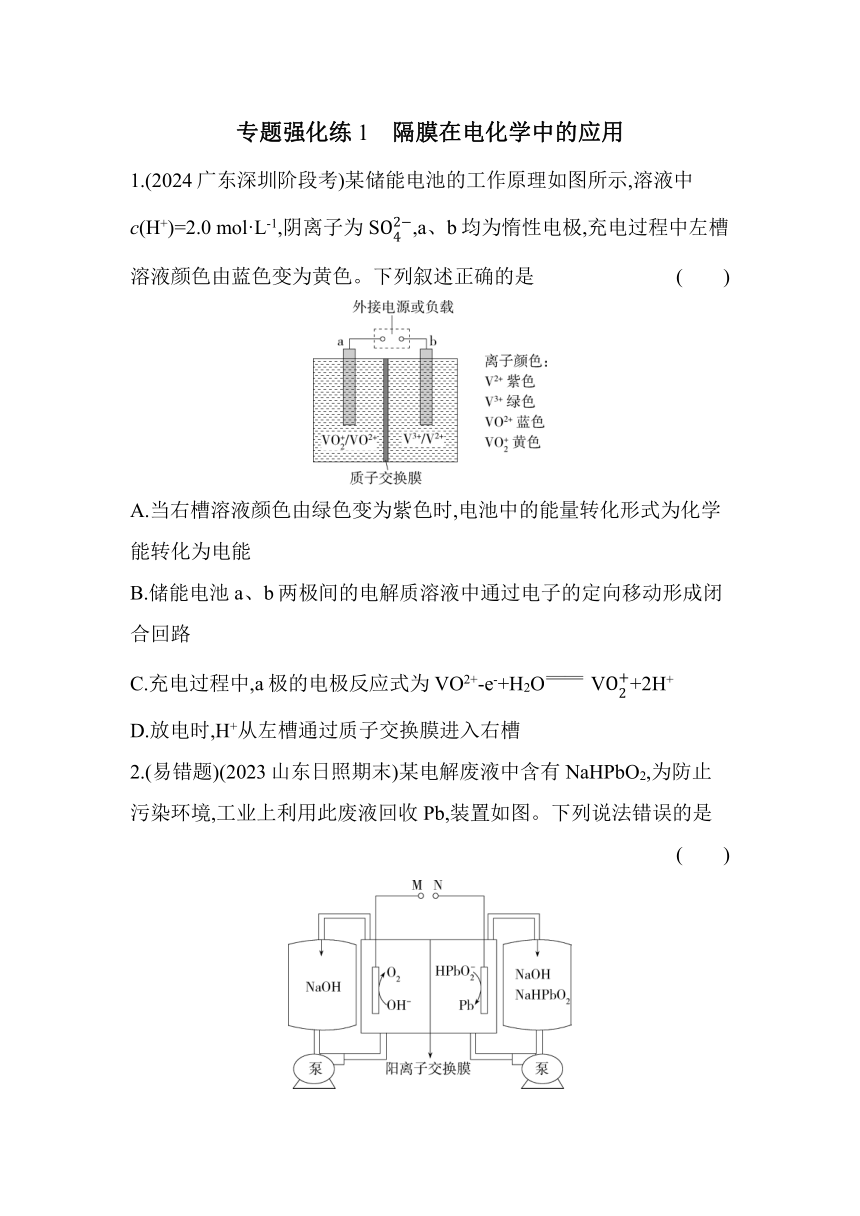
专题强化练1 隔膜在电化学中的应用 1.(2024广东深圳阶段考)某储能电池的工作原理如图所示,溶液中c(H+)=2.0 mol·L-1,阴离子为S,a、b均为惰性电极,充电过程中左槽溶液颜色由蓝色变为黄色。下列叙述正确的是 ( ) A.当右槽溶液颜色由绿色变为紫色时,电池中的能量转化形式为化学能转化为电能 B.储能电池a、b两极间的电解质溶液中通过电子的定向移动形成闭合回路 C.充电过程中,a极的电极反应式为VO2+-e-+H2O V+2H+ D.放电时,H+从左槽通过质子交换膜进入右槽 2.(易错题)(2023山东日照期末)某电解废液中含有NaHPbO2,为防止污染环境,工业上利用此废液回收Pb,装置如图。下列说法错误的是 ( ) A.M电极的电势高于N B.若电路中转移2 mol电子,阴极室溶液质量减少207 g C.阴极的电极反应式为HPb+2e-+H2O Pb+3OH- D.将阳离子交换膜换成阴离子交换膜,对Pb的产率无影响 3.(2024山东枣庄期末联考)双极膜(BP)是阴、阳复合膜,在直流电作用下,阴、阳膜复合层间的H2O解离成H+和OH-。利用双极膜电渗析法和惰性电极电解食盐水可获得淡水、NaOH溶液和盐酸,其工作原理如下图所示,M、N为离子交换膜。下列说法错误的是 ( ) A.M膜为阳离子交换膜 B.出口2的产物是盐酸 C.若去掉双极膜(BP),阳极室会有Cl2生成 D.电路中每转移1 mol电子,两极共得到0.5 mol气体 4.(2023福建龙岩一中月考)一种电解法制备高纯铬和硫酸的简单装置如图所示。回答下列问题: (1)b为直流电源的 极;阴极反应式为 。 (2)A膜为 离子交换膜,B膜为 离子交换膜(填“阴”或“阳”)。 (3)当外电路转移4 mol电子时,理论上丙中溶液质量减轻 g。 答案与分层梯度式解析 1.C 2.B 3.D 1.C 充电过程中左槽溶液颜色由蓝色变为黄色,则外接电源左侧为正极,右侧为负极,a为阳极,b为阴极,放电过程中a为正极,b为负极。当右槽溶液颜色由绿色变为紫色,V3+得到电子,化合价降低,发生还原反应,b作阴极,此时的能量转化形式为电能转化为化学能,A项错误;储能电池a、b两极间的电解质溶液中通过离子的定向移动形成闭合回路,B项错误;充电过程中,a为阳极,VO2+失去电子变成V,电极反应式为VO2+-e-+H2O V+2H+,C项正确;放电过程中H+移向正极,即从右槽通过质子交换膜进入左槽,D项错误。 方法点津 有“膜”条件下离子移动方向的判断方法 2.B 左侧电极上OH-失去电子生成O2,左侧电极为阳极,电极反应为4OH--4e- O2↑+2H2O,M为正极;右侧电极上HPb得到电子生成Pb,右侧电极为阴极,电极反应为HPb+2e-+H2O Pb+3OH-,N为负极,M电极的电势高于N,A正确;阴极电极反应为HPb+2e-+H2O Pb+3OH-,转移2 mol电子时,有2 mol Na+由左侧经阳离子交换膜到达右侧,阴极室溶液质量减少207 g-2 mol×23 g·mol-1=161 g,B错误、C正确;Na+由左侧经阳离子交换膜到达右侧,将阳离子交换膜换成阴离子交换膜,多余的OH-经阴离子交换膜由右侧到达左侧,对Pb的产率无影响,D正确。 易错分析 分析某室质量的变化,既要考虑该区的电极反应或化学反应,又要考虑通过隔膜的离子带来的质量变化,本题中电路中转移2 mol电子时,有1 mol Pb析出,溶液的质量减少207 g,同时Na+由左侧经阳离子交换膜到达右侧,溶液的质量增加2 mol×23 g·mol-1=46 g,即阴极室溶液减少的质量是二者的差。 3.D 根据图示信息可知,阴极反应式为2H2O+2e- H2↑+2OH-,阳极反应式为2H2O-4e- O2↑+4H+,总反应是电解水。由盐室得到的产物为淡水,知盐室中Na+经过M膜移向左侧产品室,Cl-经过N膜移向右侧产品室,出口2的产物是盐酸,A、B正确;若去掉双极膜(BP),Cl-会发生电极反应:2Cl--2e- Cl2↑,C正确;总的电极反应为2H2O 2H2↑+O2↑,每转移1 mol电子,两极共得到0.75 mol气体,D错误。 4.答案 (1)正 Cr3++3e- Cr (2)阴 阳 (3)36 解析 该装置制备高纯铬和硫酸, ... ...
~~ 您好,已阅读到文档的结尾了 ~~