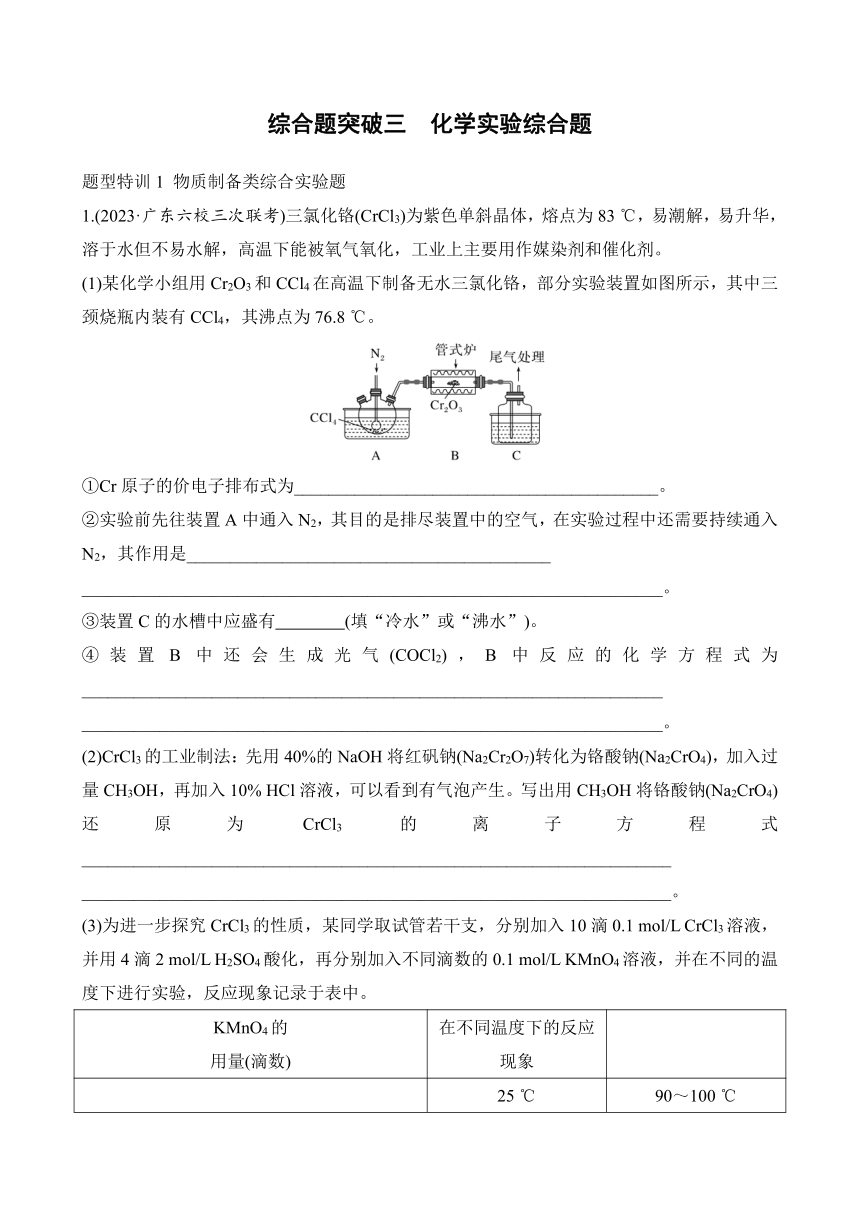
综合题突破三 化学实验综合题 题型特训1 物质制备类综合实验题 1.(2023·广东六校三次联考)三氯化铬(CrCl3)为紫色单斜晶体,熔点为83 ℃,易潮解,易升华,溶于水但不易水解,高温下能被氧气氧化,工业上主要用作媒染剂和催化剂。 (1)某化学小组用Cr2O3和CCl4在高温下制备无水三氯化铬,部分实验装置如图所示,其中三颈烧瓶内装有CCl4,其沸点为76.8 ℃。 ①Cr原子的价电子排布式为_____。 ②实验前先往装置A中通入N2,其目的是排尽装置中的空气,在实验过程中还需要持续通入N2,其作用是_____ _____。 ③装置C的水槽中应盛有 (填“冷水”或“沸水”)。 ④装置B中还会生成光气(COCl2),B中反应的化学方程式为_____ _____。 (2)CrCl3的工业制法:先用40%的NaOH将红矾钠(Na2Cr2O7)转化为铬酸钠(Na2CrO4),加入过量CH3OH,再加入10% HCl溶液,可以看到有气泡产生。写出用CH3OH将铬酸钠(Na2CrO4)还原为CrCl3的离子方程式_____ _____。 (3)为进一步探究CrCl3的性质,某同学取试管若干支,分别加入10滴0.1 mol/L CrCl3溶液,并用4滴2 mol/L H2SO4酸化,再分别加入不同滴数的0.1 mol/L KMnO4溶液,并在不同的温度下进行实验,反应现象记录于表中。 KMnO4的 用量(滴数) 在不同温度下的反应现象 25 ℃ 90~100 ℃ 1 紫红色 蓝绿色溶液 2~9 紫红色 黄绿色溶液,且随KMnO4滴数增加,黄色成分增多 10 紫红色 澄清的橙黄色溶液 11~23 紫红色 橙黄色溶液,有棕褐色沉淀,且随KMnO4滴数增加,沉淀增多 24~25 紫红色 紫红色溶液,有较多的棕褐色沉淀 ①温度对反应的影响。 CrCl3与KMnO4在常温下反应,观察不到Cr2O离子的橙色,甲同学认为其中一个原因是Cr2O离子的橙色被MnO离子的紫红色掩盖,另一种可能的原因是_____ _____, 所以必须将反应液加热至沸腾4~5 min后,才能观察到反应液由紫红色逐渐变为橙黄色的实验现象。 ②CrCl3与KMnO4的用量对反应的影响。 对表中数据进行分析,在上述反应条件下,欲将Cr3+氧化为Cr2O,CrCl3与KMnO4最佳用量比为 。这与由反应10Cr3++6MnO+11H2OCr2O+6Mn2++22H+所推断得到的用量比不符,你推测的原因是_____ _____。 2.(2023·梅州二模)Fe/Fe3O4磁性材料在很多领域具有应用前景,其制备过程如下:在氩气气氛下,向装有50 mL 1 mol·L-1 FeCl2溶液的三颈烧瓶(装置如图)中逐滴加入100 mL 14 mol·L-1 KOH溶液,用磁力搅拌器持续搅拌,在100 ℃下回流3 h,得到成分为Fe和Fe3O4的黑色沉淀。 (1)使用恒压滴液漏斗的优点是_____。 (2)三颈烧瓶中发生反应的离子方程式为_____ _____。 (3)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40 ℃下干燥后焙烧3 h,得到Fe/Fe3O4复合物产品3.24 g。 ①焙烧需在隔绝空气的条件下进行,原因是_____ _____。 ②判断沉淀是否已经用水洗涤干净,应选择的试剂为 ;使用乙醇洗涤的目的是_____ _____。 ③计算实验所得产品的产率:_____。 (4)已知FeO的晶胞结构如图所示,Fe原子的配位数是 ,设其中原子坐标参数A为(0,0,0),B为(1,1,0),则C的坐标参数为 。 3.(2023·茂名二模)84消毒液的有效成分为NaClO,广泛应用于物体表面和环境等的消毒。实验室利用以下装置制备NaClO并进行性质探究。 (1)装置B的作用是_____。 (2)生成NaClO的离子反应方程式为_____ _____。 (3)某小组研究25 ℃下NaClO稳定性的影响因素。 提出假设:NaClO溶液中加入Na2SiO3或改变NaCl浓度,对NaClO的稳定性有影响。 设计方案并完成实验: 用浓度为1 mol·L-1的NaClO溶液、NaCl溶液、Na2SiO3溶液和NaOH溶液按下表配制总体积相同的系列溶液;相同时间内测定溶液中有效氯(指次氯酸钠中氯元素质量占样品的百分含量),记录数据。 序 号 V(N ... ...
~~ 您好,已阅读到文档的结尾了 ~~

