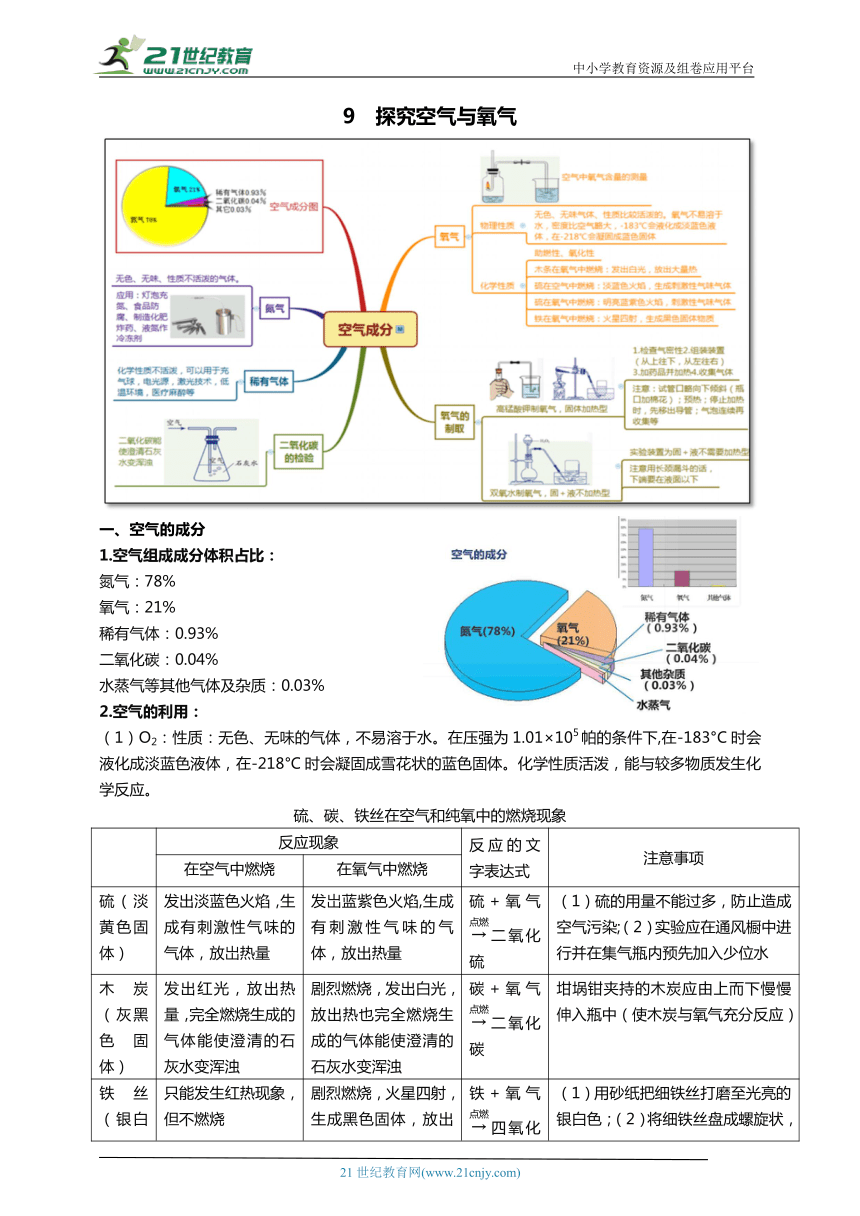
中小学教育资源及组卷应用平台 9 探究空气与氧气 空气的成分 1.空气组成成分体积占比: 氮气:78% 氧气:21% 稀有气体:0.93% 二氧化碳:0.04% 水蒸气等其他气体及杂质:0.03% 2.空气的利用: (1)O2:性质:无色、无味的气体,不易溶于水。在压强为1.01×105帕的条件下,在-183°C时会液化成淡蓝色液体,在-218°C时会凝固成雪花状的蓝色固体。化学性质活泼,能与较多物质发生化学反应。 硫、碳、铁丝在空气和纯氧中的燃烧现象 反应现象 反应的文字表达式 注意事项 在空气中燃烧 在氧气中燃烧 硫(淡黄色固体) 发出淡蓝色火焰,生成有刺激性气味的气体,放岀热量 发岀蓝紫色火焰,生成有刺激性气味的气体,放出热量 硫+氧气二氧化硫 (1)硫的用量不能过多,防止造成空气污染;(2)实验应在通风橱中进行并在集气瓶内预先加入少位水 木炭(灰黑色固体) 发出红光,放出热量,完全燃烧生成的气体能使澄清的石灰水变浑浊 剧烈燃烧,发出白光,放出热也完全燃烧生成的气体能使澄清的石灰水变浑浊 碳+氧气二氧化碳 坩埚钳夹持的木炭应由上而下慢慢伸入瓶中(使木炭与氧气充分反应) 铁丝(银白色固体) 只能发生红热现象,但不燃烧 剧烈燃烧,火星四射,生成黑色固体,放出大量的热 铁+氧气四氧化三铁 (1)用砂纸把细铁丝打磨至光亮的银白色;(2)将细铁丝盘成螺旋状,并在下端系一根火柴;(3)待火柴快燃尽时,再将铁丝伸人集气瓶中;(4)集气瓶中要预先加入少量水或铺一层细沙 用途:供给呼吸;支持燃烧,也叫助燃,常用于焊接、切割金属等方面。 (2)N2:性质:无色、无味的气体,难溶于水;不支持燃烧。化学性质较稳定。 用途:灯泡中充氮气可延长使用寿命;食品包装充入氮气可防腐;制造化肥、炸药的重要原料;液氮可以做冷冻剂,医疗上用液氮冷冻麻醉或冷藏人体细胞组织等。 (3)稀有气体:又叫惰性气体,是氦、氖、氩、氪、氙和氡等气体的总称,是混合物。 性质:无色、无味的气体,难溶于水,化学性质很稳定。 用途:常用作保护气;做光源(稀有气体通电能发出不同颜色的光)。 CO:性质:无色无味气体,比空气重。 用途:二氧化碳可用于灭火;固态二氧化碳(又称干冰)是一种致冷剂, 可用来保藏食品,也可用于人工降雨.二氧化碳是植物光合作 用的原料,是一种气体肥料二氧化碳是一种化工原料,可用于制纯碱、尿素和汽水。 3.空气中氧气成分的测定 (1)实验方案设计: 在相同气压下,看消耗掉氧气后,剩余气体的体积占原空气的体积数。用红磷燃烧,生成P2O5固体颗粒且可溶于水。 (2)装置图 (3)实验现象: a、红磷燃烧发出黄白色火焰,放出热量,有大量白烟产生。 b、待集气瓶冷却后,打开止水夹,水经导管进入集气瓶,约占集气瓶内空气总体积的1/5。 (4)实验结论:空气中氧气的体积约占空气总体积的1/5。 (5)化学方程式: 4P + 5O2 2P2O5 (6)注意事项: a.装置的气密性要好,(否则测量结果偏小); b.所用的红磷必须过量,过少则氧气没有全部消耗完,(会导致测量结果偏小); c.要等集气瓶(装置)冷却后才能打开弹簧夹,(否则测量结果偏小); d.在实验前,导管应预先注满水,(否则测量结果偏小); e.要先夹住橡皮管,然后再点红磷(否则测量结果偏大); f.点燃红磷伸入瓶中要立即塞紧瓶塞(否则测量结果偏大) (7)实验原理:红磷和氧气发生反应,生成物为P2O5为固体,溶于水后,使瓶内气体压强减小,打开止水夹后,大气压把水压入集气瓶中,直至内外压强相等。 (8)实验装置的改进方案图: 二、氧气的制取 1.实验室里制取氧气的方法有:分解 H2O2 和加热分解 KMnO4 或 KClO3,化学方程式为: (1)2H2O2 MnO2 2H2O + O2 ↑ (2)2KMnO4 K2MnO4 + MnO2 + O2↑ (3)2KClO3 MnO2 2KCl + 3O2↑ ... ...
~~ 您好,已阅读到文档的结尾了 ~~