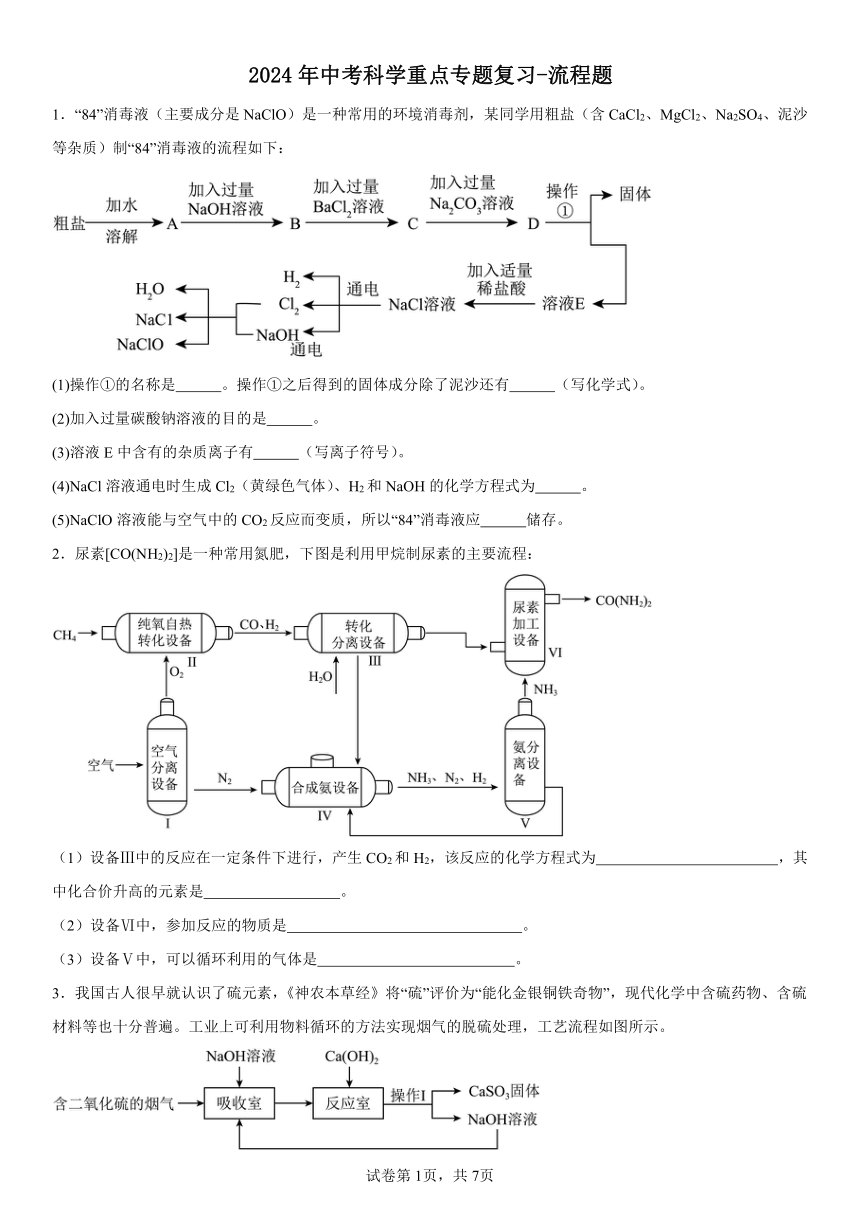
2024年中考科学重点专题复习-流程题 1.“84”消毒液(主要成分是NaClO)是一种常用的环境消毒剂,某同学用粗盐(含CaCl2、MgCl2、Na2SO4、泥沙等杂质)制“84”消毒液的流程如下: (1)操作①的名称是 。操作①之后得到的固体成分除了泥沙还有 (写化学式)。 (2)加入过量碳酸钠溶液的目的是 。 (3)溶液E中含有的杂质离子有 (写离子符号)。 (4)NaCl溶液通电时生成Cl2(黄绿色气体)、H2和NaOH的化学方程式为 。 (5)NaClO溶液能与空气中的CO2反应而变质,所以“84”消毒液应 储存。 2.尿素[CO(NH2)2]是一种常用氮肥,下图是利用甲烷制尿素的主要流程: (1)设备Ⅲ中的反应在一定条件下进行,产生CO2和H2,该反应的化学方程式为 ,其中化合价升高的元素是 。 (2)设备Ⅵ中,参加反应的物质是 。 (3)设备Ⅴ中,可以循环利用的气体是 。 3.我国古人很早就认识了硫元素,《神农本草经》将“硫”评价为“能化金银铜铁奇物”,现代化学中含硫药物、含硫材料等也十分普遍。工业上可利用物料循环的方法实现烟气的脱硫处理,工艺流程如图所示。 (1)操作Ⅰ的名称是 ; (2)吸收室中发生的反应之一是氢氧化钠和二氧化硫的反应,类比氢氧化钠和二氧化碳的反应,写出氢氧化钠和二氧化硫反应的化学方程式 ; (3)理论上只需不断加入 (填化学式) 便可持续实现烟气的脱硫处理。 4.铝在地壳中主要以铝土矿的形式存在,铝土矿的主要成分为 Al2O3(含少量 Fe2O3、SiO2等杂质)。工业上冶炼铝的工艺流程见图: (1)操作①加入足量盐酸后,得到的滤液中一定含有的金属阳离子有 (填符号)。 (2)操作⑧得到的 Al(OH)3受热分解生成两种氧化物,该反应的化学方程式为 。 (3)在冰晶石作助熔剂条件下,电解Al2O3得到金属铝,该反应的化学方程式为 。 (4)假设铝土矿中的铝元素全部转化成单质铝,现用质量分数为80%的铝土矿,经冶炼得到铝540t,则需要铝土矿的质量为 。 5.为了实现碳减排目标,许多国家都在研究二氧化碳的减排措施,其中“碳捕捉和封存”技术是实现这一目标的重要途径之一。工业流程如图所示: 请回答以下有关问题: (1)“捕捉室”中发生反应的化学方程式为 。 (2)进入“反应分离器”中物质A是 (填化学式)。 (3)整个过程中,发生化学反应的基本类型有 种。 6.粗盐中除NaCl外还含有MgSO4以及泥沙等杂质。提纯粗盐的实验流程如下: (1)用托盘天平称量3.6 g粗盐时,发现天平指针偏向左盘,此时应 (填序号)。 A.向左盘添加粗盐 B.减少左盘粗盐 C.向左移动游码 D.向右移动游码 (2)操作①、②依次为下图1中的 , (填标号)。 (3)玻璃棒在溶解时所起的作用是 。 (4)本实验从滤液得到精盐,采用的是蒸发溶剂而不是降温的方法,结合图2说明其原因是 。 (5)在温度约为 ℃时(取整数),MgSO4饱和溶液的溶质质量分数最大,此时结晶出的NaCl纯度较高。 7.合成氨是人类科学技术上得一项重大突破,对社会发展与进步做出了巨大贡献,合成氨的工艺流程图如下: (1)合成氨需要的氮气来自空气,空气中氮气的体积分数约为 。 (2)焦炭和水蒸气在高温条件下反应生成两种可燃性气体,该反应的化学方程式为 。 (3)原料中N2、H2中常含有CO2和水蒸气,反应前要净化,净化的过程是 。 (4)写出N2、H2反应生成NH3的化学方程式 。 8.真空热还原法生产钙的主要转化过程如下(部分产物略去)。 (1)氧化钙的化学式 。 (2)反应Ⅱ只生成两种产物钙蒸气和固体X,从元素守恒角度说明固体X含有 (填元素符号)元素。 (3)工业上,煅烧石灰石,如果要制取2.8t氧化钙,需要碳酸钙的质量是 t。 9.实验室有一瓶无色溶液 A,已知其中的溶质可能是 NaOH 和 Ba(NO3)2或两者之一,另有一固体混合物 B,其中可能含有 NH4Cl、MgSO4、(NH4)2SO4、Fe(NO3)3四种物质 ... ...
~~ 您好,已阅读到文档的结尾了 ~~