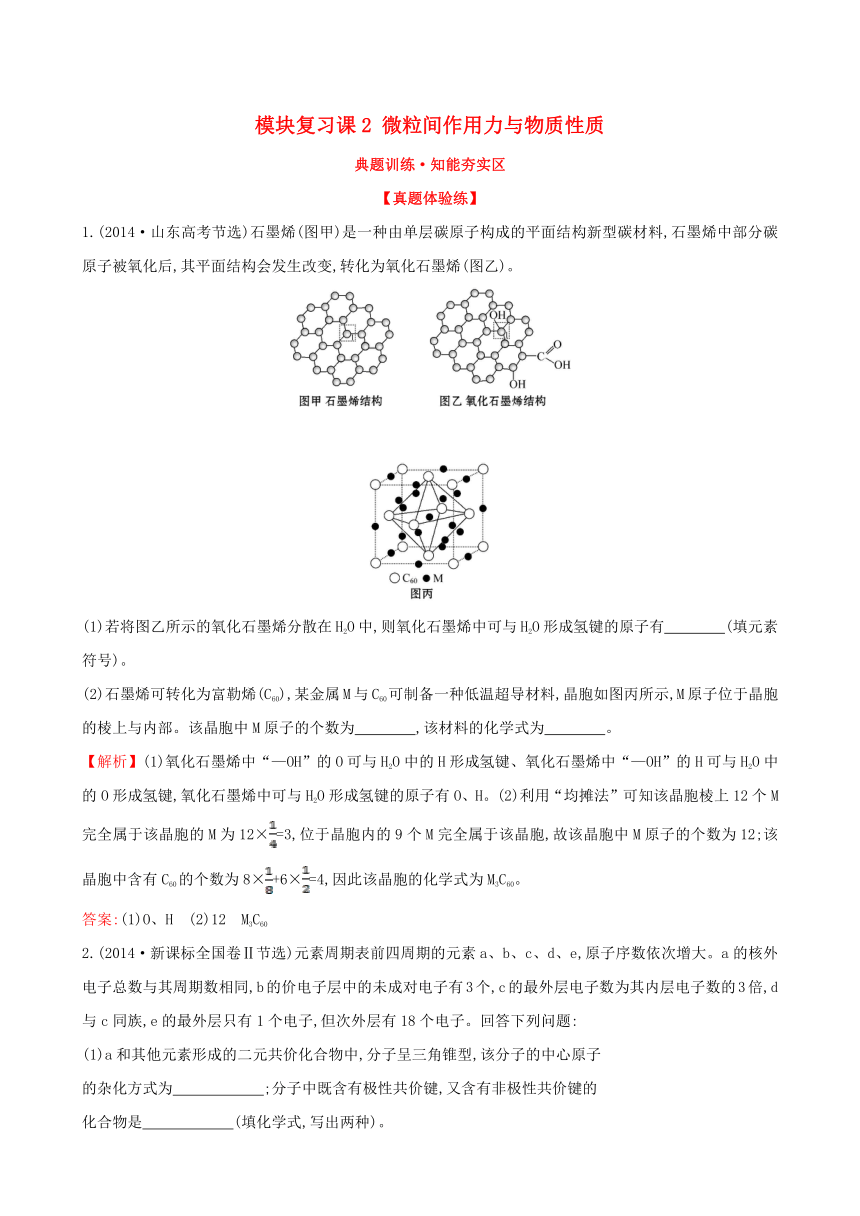
模块复习课2 微粒间作用力与物质性质 典题训练·知能夯实区 【真题体验练】 1.(2014·山东高考节选)石墨烯(图 出卷网甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(图乙)。 出卷网 出卷网 (1)若将图乙所示的氧化石墨烯分散在H2O中,则氧化石墨烯中可与H2O形成氢键的原子有 (填元素符号)。 (2)石墨烯可转化为富勒烯(C60),某金 出卷网属M与C60可制备一种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部。该晶胞中M原子的个数为 ,该材料的化学式为 。 【解析】(1)氧化石墨烯中“—OH”的O可与H2O中的H形成氢键、氧化石墨烯中“—OH”的H可与H2O中的O形成氢键,氧化石墨烯中可与H2O形成氢键的原子有O、H。(2)利用“均摊法”可知该晶胞棱上12个M完全属于该晶胞的M为12×=3,位于晶胞内的9个M完全属于该晶胞,故该晶胞中M原子的个数为12;该晶胞中含有C60的个数为8×+6×=4,因此该晶胞的化学式为M3C60。 答案:(1)O、H (2)12 M3C60 2.(2014·新课标全国卷Ⅱ节选)元素周 出卷网期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族,e的最外层只有1个电子,但次外层有18个电子。回答下列问题: (1)a和其他元素形成的二元共价化合物中,分子呈三角锥型,该分子的中心原子 的杂化方式为 ;分子中既含有极性共价键,又含有非极性共价键的 化合物是 (填化学式,写出两种)。 (2)e和c形成的一种离子化合物的晶体结构如图1,则e离子的电荷 为 。 (3)这5种元素形成的一种1∶1型离子化合物中,阴离子呈四面体结构;阳离子 呈轴向狭长的八面体结构(如图2所示)。 出卷网 该化合物中,阴离子为 ,阳离子中存在的化学键类型 有 ;该化合物加热时首先失去的组分是 , 判断理由是 。 【解析】a的核外电子总数与 出卷网其周期数相同,则a为氢;b的价电子层中的未成对电子有3个,则b为氮;c的最外层电子数为其内层电子数的3倍,则c为氧;d与c同主族,d为硫;e的最外层只有1个电子,但次外层有18个电子,其电子排布式应为1s22s22p63s23p63d104s1,为铜元素。 (1)根据题意应该是形成氨气,氨气中氮原子为sp3杂化,分子中既有非极性键又有极性键的二元化合物有H2O2、N2H4、C2H6等; (2)晶胞中氧离子个数为1+8×=2;铜离子的个数为4,因此该晶体为氧化亚铜,其中铜离子为+1价; (3)这5种元素形成的一种1∶1型离子 出卷网化合物中,阴离子呈四面体结构,则阴离子为硫酸根,根据阳离子的结构图可以知道该阳离子中含有一个铜离子,四个氨分子,两个水分子,因此该物质的化学式为[Cu(NH3)4(H2O)2]SO4,阳离子中存在配位键和共价键,该化合物加热时首先失去水,原因是铜离子与水所形成的配位键要比与氨气所形成的配位键弱。 答案:(1)sp3 H2O2、N2H4(合理即可) (2)+1 (3)S 共价键和配位键 H2O H2O与Cu2+的配位键比NH3与Cu2+的弱 3.(2014·新课标全国卷Ⅰ节选)早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成。回答下列问题: (1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过 方法区分晶体、准晶体和非晶体。 (2)Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。 (3)铝单质为面心立方晶体,其晶胞参数a=0.405 nm,晶胞中铝原子的配位数 为 。列式表示铝单质的密度 g·cm-3(不必计算出结果)。 【解析】(1)利用X-射线衍射法能区分晶体、准晶体和非晶体。(2)该晶胞中含 ... ...
~~ 您好,已阅读到文档的结尾了 ~~