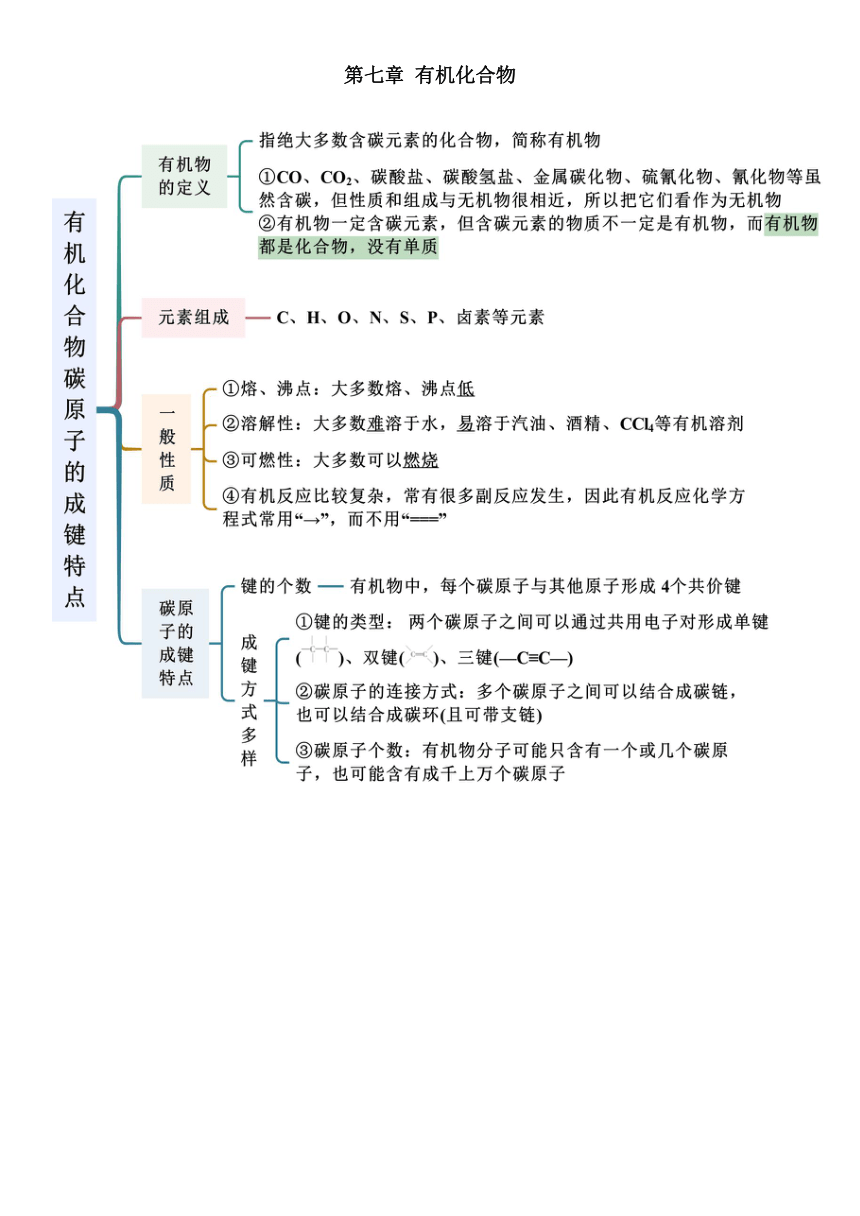
有机化合物 指绝大多数含碳元素的化合物,简称有机物 有机物 的定义 ①C0、C02、碳酸盐、碳酸氢盐、金属碳化物、硫氰化物、氰化物等虽 然含碳,但性质和组成与无机物很相近,所以把它们看作为无机物 ②有机物一定含碳元素,但含碳元素的物质不一定是有机物,而有机物 都是化合物,没有单质 有机化合物碳原子的成键特点 元素组成 一C、H、O、N、S、P、卤素等元素 ①熔、沸点:大多数熔、沸点低 ②溶解性:大多数难溶于水,易溶于汽油、酒精、CC4等有机溶剂 般 性质 ③可燃性:大多数可以燃烧 ④有机反应比较复杂,常有很多副反应发生,因此有机反应化学方 程式常用“→”,而不用=二” 键的个数一有机物中,每个碳原子与其他原子形成4个共价键 碳原 子的 ①键的类型:两个碳原子之间可以通过共用电子对形成单键 成键 ()、双键()三键(一C=C一) 特点 键方式多样 ②碳原子的连接方式:多个碳原子之间可以结合成碳链, 也可以结合成碳环(且可带支链) ③碳原子个数:有机物分子可能只含有一个或几个碳原 子,也可能含有成千上万个碳原子 有机化合物中只含有碳和氢两种元素,分子中的碳原子之间都以单 概念 键结合,碳原子的剩余价键均与氢原子结合,使碳原子的化合价都 达到“饱和”,称为饱和烃,又称烷烃 ①碳碳单键(C一 ):碳原子之间的化学键都是单键 分子 ②呈链状(直链或带支链):多个碳原子相互连接成链状,而不是封闭式环状结构 结构 特点 ③“饱和”:每个碳原子形成4个共价键,碳原子剩余价键全部跟氢原子结合 ④烷烃的空间结构中,碳原子(大于等于3时)不在一条直线上,直链 烷烃中的碳原子空间构型是折线形或锯齿状 通式 链状烷烃中的碳原子数为n,氢原子数就是2n十2,分子通式可表示为CnH2m+2 一般情况下,1~4个碳原子烷烃(烃)为气态,5~16个碳原子为液 状态一 态,16个碳原子以上为固态 溶解性一烷烃不溶于水,易溶于有机溶剂 物理性质 随着烷烃分子中碳原子数增加,相对分子质量增大,范德华力逐渐 熔沸点一增大,烷烃分子的熔、沸点逐渐升高;分子式相同的烷烃,支链越 多,熔、沸点越低,如熔、沸点:正丁烷>异丁烷 密度一 随着碳原子数的递增,密度逐渐增加;烷烃的密度都小于水的密度 ①化学性质比较稳定,常温下不与跟强酸、强碱或高锰酸钾等强氧化剂等不反应 ②氧化反应:燃完反应CH2计3n,+10:点燃nC0十a+1)H0 化学性 2 ③烷烃的取代反应:C,Hn2十X光,CH+K+K CmHm+X可与X继续发生取代反应 ④烷烃的分解反应(高温裂化或裂解)一应用于石油化工和天然气化工生产中 烷烃受热时会分解,生成含碳原子数较少的烷烃和烯烃,如:C164雀剂)CH16十CH1 加热、加国 概念 一结构相似,分子组成上相差一个或若干个CH2原子团的物质互称为同系物 同系物 ⑦ 一差: 两种物质分子组成上相差一个或多个“CH2”原子团 判断 方法 ②二同:具有相同的通式,两种物质属于同一类物质 ③二相似:两种物质结构相似,化学性质相似 ... ...
~~ 您好,已阅读到文档的结尾了 ~~