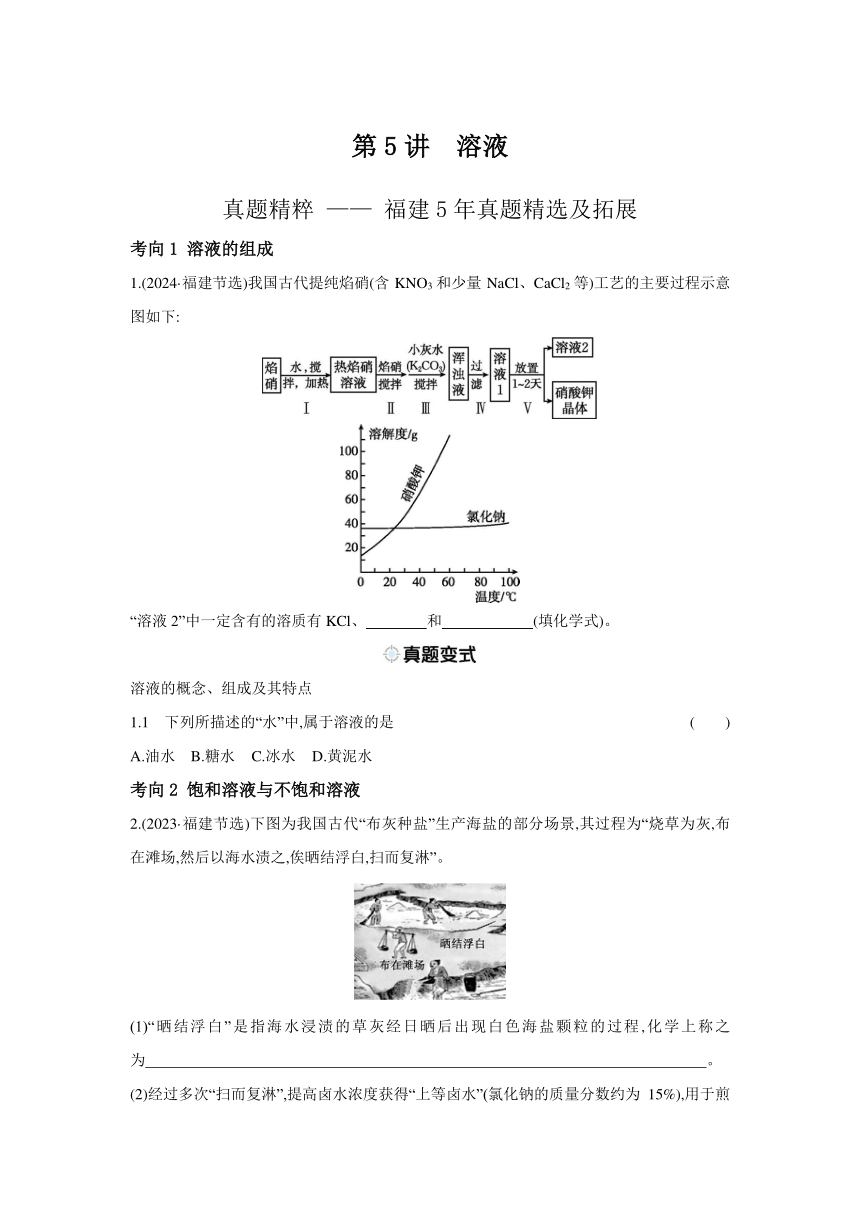
第5讲 溶液 真题精粹 ——— 福建5年真题精选及拓展 考向1 溶液的组成 1.(2024·福建节选)我国古代提纯焰硝(含KNO3和少量NaCl、CaCl2等)工艺的主要过程示意图如下: “溶液2”中一定含有的溶质有KCl、 和 (填化学式)。 溶液的概念、组成及其特点 1.1 下列所描述的“水”中,属于溶液的是 ( ) A.油水 B.糖水 C.冰水 D.黄泥水 考向2 饱和溶液与不饱和溶液 2.(2023·福建节选)下图为我国古代“布灰种盐”生产海盐的部分场景,其过程为“烧草为灰,布在滩场,然后以海水渍之,俟晒结浮白,扫而复淋”。 (1)“晒结浮白”是指海水浸渍的草灰经日晒后出现白色海盐颗粒的过程,化学上称之为 。 (2)经过多次“扫而复淋”,提高卤水浓度获得“上等卤水”(氯化钠的质量分数约为15%),用于煎炼海盐。 ①1 000 g “上等卤水”蒸干后,可得到氯化钠的质量约为 g。 ②将“上等卤水”在100 ℃恒温蒸发至刚有晶体析出,所得溶液的组成为150 g溶液中含水100 g、NaCl 39.8 g、MgCl27.65 g及其他成分2.55 g。将150 g此溶液降温至20 ℃,有 g NaCl析出(溶解度见表)。此时, (选填“有”或“没有”)MgCl2析出,原因是 。 温度/℃ 20 60 100 溶解度/g NaCl 36.0 37.3 39.8 MgCl2 54.8 61.3 73.0 3.(2024·福建节选)我国古代提纯焰硝(含KNO3和少量NaCl、CaCl2等)工艺的主要过程示意图如下: (1)上图为硝酸钾、氯化钠的溶解度曲线。步骤Ⅳ在较高温度下过滤的目的是 。 (2)步骤Ⅴ析出硝酸钾晶体的过程称之为 。 饱和溶液和不饱和溶液的相互转化 3.1 试管内盛有20 ℃的饱和硝酸钾溶液,其上漂浮一小木块如图所示。将试管插入烧杯内的冰水混合物中,一段时间后,下列有关说法不正确的是 ( ) A.试管内溶液的质量变小 B.试管内有固体析出 C.试管内溶液的溶质质量分数变大 D.小木块浸入溶液内的体积变大 考向3 溶解度与溶解度曲线 4.(2023·福建节选)为研究溶解度曲线的应用,学习小组查得资料:某钢铁厂处理高盐废水(含氯化钠、硫酸钠及微量的其他盐)的流程、相关物质的溶解度曲线如图所示。请和小组同学一起研究。 (1)当温度高于 ℃时,硫酸钠的溶解度随温度升高而降低。 (2)40 ℃时,将50 g硫酸钠固体加入100 g水中,充分搅拌后所得溶液的溶质质量分数为 (列出计算式即可)。 (3)降温至0 ℃的“冷冻结晶”过程,析出的两种物质中较多的是 。 (4)结合溶解度曲线解释,“蒸发结晶2”主要得到氯化钠的原因是 。 5.(2022·福建)NaCl和KNO3在不同温度时的溶解度如下表。下列说法错误的是 ( ) 温度/℃ 0 20 40 60 NaCl的溶解度/g 35.7 36.0 36.6 37.3 KNO3的溶解度/g 13.3 31.6 63.9 110 A.20 ℃时,100 g水中最多能溶解36.0 g NaCl B.40 ℃ 时,KNO3饱和溶液的溶质质量分数小于63.9% C.可用冷却海水的方法获取大量食盐 D.其他条件不变,升温可将KNO3饱和溶液变为不饱和溶液 固体溶解度曲线及其作用 5.1 水和溶液在生产、生活中有着重要的作用。图1所示是a、b两物质在水中的溶解度曲线,请回答下列问题: (1)曲线上P点的含义是 。 (2)将b物质的饱和溶液转化为不饱和溶液的一种方法是 。 (3)试管1、2中分别盛有20 ℃时等质量的a、b饱和溶液,底部有等质量的a、b固体剩余,向烧杯内的水中加入硝酸铵固体如图2所示,下列判断不正确的是 (填字母,不考虑溶剂的蒸发,析出的固体不含水)。 A.试管2底部的固体减少 B.a溶液由饱和溶液变成不饱和溶液 C.a溶液中溶剂质量等于b溶液中溶剂质量 D.变化后,b溶液中的溶质质量分数仍然等于a溶液中的溶质质量分数 考向2 粗盐 ... ...
~~ 您好,已阅读到文档的结尾了 ~~