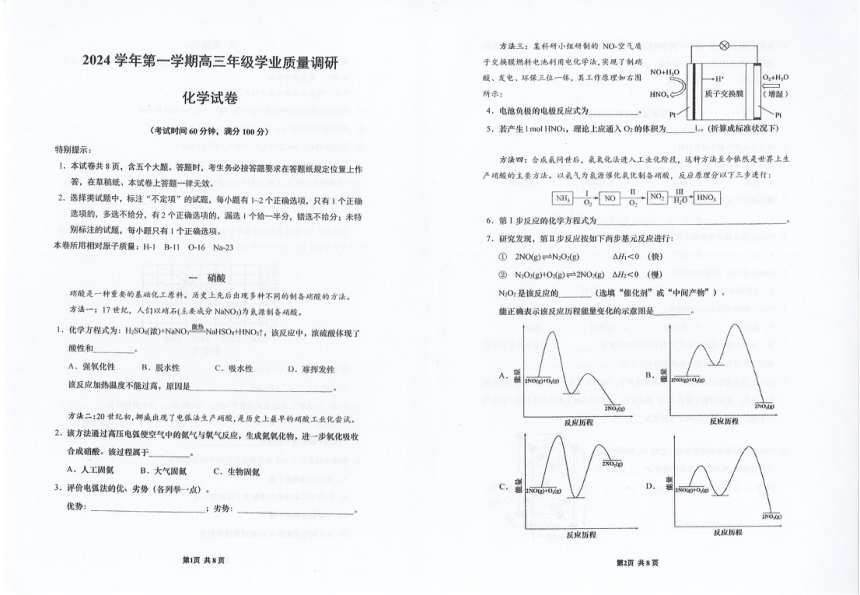
方法三:某科研小组研制的N○-空气质 2024学年第一学期高三年级学业质量调研 子交换膜燃料电池利用电化学法,实现了制硝 NO+H2O 酸、发电、环保三位一体,其工作原理如右图 -→H O2+H20 化学试卷 所示: HNO, 质子交换膜 (增湿) 4.电池负极的电极反应式为」 Pt Pt (考试时间60分钟,满分100分) 5,若产生1 mol HNO3,理论上应通入O2的体积为 L。(折算成标准状况下) 特别提示: 方法四:合成氨问世后,氨氧化法进入工业化阶段,这种方法至今依然是世界上生 1.本试卷共8页,含五个大题。答题时,考生务必按答题要求在答题纸规定位置上作 答,在草稿纸、本试卷上答题一律无效。 产硝酸的主要方法。以氨气为氮源催化氧化制备硝酸,反应原理分以下三步进行: 2.选择类试题中,标注“不定项”的试题,每小题有12个正确选项,只有1个正确 间&o&Omo 选项的,多选不给分,有2个正确选项的,漏选1个给一半分,错选不给分;未特 6.第I步反应的化学方程式为 别标注的试题,每小题只有1个正确选项。 7.研究发现,第Ⅱ步反应按如下两步基元反应进行: 本卷所用相对原子质量:H-1B-11O-16Na23 ①2NO(g)=N2O2(g) △H1<0(快) 一硝酸 ②N202(g)02(g)=2NO2(g)△h<0(慢) 硝酸是一种重要的基础化工原料。历史上先后出现多种不同的制备硝酸的方法。 N2O2是该反应的 (选填“催化剂”或“中间产物”)。 方法一:17世纪,人们以硝石(主要成分NaNO)为氣源制备硝酸。 能正确表示该反应历程能量变化的示意图是 1.化学方程式为:HSO(浓)+NaNO,热NaHSOr+HNO,该反应中,浓硫酸体现了 酸性和 A.强氧化性 B.脱水性 C.吸水性 D.难挥发性 该反应加热温度不能过高,原因是 A.2Not,e B. 盟2NOg+O4(g) ZNO:(g) 方法二:20世纪初,挪威出现了电孤法生产硝酸,是历史上最早的硝酸工业化尝试。 反应历程 反应历程 2.该方法通过高压电弧使空气中的氮氨气与氧气反应,生成氮氧化物,进一步氧化吸收 合成硝酸。该过程属于 2N0,g A.人工固氮 B.大气固氮 C.生物固氮 3.评价电弧法的优、劣势(各列举一点)。 D. 2NO(g)+O,(g) 优势: ;劣势 2N0(g 反成历程 反应历程 第1页共8页 第2页共8页
~~ 您好,已阅读到文档的结尾了 ~~