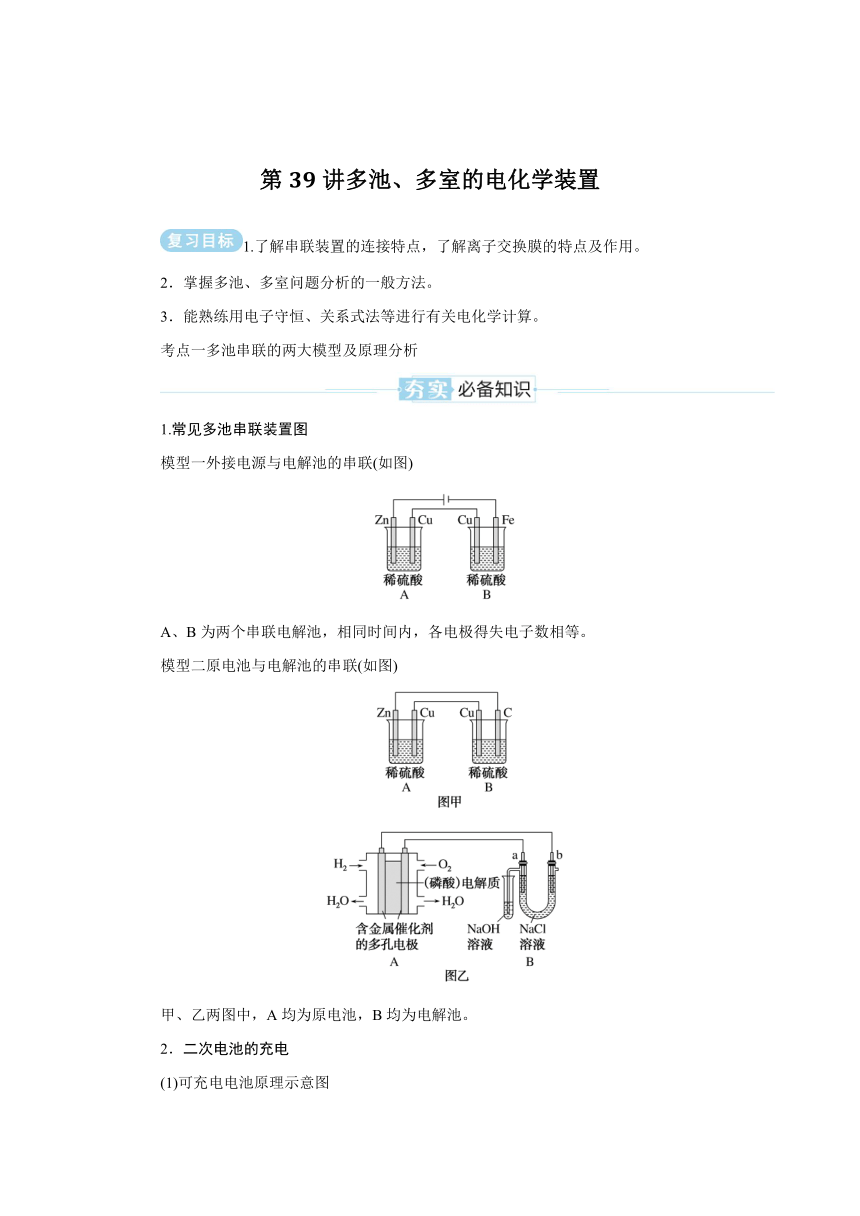
第39讲多池、多室的电化学装置 1.了解串联装置的连接特点,了解离子交换膜的特点及作用。 2.掌握多池、多室问题分析的一般方法。 3.能熟练用电子守恒、关系式法等进行有关电化学计算。 考点一多池串联的两大模型及原理分析 1.常见多池串联装置图 模型一外接电源与电解池的串联(如图) A、B为两个串联电解池,相同时间内,各电极得失电子数相等。 模型二原电池与电解池的串联(如图) 甲、乙两图中,A均为原电池,B均为电解池。 2.二次电池的充电 (1)可充电电池原理示意图 充电时,原电池负极与外接电源负极相连,原电池正极与外接电源正极相连,记作“正接正,负接负”。 (2)可充电电池有充电和放电两个过程,放电时是原电池反应,充电时是电解池反应。充电、放电不是可逆反应。 (3)放电时的负极反应和充电时的阴极反应相反,放电时的正极反应和充电时的阳极反应相反。将负(正)极反应式变换方向并将电子移项即可得出阴(阳)极反应式。 3.电化学计算的三种方法 如以电路中通过4mole-为桥梁可构建以下关系式: (式中M为金属,n为其离子的化合价数值) 该关系式具有总览电化学计算的作用和价值,熟记电极反应式,灵活运用关系式便能快速解答常见的电化学计算问题。 感悟: 【教考衔接】 典例[2022·山东卷,13]设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成CO2,将废旧锂离子电池的正极材料LiCoO2(s)转化为Co2+,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是() a.装置工作时,甲室溶液pH逐渐增大 b.装置工作一段时间后,乙室应补充盐酸 c.乙室电极反应式为 LiCoO2+2H2O+e-===Li++Co2++4OH- d.若甲室Co2+减少200mg,乙室Co2+增加300mg,则此时已进行过溶液转移 【解题关键】右侧装置为原电池,带细菌电极为负极,LiCoO2电极为正极;左侧装置为电解池,带细菌电极为阳极,CoCl2电极为阴极;两个电池为串联连接。 听课笔记 【对点演练】 1.如图所示,甲池的总反应式为N2H4+O2===N2+2H2O,下列关于该装置工作时的说法正确的是() A.该装置工作时,Ag电极上有气体生成 B.甲池中负极反应式为N2H4-4e-===N2+4H+ C.甲池和乙池中溶液的pH均减小 D.当甲池中消耗3.2gN2H4时,乙池中理论上最多产生6.4g固体 2.铅酸蓄电池是典型的可充电电池,正、负极是惰性材料,电池总反应式为Pb+PbO2+2H2SO4放电,充电2PbSO4+2H2O,回答下列问题(不考虑氢、氧的氧化还原): (1)放电时,正极的电极反应式是_。电解液中H2SO4的浓度将变_;当外电路通过1mol电子时,理论上负极板的质量增加_g。 (2)在完全放电耗尽PbO2和Pb时,若按如图连接,电解一段时间后,则在A电极上生成_,B电极上生成_,此时铅酸蓄电池的正、负极的极性将_(填“不变”或“对换”)。 3.在如图所示的装置中,若通直流电5min时,铜电极的质量增加2.16g。试回答下列问题。 (1)电源中X为直流电源的_极。 (2)pH变化:A_(填“增大”“减小”或“不变”,下同),B_,C_。 (3)通电5min时,B中共收集224mL(标准状况下)气体,溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为_(设电解前后溶液体积无变化)。 (4)常温下,若A中KCl足量且溶液的体积也是200mL,电解后,溶液的pH为_(设电解前后溶液体积无变化)。 考点二多室电化学装置 为实现特定功能需求,在电化学装置中增加离子交换膜,将原电池或电解池分隔成两个或多个相对独立的室。 1.离子交换膜的分类和应用 2.分析某室质量变化的关键 分析某室质量的变化,既要考虑该区(或该电极)的化学反应,又要考虑通过“交换膜”的离子带来的质量变化。 【教考衔接】 典例1[2022·湖南卷,8]海水电池在海洋能源领域备受关 ... ...
~~ 您好,已阅读到文档的结尾了 ~~