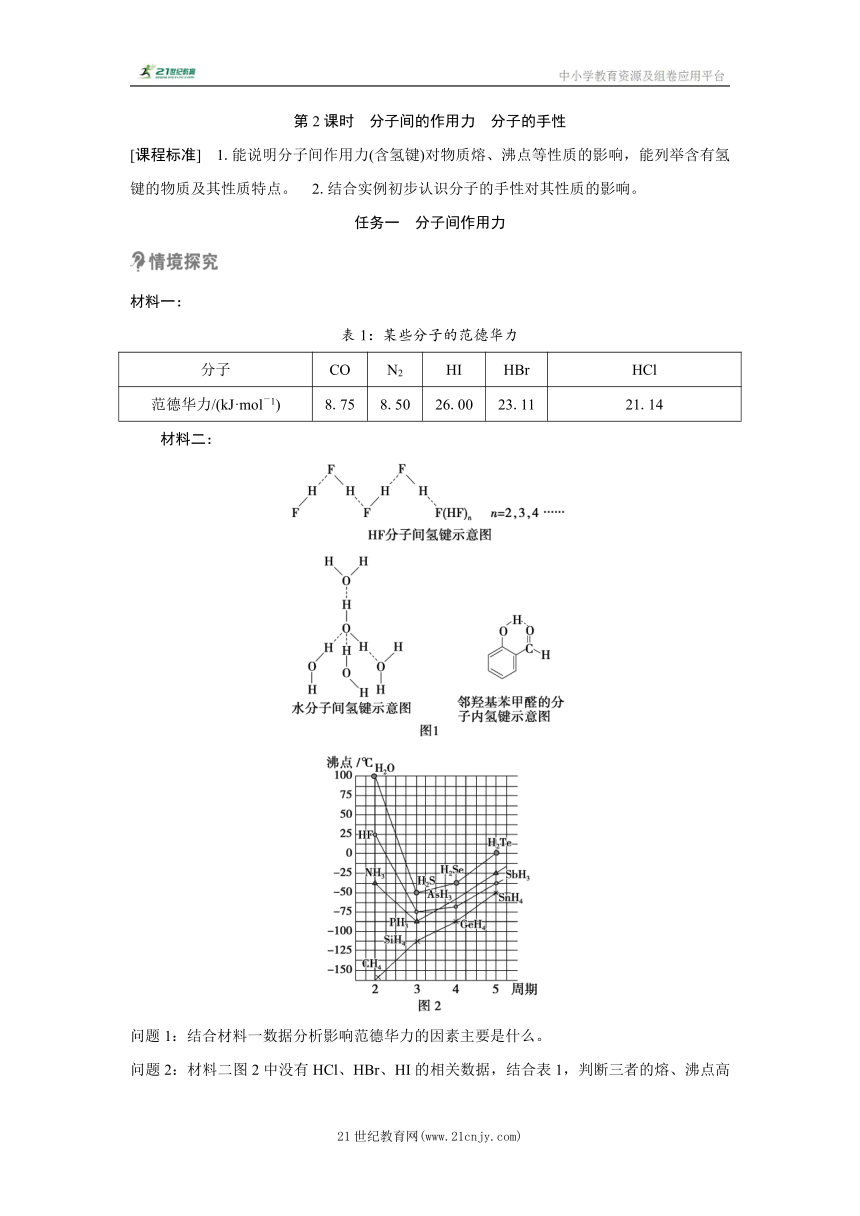
第2课时 分子间的作用力 分子的手性 [课程标准] 1.能说明分子间作用力(含氢键)对物质熔、沸点等性质的影响,能列举含有氢键的物质及其性质特点。 2.结合实例初步认识分子的手性对其性质的影响。 任务一 分子间作用力 材料一: 表1:某些分子的范德华力 分子 CO N2 HI HBr HCl 范德华力/(kJ·mol-1) 8.75 8.50 26.00 23.11 21.14 材料二: 问题1:结合材料一数据分析影响范德华力的因素主要是什么。 问题2:材料二图2中没有HCl、HBr、HI的相关数据,结合表1,判断三者的熔、沸点高低顺序及稳定性顺序。 问题3:观察材料二图1,氢键形成时有何特征? 问题4:观察材料二图2,如何解释各族元素的氢化物沸点变化?据此你对范德华力和氢键有何新的认识? 问题5:结合以上分析,解释以下问题。 (1)不断地升高温度,水可实现“冰(雪花)→水→水蒸气→氧气和氢气”的变化。各阶段被破坏的粒子间的主要相互作用依次有哪些? (2)甲醚与乙醇互为同分异构体,而乙醇与水可以任意比互溶,而甲醚溶解度较小,主要原因是什么? (3)为什么氨气极易溶于水? 提示:问题1:组成相似的分子,相对分子质量越大,范德华力越大。相对分子质量相当的分子极性越大,其范德华力越大。 问题2:熔、沸点按照HCl、HBr、HI依次升高;稳定性按照HCl、HBr、HI依次降低。 问题3:有方向性和饱和性。 问题4:CH4、SiH4、GeH4、SnH4组成和结构相似,相对分子质量越大,范德华力越大,沸点逐渐升高;NH3、H2O、HF的沸点反常的原因由于它们各自的分子间形成了氢键,增大了分子间作用力,熔、沸点升高。由此说明,氢键比化学键弱但比范德华力强。 问题5:(1)范德华力和氢键;范德华力和氢键;极性键。 (2)甲醚为非极性分子,乙醇为极性分子;乙醇与H2O之间形成分子间氢键。 (3)NH3和H2O均是极性分子,极性分子易溶于极性分子形成的溶剂中;NH3与H2O之间形成分子间氢键;NH3与H2O发生反应。 一、范德华力及其对物质性质的影响 1.含义 范德华力是分子之间普遍存在的相互作用力,它使得许多物质能以一定的凝聚态(固态和液态)存在。 2.特征 (1)范德华力很弱,约比化学键的键能小1~2个数量级。 (2)无方向性和饱和性。 3.影响因素 (1)分子的极性越大,范德华力越大。 (2)结构和组成相似的物质,相对分子质量越大,范德华力越大。 4.对物质性质的影响 范德华力主要影响物质的物理性质,如熔点、沸点;化学键主要影响物质的化学性质。范德华力越大,物质熔、沸点越高。 二、氢键及其对物质性质的影响 1.氢键的概念 氢键是一种分子间作用力。它是由已经与电负性很强的原子(如N、F、O)形成共价键的氢原子与另一个分子中或同一分子中电负性很强的原子之间的作用力。 2.氢键的表示形式 (1)通常用X—H…Y表示氢键,其中X—H表示氢原子和X原子以共价键相结合。 (2)氢键的键长是指X和Y间的距离,键能是指X—H…Y分解为 X—H和Y所需要的能量。 3.氢键形成的条件 (1)氢原子位于X原子和Y原子之间。 (2)X、Y原子所属元素具有很强的电负性和很小的原子半径。一般是氮原子、氧原子和氟原子。 4.氢键的特征 (1)氢键不属于化学键,键能较小,比化学键的键能小1~2个数量级,但比范德华力强。 (2)氢键具有一定的方向性和饱和性。 5.类型 氢键分为分子间氢键和分子内氢键。 6.氢键对物质性质的影响 (1)对物质熔点、沸点的影响: ①某些氢化物分子间存在氢键,物质的熔、沸点将升高。 如H2O、NH3、HF等,会使同族氢化物沸点反常,如H2O>H2Te>H2Se>H2S。 ②当形成分子内氢键时,物质的熔、沸点将下降。 如熔点、沸点:>。 (2)对物质溶解度的影响:溶剂和溶质之间存在氢键,溶解性好,溶质分子不能与水分子形成氢键,在水中溶解度就相对小,如NH3极易溶于水,甲醇、乙醇 ... ...
~~ 您好,已阅读到文档的结尾了 ~~