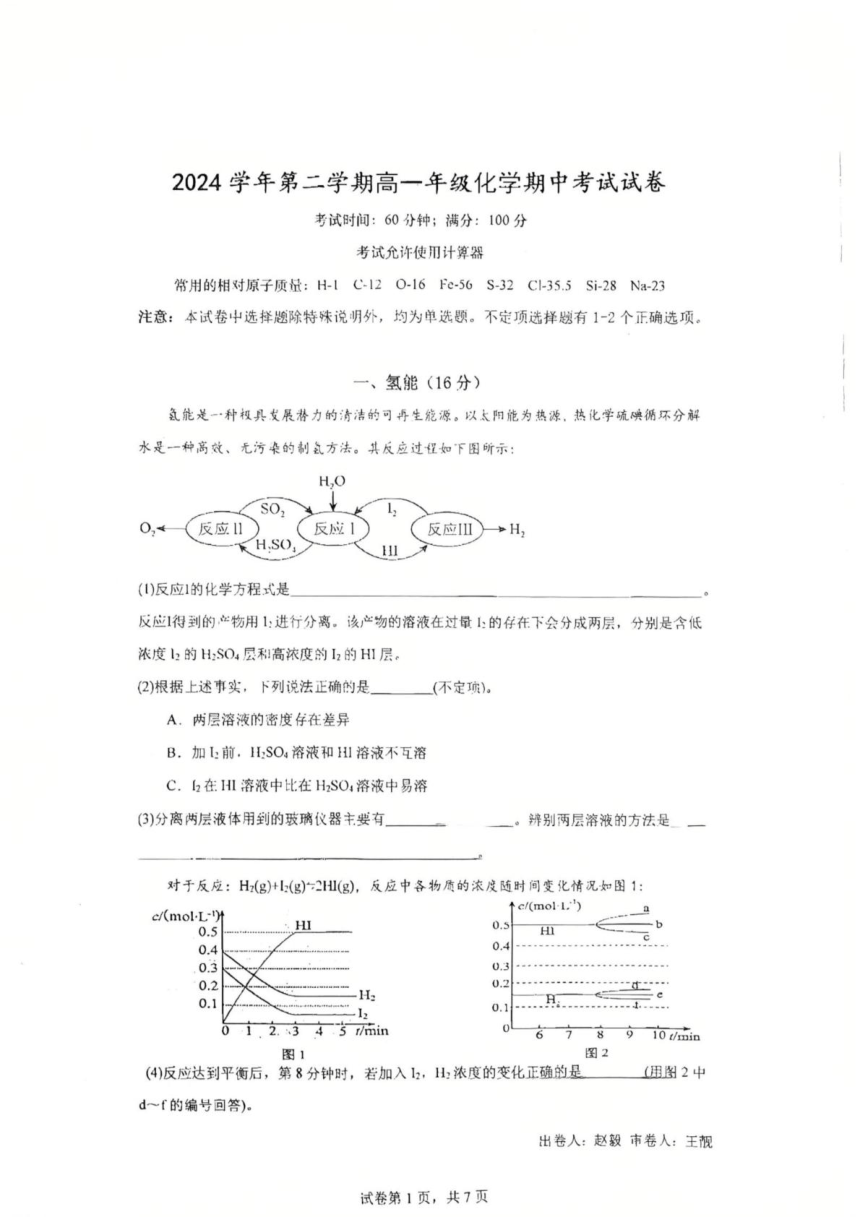
2024学年第二学期高一年级化学期中考试试卷 考试时间:60分钟;满分:100分 考试允许使用计算器 常用的相对原子质量:H-lC120-16Fc-56S-32C1-35.5Si-28Na-23 注意:本试卷中选择题除特味说明外,均为单选题。不定项选择题有1-2个正确选项。 一、氢能(16分) 急能是-·种视具发展潜力的清洁的可再生能源。以太阳能为热源、热化学硫碘循环分解 水是一种高效、无污朵的制盆方法。其反应过程如下图所示: H,O SO 02 反应1 反成 反应l +H3 H.SO 山 ()反应1的化学方程式是 反应1得到的亡物用1:进行分离。该产物的溶液在过量上:的存在下会分成两层,分别是含低 浓度l2的HSO4层利和高浓度的12的HI层。 (2)根据上述事实,下列说法正确的是 (不定项)。 A.两层溶液的密度存在差异 B.加【前.1【SO,溶液和H1溶液不互溶 C.2在IHl溶液中比在HSO:溶液中易溶 (③)分离两层液体用到的玻璃仪器主要有 辨别两层溶液的方法是一 对于反应:H(g)+l(g)片2H山(g),反应中各物质的浓度随时间变化情况如图1: ↑c/(moll') e/(molL)t 0.5 HI 0.5 HI -b 0.4 0.4 0.3 03 0.2 0.2 H: -e 0.1 0. 01,2.345in 右78910猫i加 图1 图2 (4)反应达到平衡后,第8分钟时,若加入12,H浓度的变化正确的是 (用图2中 d~f的编号回答) 出卷人:赵毅市卷人:王视 试卷第1页,共7页 (5)反应达到平衡后,第8分钟时,若反应容器的容积扩大一倍,请在图3中画出8分钟后 H浓度的变化情况。 ↑c(moll, 0.5 HI 0.4 0.3 0.2 0.1 0 6 78910in 3 〔⑥LiBH:是储氢材料,其释旅氢气的原理2LiBH=2LiH+2B+31l↑。氢化锂(LiH)是离子化 合物,写出其电子式: 若该反应中释放67.2LH:(标况下),则转 移的电子数为 个 二、氯气(22分) 氣气可直接用于自来水的消毒,也可以制取漂粉精、高铁酸钠等物质来对自来水消毒。 已知:硫酸铁与明矾都能作为絮凝剂。 ()氯气通水中可用来杀菌消毒,其有效成分的电子式是 (2)氯气可用来制取漂粉相,似十燥的氢氧化钙与氯气并不易发生反应,氯气只能被氧氧化 钙所吸附。为此,在工业上采用加入少许水的消石灰来进行氯化。其原因是 (3)用氯气对饮用水消海刮作用多,产生影响人体健康有机氯衍生物。可用氯气制取高铁酸 钠净水。请补全缺项,并配平上述离子方程式: Fe3++ Cl2=FeO+ H2O (4)计算NazFeO:的消海效率(以单位质量得到的电子数表示)约是氯气 倍。说明该净 水剂与氯气相比较有何优越性 (写出2点)。 (5(CNz是一种与C性质相似的气体,该分了中每个原子都达到了8电子稳定结构,写出 (CNh的结构式: (6)自来水(经消毒)中含疏量约70mgL,它只能以 (填微粒符号)形态存在。 (7)氯气与KOH溶液反应,产物为KCO、KC1和HO。该反应中氧化剂与还原剂的质量比 为 试卷第2页,共7页 ... ...
~~ 您好,已阅读到文档的结尾了 ~~