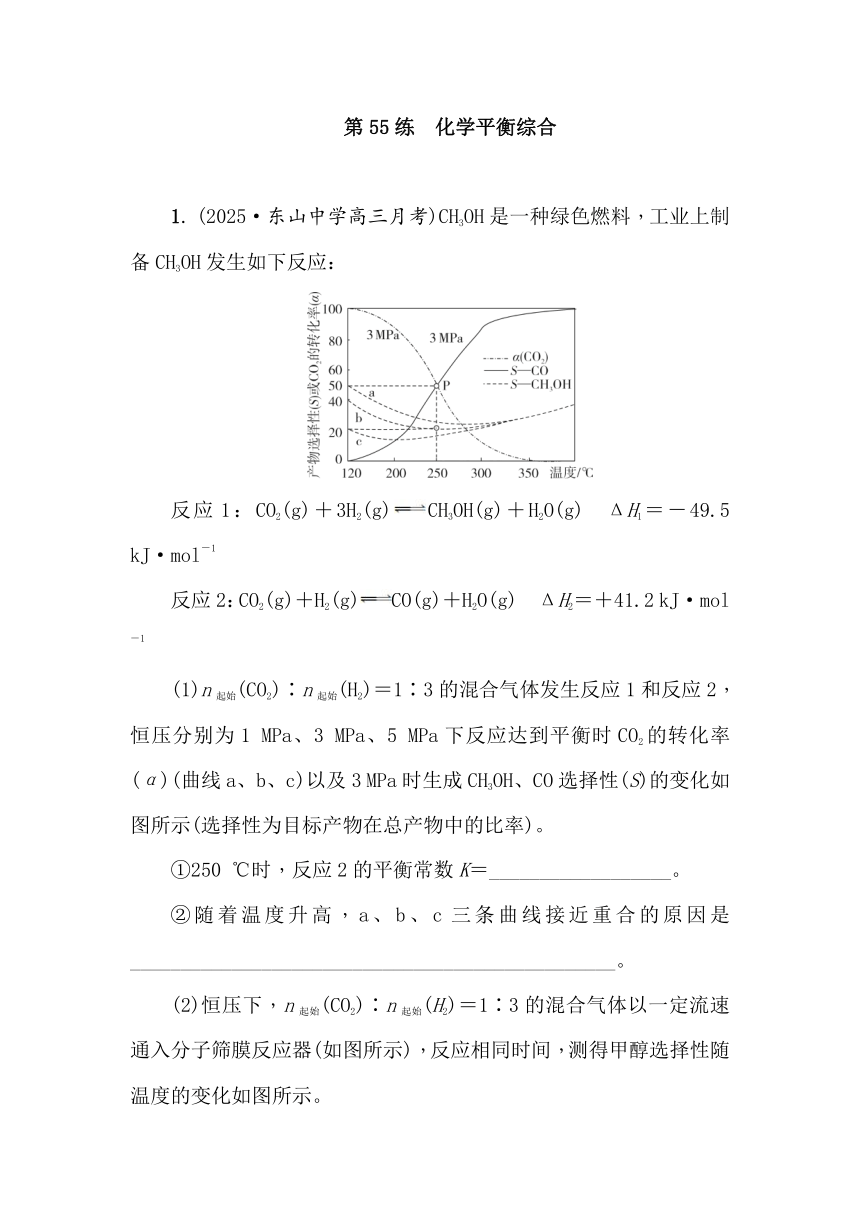
第55练 化学平衡综合 1. (2025·东山中学高三月考)CH3OH是一种绿色燃料,工业上制备CH3OH发生如下反应: 反应1:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH1=-49.5 kJ·mol-1 反应2:CO2(g)+H2(g)CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1 (1)n起始(CO2)∶n起始(H2)=1∶3的混合气体发生反应1和反应2,恒压分别为1 MPa、3 MPa、5 MPa下反应达到平衡时CO2的转化率(α)(曲线a、b、c)以及3 MPa时生成CH3OH、CO选择性(S)的变化如图所示(选择性为目标产物在总产物中的比率)。 ①250 ℃时,反应2的平衡常数K=_____。 ②随着温度升高,a、b、c三条曲线接近重合的原因是_____。 (2)恒压下,n起始(CO2)∶n起始(H2)=1∶3的混合气体以一定流速通入分子筛膜反应器(如图所示),反应相同时间,测得甲醇选择性随温度的变化如图所示。 ①随温度升高,平衡时CH3OH选择性降低的原因是_____。 ②温度相同时,CH3OH选择性的实验值高于平衡值,其原因可能是_____。 ③分子筛膜反应器可提高CO2转化率的原因是_____。 2. 乙醇被广泛应用于能源、化工、食品等领域,工业上可用以下两种方法制备乙醇。 Ⅰ.2CO2(g)+6H2(g)C2H5OH(g)+3H2O(g)。一定条件下,在一密闭容器中充入4 mol CO2和14 mol H2发生该反应,如图表示不同压强下CO2的平衡转化率与温度的关系。回答下列问题。 (1)活化能Ea(正)_____Ea(逆)(填“>”或“<”)。 (2)若在恒容绝热的容器中发生该反应,下列情况下反应一定达到平衡状态的是_____(填序号)。 A. 容器内CO2和H2体积比不再改变 B. 容器内气体密度不再改变 C. 容器内温度不再发生改变 D. 断开C===O键与断开O—H键的数目之比为2∶3 Ⅱ.乙酸甲酯(CH3COOCH3)催化加氢制取乙醇。包括以下主要反应: ①CH3COOCH3(g)+2H2(g)C2H5OH(g)+CH3OH(g) ΔH1 ②CH3COOCH3(g)+H2(g)CH3CHO(g)+CH3OH(g) ΔH2=+13.6 kJ·mol-1 (3)已知CH3COOCH3、H2、C2H5OH、CH3OH的燃烧热分别为1 593.4 kJ·mol-1,285.8 kJ·mol-1,1 366.8 kJ·mol-1,725.8 kJ·mol-1,ΔH1=_____。 (4)其他条件相同,将乙酸甲酯与氢气按一定流速通过固体催化剂表面,乙酸甲酯的转化率随氢酯比[]的关系如图所示。已知固体催化剂作用下的反应速率与催化剂表面各反应物的吸附率有关。氢酯比为8附近,乙酸甲酯的转化率存在最大值的原因是_____。 (5)T ℃时在1 L密闭容器内通入1 mol CH3COOCH3和3 mol H2,初始压强为100 MPa,发生反应①和②,达到平衡时体系压强变成90 MPa且H2的分压为CH3COOCH3分压的5倍,反应①的平衡常数Kp=_____ MPa-1。 3. (2025·玄武高中高三下月考)苯乙烯是合成橡胶和塑料的重要原料,可由乙苯为原料制得。 (1)利用“乙苯脱氢反应”可制备苯乙烯。 C6H5C2H5(g)C6H5CH===CH2(g)+H2(g) ΔH=a kJ·mol-1 保持气体总压不变,原料气按以下A、B、C三种投料方式进行: A. 乙苯 B. n(乙苯)∶n(N2)=1∶10 C. n(乙苯)∶n(CO2)=1∶10 三种投料分别达到平衡时,乙苯转化为苯乙烯的转化率与温度的关系如图1所示。 ①a_____0(填“>”、“<”或“不能确定”)。 ②相同温度下,投料方式B乙苯的平衡转化率比投料方式A的高,其原因是_____。 ③相同温度下,投料方式C乙苯的平衡转化率比投料方式B的高,其可能原因是_____。 ④工业上利用“乙苯脱氢反应”生产苯乙烯时,会产生少量积碳。使用相同条件下的水蒸气代替N2,可较长时间内保持催化剂的催化活性,其原因是_____。 (2)CO2用于制备苯乙烯有助于实现“碳中和”。 ①在催化剂X作用下,CO2参与反应的机理如图2所示(α、β表示乙苯分子中C或H原子的位置;A、B为催化剂的活性位点,其中A位点带部分正 ... ...
~~ 您好,已阅读到文档的结尾了 ~~