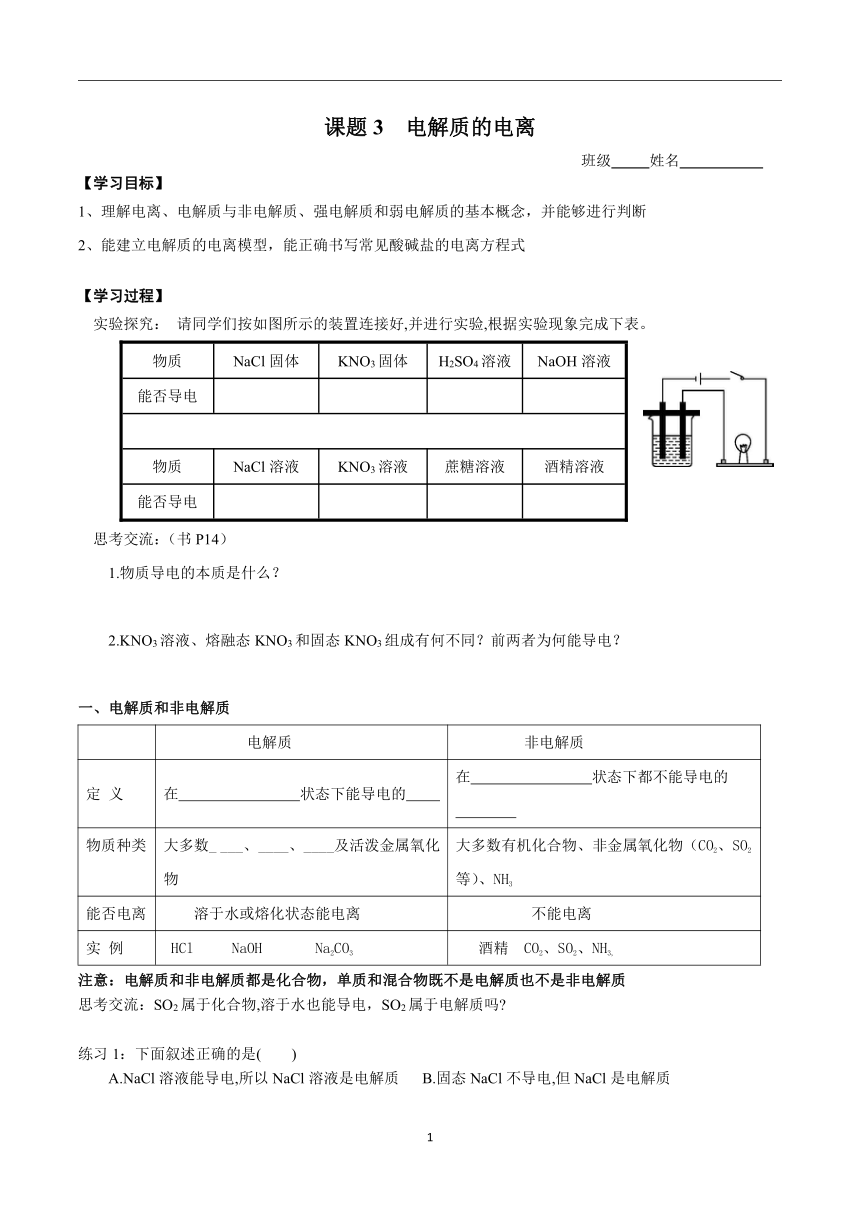
课题3 电解质的电离 班级 姓名 【学习目标】 1、理解电离、电解质与非电解质、强电解质和弱电解质的基本概念,并能够进行判断 2、能建立电解质的电离模型,能正确书写常见酸碱盐的电离方程式 【学习过程】 实验探究: 请同学们按如图所示的装置连接好,并进行实验,根据实验现象完成下表。 物质 NaCl固体 KNO3固体 H2SO4溶液 NaOH溶液 能否导电 物质 NaCl溶液 KNO3溶液 蔗糖溶液 酒精溶液 能否导电 思考交流:(书P14) 1.物质导电的本质是什么? 2.KNO3溶液、熔融态KNO3和固态KNO3组成有何不同?前两者为何能导电? 一、电解质和非电解质 电解质 非电解质 定 义 在 状态下能导电的 在 状态下都不能导电的 物质种类 大多数_ ___、____、____及活泼金属氧化物 大多数有机化合物、非金属氧化物(CO2、SO2等)、NH3 能否电离 溶于水或熔化状态能电离 不能电离 实 例 HCl NaOH Na2CO3 酒精 CO2、SO2、NH3, 注意:电解质和非电解质都是化合物,单质和混合物既不是电解质也不是非电解质 思考交流:SO2属于化合物,溶于水也能导电,SO2属于电解质吗 练习1:下面叙述正确的是( ) A.NaCl溶液能导电,所以NaCl溶液是电解质 B.固态NaCl不导电,但NaCl是电解质 C.HCl水溶液能导电,所以HCl是电解质 D.SO3溶于水能导电,所以SO3是电解质 E.Cu能导电,所以是电解质 F.BaSO4的水溶液不能导电,所以BaSO4是非电解质 二、电离 1.概念: 2.电离的表示———电离方程式 如:NaCl = Na+ + Cl- 练习2:尝试书写以下物质的电离方程式,并将结果进行交流讨论。 KClO3 = H2SO4= Ba(OH)2 = 三、强电解质与弱电解质 强电解质 弱电解质 定 义 在水溶液中, 电离的电解质 在水溶液中, 电离的电解质 物质种类 强酸、强碱和许多盐类 弱酸、弱碱,H2O等 电离程度 电离 电离 溶质粒子 离子 和离子 实例 HCl、NaOH 、Ba(OH)2 、Ca(OH)2、Na2CO3 、BaSO4 醋酸(CH3COOH)、一水合氨(NH3·H2O)、氢硫酸(H2S)、H2CO3来源:Zx、亚硫酸(H2SO3x*)、次氯酸(HClO*)、Fe(OH)2、Fe(OH)3om2]、Cu(OH)2 练习3:写出下列物质在水溶液中的电离方程式。 (1)醋酸(CH3COOH): ; (2)一水合氨(NH3·H2O): ; (3)碳酸: ; (4)碳酸氢钠: ; (5)硫酸氢钠: ; 练习4:下列物质属于强电解质的是_____ ;属于弱电解质的是_____ 。 ①H2SO4 ②氨水 ③NaHCO3 ④H2CO3 ⑤盐酸 ⑥NH3 ⑦BaSO4 练习5:判断正误: ( )①AgCl难溶于水,所以AgCl是弱电解质。 ( )②盐酸的导电性一定比醋酸的导电性强。 ( )③导电性弱的电解质溶液,电解质为弱电解质。 ( )④熔融的电解质都能导电 ( )⑤强电解质溶液中,不存在分子。 【课后限时练】 【A基础夯实】 1.下列物质中,导电性能最差的是( ) A.熔融的氢氧化钠 B.石墨棒 C.盐酸溶液 D.固态氯化钾 2.下列物质中,属于电解质的是( ) A.二氧化氮 B.蔗糖 C.铜 D.硝酸钾 3.化学兴趣小组在家中进行化学实验,按照左图连接好线路发现灯泡不亮,按照右图连接好线路发现灯泡亮,由此得出的结论正确的是( ) A.NaCl是非电解质 B.NaCl溶液是电解质 C.NaCl在水溶液中电离出了可以自由移动的离子 D.NaCl溶液中,水电离出大量的离子 4.在下列化合物中,只有在水溶液中才能导电的电解质是( ) A.NaCl B.酒精 C.H2SO4 D.KCl 5.下列物质既不是电解质,又不是非电解质的是( ) A.NaHSO4 B.Cu(OH)2 C.O2 D.HCl 6.下列物质的水溶液能导电,但属于非电解质的是( ) A.CH3COOH B.Cl2 C.NH4HCO3 D.NH3 7.下列物质的水溶液中存在溶质分子的是( ) A.HCl B.NaOH C.Na2CO3 D.蔗糖 8.下列说法正确的是( ) ... ...
~~ 您好,已阅读到文档的结尾了 ~~