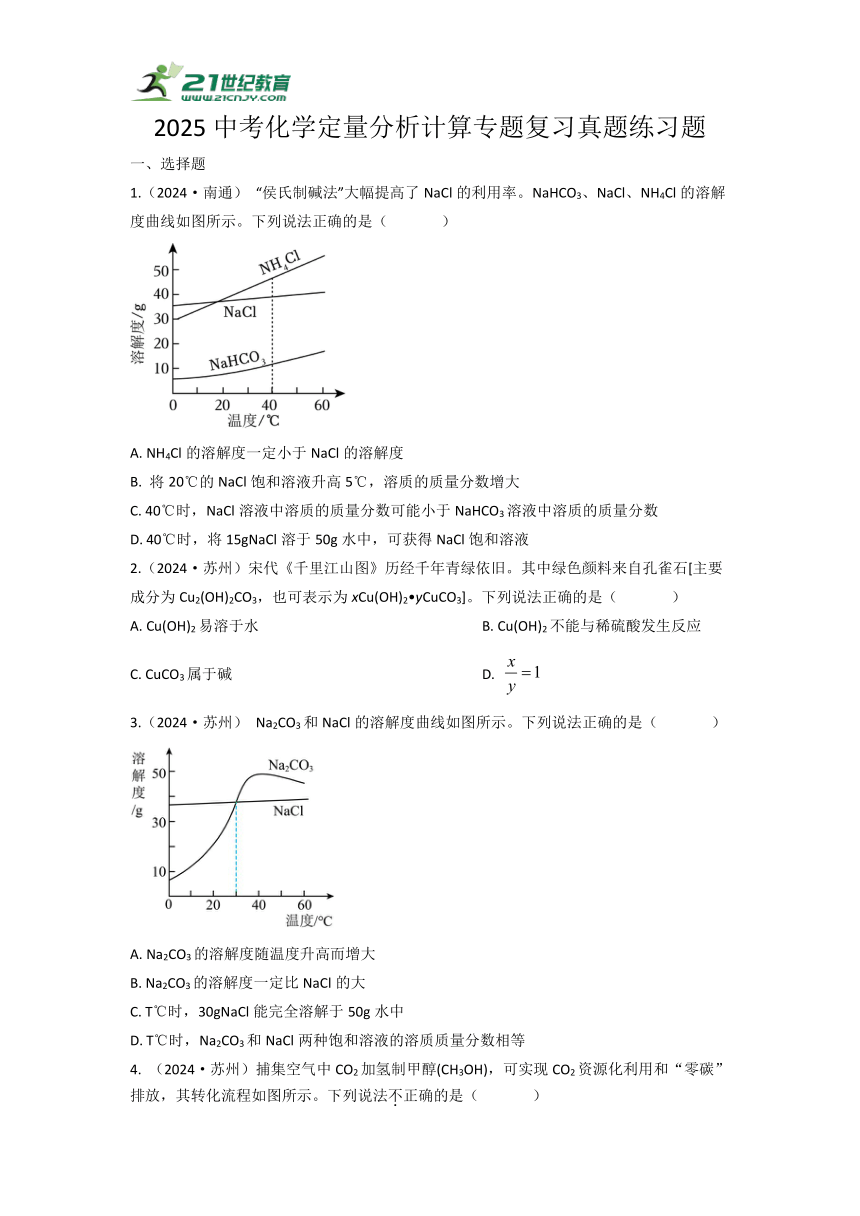
2025中考化学定量分析计算专题复习真题练习题 一、选择题 1.(2024·南通) “侯氏制碱法”大幅提高了NaCl的利用率。NaHCO3、NaCl、NH4Cl的溶解度曲线如图所示。下列说法正确的是( ) A. NH4Cl的溶解度一定小于NaCl的溶解度 B. 将20℃的NaCl饱和溶液升高5℃,溶质的质量分数增大 C. 40℃时,NaCl溶液中溶质的质量分数可能小于NaHCO3溶液中溶质的质量分数 D. 40℃时,将15gNaCl溶于50g水中,可获得NaCl饱和溶液 2.(2024·苏州)宋代《千里江山图》历经千年青绿依旧。其中绿色颜料来自孔雀石[主要成分为Cu2(OH)2CO3,也可表示为xCu(OH)2 yCuCO3]。下列说法正确的是( ) A. Cu(OH)2易溶于水 B. Cu(OH)2不能与稀硫酸发生反应 C. CuCO3属于碱 D. 3.(2024·苏州) Na2CO3和NaCl的溶解度曲线如图所示。下列说法正确的是( ) A. Na2CO3的溶解度随温度升高而增大 B. Na2CO3的溶解度一定比NaCl的大 C. T℃时,30gNaCl能完全溶解于50g水中 D. T℃时,Na2CO3和NaCl两种饱和溶液的溶质质量分数相等 4. (2024·苏州)捕集空气中CO2加氢制甲醇(CH3OH),可实现CO2资源化利用和“零碳”排放,其转化流程如图所示。下列说法不正确的是( ) A. 反应①中,电解水生成的H2和O2的分子个数比为2:1 B. 反应②中,生产1.6kgCH3OH理论上要消耗2.2kgCO2 C. 转化过程中,H2O和H2循环转化,无需额外补充 D. 等质量的甲醇制取时消耗的CO2与燃烧时生成的CO2相等,实现“零碳”排放 5.(2024南通) 学习小组为探究氢气还原氧化铜所得固体产物X组成,设计如下实验: 步骤1 观察产物X的颜色为红色。 步骤2 向产物X中加入过量的盐酸充分反应,过滤得到9.6g红色固体和蓝色溶液。 步骤3 向步骤2所得蓝色溶液中加入过量的Na2H2Y溶液,测得与CuCl2反应的Na2H2Y的质量为33.6g。 已知:①Na2H2Y的相对分子质量为336 ②Cu2O为红色固体 ③Cu2O+2HCl=Cu+CuCl2+H2O CuCl2+Na2H2Y=CuH2Y+2NaCl 下列说法正确的是( ) A. 产物X为Cu单质 B. 步骤2所得蓝色溶液中仅含有Cu2+、Cl﹣两种离子 C. 步骤3中参加反应的CuCl2的质量为27g D. 产物X中Cu元素的质量分数为90.9% 6.(2024·无锡) 维生素C(C6H8O6)可以调节人体的新陈代谢。下列叙述正确的是( ) A. 维生素C属于有机高分子化合物 B. 维生素C由碳、氢、氧三种元素组成 C. 维生素C由20个原子构成 D. 维生素C中氢元素的质量分数最高 7. (2024·无锡)一定条件下,甲和乙反应的微观过程如图所示。下列叙述正确的是( ) A. 甲、乙、丙、丁中有3种氧化物 B. 反应前后原子种类改变 C. 参加反应的甲和乙的分子个数比为1:1 D. 反应生成的丙和丁的质量比为5:3 8. (2024·徐州)为了实现碳的资源化利用,我国科学家用纳米镍粒子作催化剂将二氧化碳合成甲烷,反应的化学方程式为。下列说法正确的是( ) A. X的化学式为H2O2 B. 甲烷中碳、氢元素的质量比为3∶1 C. 反应前后分子的数目不变 D. 参加反应的CO2和H2的质量比为22∶1 9.(2024·盐城)同学们课后走进实验室,回收处理金属Mg、Cu与氧气反应的废弃物。取和粉末的混合物5g,加入一定量的稀硫酸恰好完全反应,得到100g含硫元素质量分数为的不饱和溶液;经多步处理后,得13g晶体(不含结晶水)。则原混合物中Mg、Cu两种元素质量分数之和为( ) A. B. C. D. 10. (2024·镇江)已知:2NaHCO3Na2CO3+CO2↑+H2O,将16.8gNaHCO3固体加热一段时间后,剩余固体质量为13.7g。下列说法正确的是( ) A. 原固体加热生成3.1gCO2 B. 加热后,固体中钠元素的质量分数减小 C. 剩余固体中NaHCO3和Na2CO3的质量比为42:53 D. 将13.7g剩余固体溶于足量盐酸后,蒸发结晶,得11.7gNaCl 11.(2024·江西)向盛有一定量氢氧化钙溶液的烧杯中通入适量的二氧化碳气体,反应过程中相关量Y与反应 ... ...
~~ 您好,已阅读到文档的结尾了 ~~