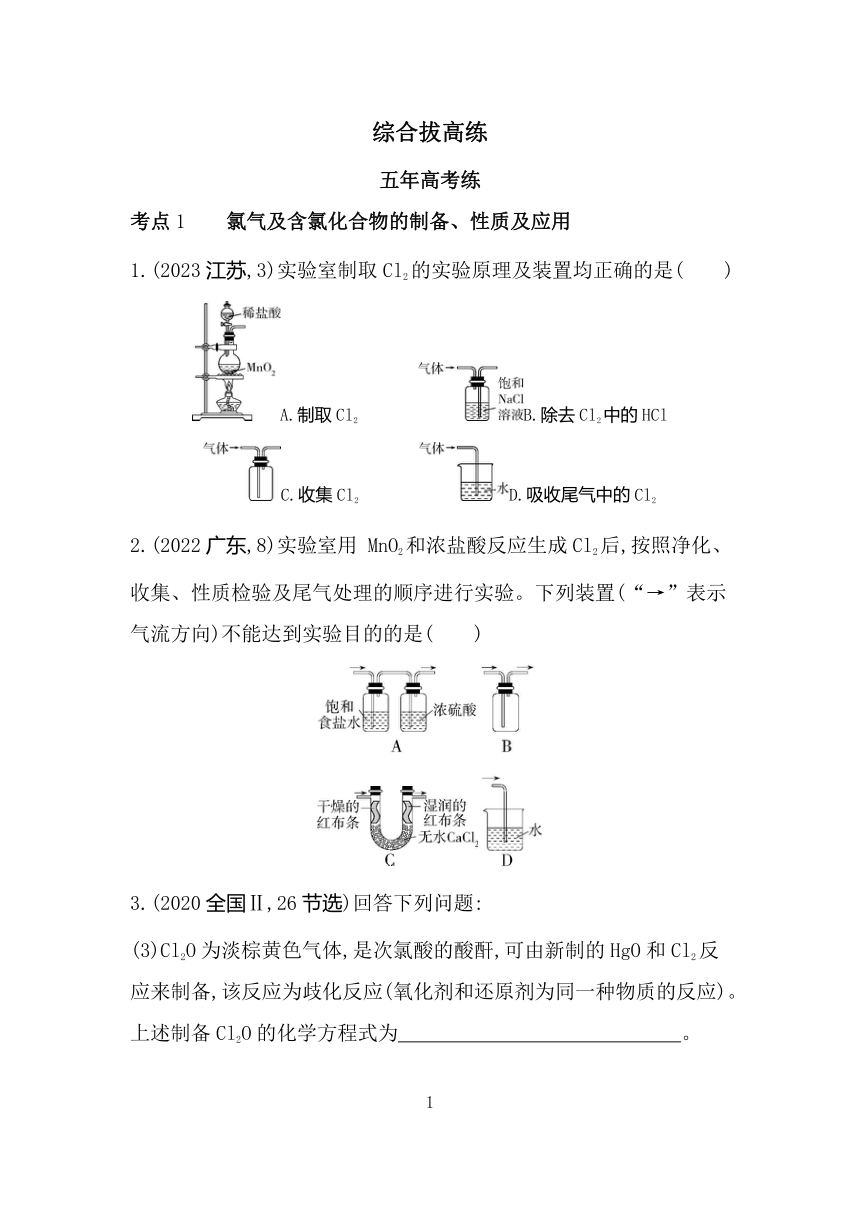
综合拔高练 五年高考练 考点1 氯气及含氯化合物的制备、性质及应用 1.(2023江苏,3)实验室制取Cl2的实验原理及装置均正确的是( ) A.制取Cl2 B.除去Cl2中的HCl C.收集Cl2 D.吸收尾气中的Cl2 2.(2022广东,8)实验室用 MnO2和浓盐酸反应生成Cl2后,按照净化、收集、性质检验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是( ) 3.(2020全国Ⅱ,26节选)回答下列问题: (3)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为 。 (4)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为 mol;产生“气泡”的化学方程式为 。 (5)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是 (用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1 000 kg该溶液需消耗氯气的质量为 kg(保留整数)。 4.(2021广东,17节选)含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,并命名为chlorine(中文命名“氯气”)。 (1)实验室沿用舍勒的方法制取Cl2的化学方程式为 。 (2)实验室制取干燥Cl2时,净化与收集Cl2所需装置的接口连接顺序为 。 (3)某氯水久置后不能使品红溶液褪色,可推测氯水中 已分解。检验此久置氯水中Cl-存在的操作及现象是 。 5.(2020山东,20节选)某同学利用Cl2氧化K2MnO4制备KMnO4的装置如图所示(夹持装置略): 已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应: 3Mn+2H2O 2Mn+MnO2↓+4OH- 回答下列问题: (1)装置A中a的作用是 ;装置C中的试剂为 ;装置A中制备Cl2的化学方程式为 。 (2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是 。 考点2 氧化还原反应及相关规律 6.(2021广东,15)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应方程式书写正确的是( ) A.Na2O2放入水中:Na2O2+H2O2NaOH+O2↑ B.H2O(g)通过灼热铁粉:3H2O+2FeFe2O3+3H2 C.铜丝插入热的浓硫酸中:Cu+H2SO4CuSO4+H2↑ D.SO2通入酸性KMnO4溶液中:5SO2+2H2O+2Mn5S+4H++2Mn2+ 7.(2022山东,8)实验室制备KMnO4过程为①高温下在熔融强碱性介质中用KClO3氧化MnO2制备K2MnO4;②水溶后冷却,调溶液pH至弱碱性,K2MnO4歧化生成KMnO4和MnO2;③减压过滤,将滤液蒸发浓缩、冷却结晶,再减压过滤得KMnO4。下列说法正确的是( ) A.①中用瓷坩埚作反应器 B.①中用NaOH作强碱性介质 C.②中K2MnO4只体现氧化性 D.MnO2转化为KMnO4的理论转化率约为66.7% 8.(2021山东,13改编)实验室中利用固体KMnO4进行如下实验,下列说法错误的是( ) →固体→→气体单质H A.G与H均为氧化产物 B.KMnO4既是氧化剂又是还原剂 C.Mn元素至少参与了3个氧化还原反应 ... ...
~~ 您好,已阅读到文档的结尾了 ~~

