(
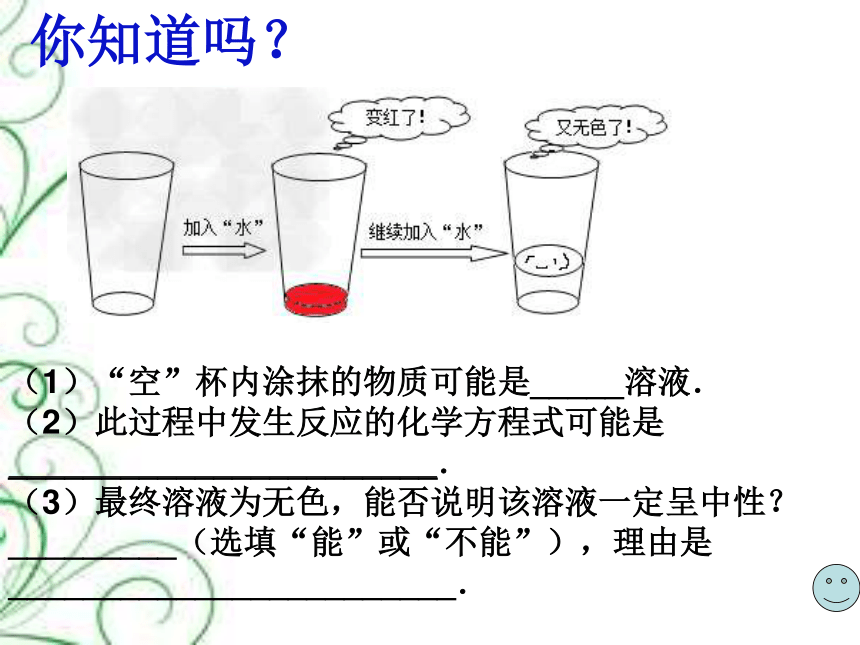
课件网) 你知道吗? (1)“空”杯内涂抹的物质可能是_____溶液. (2)此过程中发生反应的化学方程式可能是_____. (3)最终溶液为无色,能否说明该溶液一定呈中性?_____(选填“能”或“不能”),理由是_____. 蚊子叮咬 蚊虫叮咬时,在蚊子的口器中分泌出一种有机酸--蚁酸,在家庭中可用浓肥皂水涂抹可迅速止痒。 切身体会: 第十单元 酸和碱 课题2 酸碱的中和反应(1) 学生探究: (1)取一支试管,加入少量NaOH 溶液 (2)用滴管加入HCl; (3)观察现象。 想一想: 酸与碱有没有发生反应呢? 如何证明氢氧化钠和盐酸 发生了反应? 请小组合作,将你们的实验方案写在导学案上。 投影展示 方案展示: 方案一:在烧杯中加入少量NaOH ,然后滴入几 滴酚酞溶液,再用滴管慢慢滴加稀盐酸,边滴加边 搅拌,至溶液恰好变成无色为止。 方案二:在烧杯中加入少量HCl溶液,然后滴加几滴 紫色石蕊,再用滴管慢慢滴加氢氧化钠溶液,边滴加 边搅拌,至溶液恰好由红色变为紫色为止。 方案三:在烧杯中加入少量NaOH 溶液,测量温度; 另一个烧杯中加入少量HCl溶液,测量温度;将两烧杯 中的液体混合,再次测量温度。观察温度有没有 升高? 合作探究:氢氧化钠和盐酸会发生什么? NaOH溶液 滴入( )溶液 溶液为( )色 再滴入( )溶液 溶液为( )色 无色酚酞 红 盐酸 无 HCl溶液 滴入(紫色石蕊) 溶液 溶液为( 红 )色 再滴入( NaOH )溶液 溶液为( 紫 )色 小组展示: NaOH 溶液和稀盐酸混合后溶液的 温度有变化吗?升高还是降低? 思考: 氢氧化钠和盐酸的反应有 什么特点? NaOH + HCl = NaCl + H2O 碱 酸 水 盐 注意: 这个“盐”是指一类物质,和平时说的“食盐”不同! 归纳总结: 想一想:下列反应有何共同特点? NaOH+HCl == NaCl + H2O Ca(OH)2+2HCl== CaCl2 + 2H2O 2NaOH + H2SO4== Na2SO4 + 2H2O 酸根离子 盐 盐:由金属离子(铵根离子NH4+ )和酸根离子组成的化合物 酸 + 碱 → 盐 + 水 酸和碱作用生成盐和水的反应。 中和反应: 注意:有盐和水生成的反应一定是中和反应吗? 练一练: 分别写出氢氧化钙和盐酸、稀硫酸, 氢氧化钠和稀硫酸反应的方程式 Ca(OH)2 + 2HCl = CaCl2 + 2H2O Ca(OH)2 + H2SO4 = CaSO4 + 2H2O 2NaOH + H2SO4 = Na2SO4 + 2H2O 中和反应的实质: + 你认为判断一个反应是不是中和反应的关键是什么? 反应物必须是酸与碱, 生成物必须是盐和水 用适量盐酸可以将热水瓶胆壁上的水垢[主要成分是Mg(OH)2和CaCO3]除去。说明去垢的原理,写出有关的化学方程式。 Mg(OH)2+2HCl=MgCl2+2H2O CaCO3+2HCl=CaCl2+CO2↑+H2O 盐酸将不溶性的Mg(OH)2和CaCO3生成可溶性的氯化镁和氯化钙而便于洗去。 二、中和反应在实际中的应用 植物需要在一定酸碱性的土壤中生长,但近年来由于不合理使用化肥,或酸雨的形成,破坏土壤的酸碱性,不利于植物的生长,应怎样去改变酸性土壤? 用熟石灰中和。 你会处理废水吗? 某硫酸厂排出的废水中含有硫酸等杂质,严重危害当地的生态环境,你会怎样处理这些废水呢? 用碱性物质(例如熟石灰)进行中和处理。 Ca(OH)2 + H2 SO4 == CaSO4 + 2H2O 胃药胶囊的主要成分 你知道它的作用吗? 胃酸的主要成分是 盐酸 氢氧化铝 [思考] 此药中含有氢氧化铝,试写出治胃酸过多 的原理 3HCl+Al(OH)3 = AlCl3+3H2O 拓展提升: 1、下列物质能与盐酸发生中和反应的是( ) A、 硝酸银 B、氧化铜 C、熟石灰 D、锌 拓展提升: 2、下列各组物质间的反应,由于现象不明显 需要借助酸碱指示剂才能判断出反应发生的 是( ) A、 镁和稀盐酸 B 、烧碱溶液和稀硫酸 C、氧化铁和稀硫酸 D、澄清石灰水中通入二氧化碳 3、将稀盐酸慢慢滴入盛有 ... ...