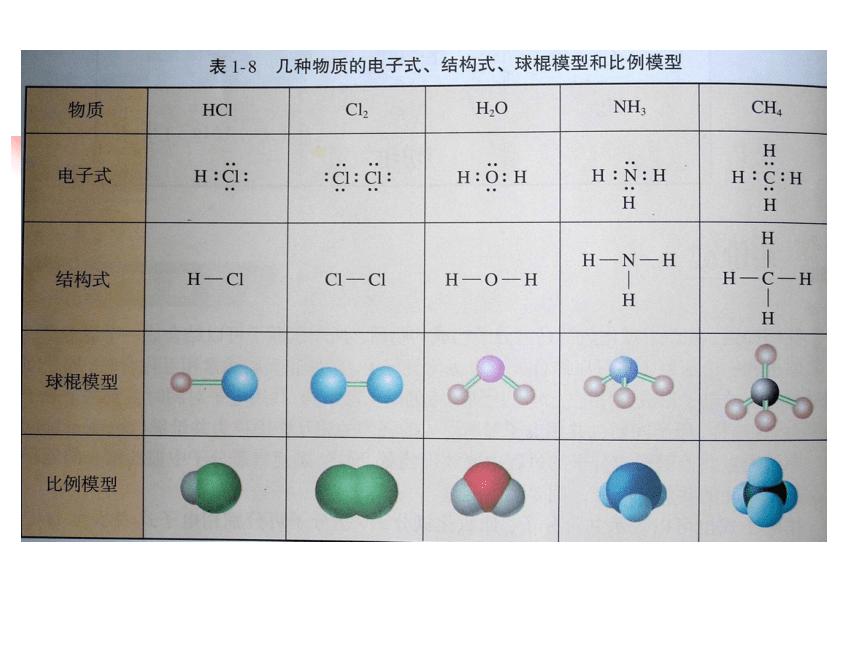
课件29张PPT。 共价化合物分子中各原子有一定的连接方式,分子有一定的空间结构,可以用球棍模型、比例模型表示共价分子的空间结构。离子键和共价键的比较H-Cl阴、阳离子原子静电作用共用电子对典型的金属元素、典型的非金属元素之间 强碱、大部分盐、低价金属氧化物等同种元素或同类非金属元素之间 酸、非金属单质、非金属氧化物、气态氢化物、有机物等指出下列化合物内部的键型和化合物的分类 (离子化合物、共价化合物)共价键离子键既有离子键又有共价键 离子化合物离子键共价键既有离子键又有共价键 离子化合物共价化合物共价化合物离子化合物离子化合物离子键与共价键的关系———键的多重性 离子键 共价键 离子键、共价键 离子化合物共价化合物离子化合物如:NaOH8e-不是唯一的稳定结构,在共价化合物 中,有的原子最外层电子数少于8e- ,而有的原子最外层电子比8e-多. 一个化学反应的的过程,本质上就是旧化学键断裂和新化学键形成的过程。讨论: 用化学键的观点来分析化学反应的本质是什么?化学键的形成放出能量化学键的断裂吸收能量几种重要的物质的电子式:NaOHNH4Cl影响共价键强弱的因素:(1)原子半径 :成键半径越小,共价键越强* 共用电子对数目的确定: 8-最外层电子数(2)共用电子对数目:电子对数目越多,共价键越强如:下列分子中,共价键最强的是( ) A、H-Cl B、F-F C、H-F D、H-OC指出下列化合物所含化学键类型:NaBr、H2S、NaOH、SO2、NH4NO3 属于离子化合物的有 属属于共价化合物的有 . 并判断对错: 1、含有共价键的化合物一定是共价化合物。 2、共价化合物只含共价键。 3、含有离子键的化合物一定是离子化合物。 4、离子化合物只含离子键。 5、只含有共价键的物质一定是共价化合物。 6、氦气是共价化合物。 稀有气体元素结构稳定,是单原子分子,没有形成共价键错(NaOH)错(单质)对错对错(NaOH)NaBr、NaOH、NH4NO3H2S 、SO2微粒间的作用———三键一力1、三键一力化学键离子键共价键金属键分子间作用力 “三键一力”是微观粒子(原子、分子、离子)结合 在一起构成客观物质的四种基本作用力,它的强弱不仅 决定着物质的存在形态(气、固、液),熔沸点高低, 硬度大小,而且与物质的化学性质也有密切的关系2、化学键:使离子相结合或使原子相结合的作用力分子间作用力【问题探究一】干冰气化现象是物理变化还是化学变化?干冰气化过程中有没有破坏其中的化学键?那为什么干冰气化过程仍要吸收能量呢?分子间作用力 分子间存在着将分子聚集在一起的作用力,这种作用力称为分子间作用力又称为范德华力【问题探究二】干冰汽化后化学性质是否发生变化? 分子间作用力对物质化学性质有没有影响?分子间作用力的特点1.广泛存在(由分子构成的物质)2.作用范围小3.作用力弱4.主要影响物质的物理性质(熔沸点)相邻的原子间强烈的相互作用把分子聚集在一起的作用力分子内原子间分子之间较 强与化学键相比弱的多主要影响化学性质主要影响物理性质(如熔沸点)化学键与分子间作用力的比较离子键、共价键、金属键、分子间作用力都是微粒间的作用力。下列物质中,只存在一种作用力的是 ( ) A.干冰 B.NaCl C.NaOH D.I2 E.H2SO4B【问题探究三】 分子间作用力如何影响物质的物理性质?卤族元素单质物理性质差异【拓展视野】氢 键1.氢键是一种特殊的分子间作用力,不是化学键H2O中的氢键【问题探究三】冰中的氢键4.氢键对物质性质的影响⑴氢键的存在使物质的熔沸点相对较高⑵解释一些反常现象:如水结成冰时,为什么体积会膨胀。固体冰中不存在的作用力是 ( ) A.离子键 B.共价键 C. 氢键 D. 范德华力 A 电子对偏向ClHCl分子 ... ...
~~ 您好,已阅读到文档的结尾了 ~~