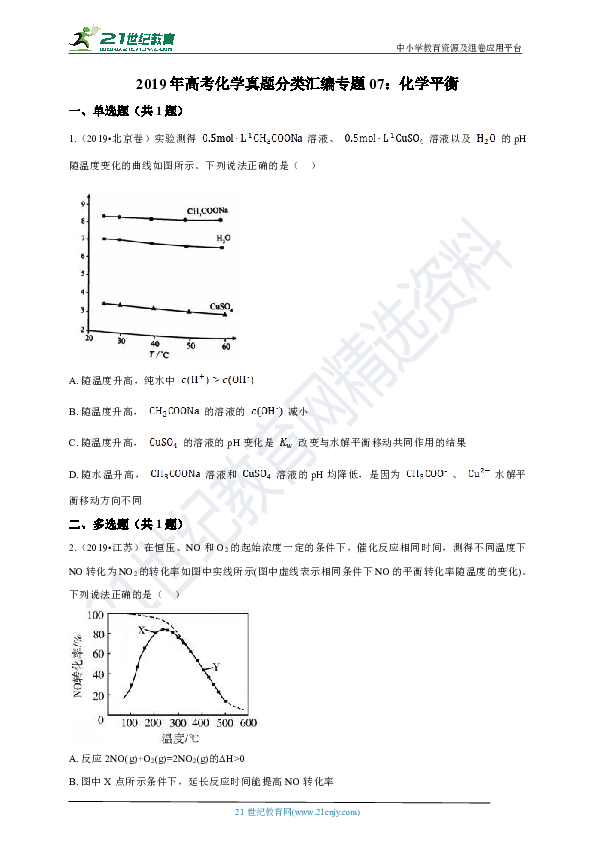
2019年高考化学真题分类汇编专题07:化学平衡 一、单选题(共1题) 1.(2019?北京卷)实验测得 溶液、 溶液以及 的pH随温度变化的曲线如图所示。下列说法正确的是(?? ) A.?随温度升高,纯水中 B.?随温度升高, 的溶液的 减小�C.?随温度升高, 的溶液的pH变化是 改变与水解平衡移动共同作用的结果�D.?随水温升高, 溶液和 溶液的pH均降低,是因为 、 水解平衡移动方向不同 二、多选题(共1题) 2.(2019?江苏)在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是(?? ) A.?反应2NO(g)+O2(g)=2NO2(g)的ΔH>0�B.?图中X点所示条件下,延长反应时间能提高NO转化率�C.?图中Y点所示条件下,增加O2的浓度不能提高NO转化率�D.?380℃下,c起始(O2)=5.0×10?4 mol·L?1 , NO平衡转化率为50%,则平衡常数K>2000 三、实验探究题(共2题) 3.(2019?全国Ⅱ)环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题: (1)已知: (g) =? (g)+H2(g)????? ΔH1=100.3 kJ·mol ?1???? ① H2(g)+ I2(g) =2HI(g)?????????????????????????? ΔH2=?11.0 kJ·mol ?1???? ② 对于反应: (g)+ I2(g) = (g)+2HI(g)? ③? ΔH3=_____kJ·mol ?1。 (2)某温度下,等物质的量的碘和环戊烯( )在刚性容器内发生反应③,起始总压为105Pa,平衡时总压增加了20%,环戊烯的转化率为_____,该反应的平衡常数Kp=_____Pa。达到平衡后,欲增加环戊烯的平衡转化率,可采取的措施有_____(填标号)。 A.通入惰性气体??????????????B.提高温度 C.增加环戊烯浓度??????????? D.增加碘浓度 (3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯浓度与反应时间的关系如图所示,下列说法正确的是_____(填标号)。 A.?T1>T2??????????????????????????????????????????????????????????????? B.?a点的反应速率小于c点的反应速率�C.?a点的正反应速率大于b点的逆反应速率??????????????D.?b点时二聚体的浓度为0.45 mol·L?1 (4)环戊二烯可用于制备二茂铁(Fe(C5H5)2结构简式为 ),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。 该电解池的阳极为_____,总反应为_____。电解制备需要在无水条件下进行,原因为_____。 4.(2019?全国Ⅲ)近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题: (1)Deacon发明的直接氧化法为:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)。下图为刚性容器中,进料浓度比c(HCl) ∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系: 可知反应平衡常数K(300℃)_____K(400℃)(填“大于”或“小于”)。设HCl初始浓度为c0 , 根据进料浓度比c(HCl)∶c(O2)=1∶1的数据计算K(400℃)=_____(列出计算式)。按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O2)过低、过高的不利影响分别是_____。 (2)Deacon直接氧化法可按下列催化过程进行: CuCl2(s)=CuCl(s)+ Cl2(g)? ΔH1=83 kJ·mol-1 CuCl(s)+ O2(g)=CuO(s)+ Cl2(g)?? ΔH2=-20 kJ·mol-1 CuO(s)+2HCl(g)=CuCl2(s)+H2O(g)??? ΔH3=-121 kJ·mol-1 则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH=_____ kJ·mol-1。 (3)在一定温度的条件下,进一步提高HCl的转化率的方法是_____。(写出2种)�(4)在传统的电解氯化氢回收氯气技术的基础上,科学家 ... ...
~~ 您好,已阅读到文档的结尾了 ~~

