(
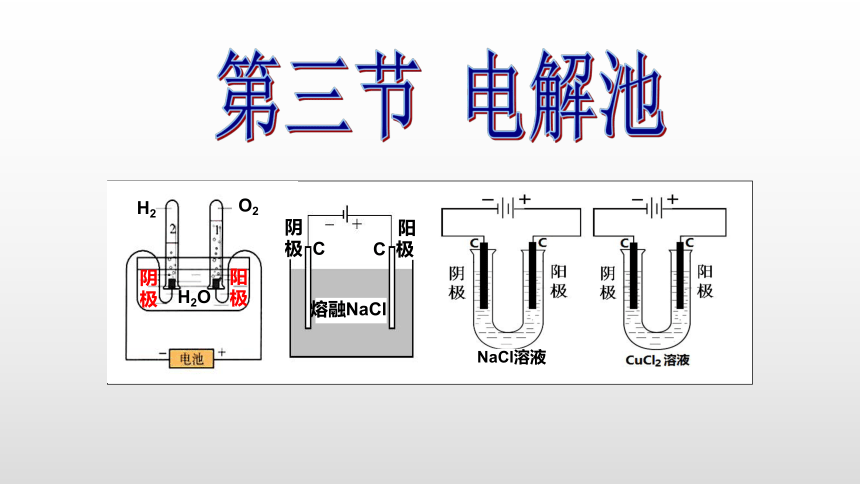
课件网) 第三节 电解池 NaCl溶液 H2 O2 H2O 熔融NaCl 阴 极 C 阳 C 极 阴 极 阳 极 思考: 1.什么叫电解池,怎么判断装置属于电解池? 2.电解池的结构如何? 两极的名称叫什么? 怎么判断两极? 两极分别发生什么反应? 怎么写电极方程式? 练一练 Fe Cu 氯化铜溶液 氯化铜溶液 C C A B Fe Cu 盐酸溶液 1、分析下图,属于电解池的是( ) C Cu 氯化铜溶液 D C D 一、电解原理: 1.电解:电流通过电解质溶液(或熔融电解质) 而在阴、阳两极引起氧化还原反应的过程。 2.电解池:电能转化为化学能的装置。 二、构成电解池的条件: 1.直流电源 2.两个电极: 3.电解质溶液或熔融的电解质; 4.闭合回路。 阴极:与电源负极相连 [还原反应] 阳极:与电源正极相连 [氧化反应] 1.电解: 2.电解池: 三、放电顺序: 阴极—阳离子,得电子能力(氧化性)强的离子先得 活泼金属 > S2->I->Br->Cl->OH- >…含氧酸根>F- 阳极—阴离子 ,失电子能力(还原性)强的离子先失 Ag+>Hg2+>Cu2+>H+>Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca2+>K+ (与离子得失电子的难易程度有关) 强者先上! 若以活泼金属(相对于Au、Pt、石墨)电极为阳极如Fe、Cu、Ag,阳极金属本身易失电子,故金属失电子。 现象: H2O H++OH- CuCl2=Cu2++2Cl- 阳极产生黄绿色气体, 阴极析出红色物质。 阳极:2Cl--2e-=Cl2↑ 阴极:Cu2++2e-=Cu CuCl2 Cl2↑+Cu 电解 电极反应式: 总反应式: e- e- 阳极:Fe-2e-=Fe2+ 阴极:2H++2e-=H2 ↑ 电极反应式: 总反应式: Fe+2H2O H2 ↑+Fe(OH)2 电解 e- e- 现象: 阳极铁丝溶解。 阴极产生无色气体,滴加酚酞溶液变红。 H2O H++OH- NaCl=Na+ +Cl- 阳极:2Cl--2e-=Cl2↑ 阴极:2H++2e-=H2 ↑ 电极反应式: 现象: 总反应式: 2NaCl +2H2O Cl2↑+ H2↑+2NaOH 2Cl- +2H2O Cl2↑+ H2 ↑+2OH- 电解 电解 e- e- 阳极产生黄绿色气体,使湿润的淀粉KI试纸变蓝。 阴极产生无色气体,滴加酚酞溶液变红。 H2 O2 H2O 阴 极 阳 极 现象:阴极和阳极上均产生气泡,体积比约为2:1。 Pt 阳极:4OH--4e-=2H2O+O2↑ 阴极:4H++4e-=2H2↑ 电极反应式: H+ 2H2O 2H2 ↑ +O2 ↑ 电解 OH- H2O H++OH- e- e- 2NaCl(熔融) 2Na +Cl2 ↑ 熔融NaCl 阴 极 C 阳 C 极 电解 NaCl=Na+ +Cl- 阳极:2Cl--2e-=Cl2↑ 阴极:2Na++2e-=2Na 电极反应式: 现象:阳极产生黄绿色气体。 e- e- 1、标出图中电解池的阴、阳极。 2、写出电极反应式和总反应式 阳极:4OH--4e-=2H2O+O2↑ 阴极:4H++4e-=2H2↑ 2H2O 2H2 ↑ +O2 ↑ 电解 阴 极 阳 极 阴 极 阳 极 Cu Fe (3)稀H2SO4 Cu Fe (4)CuSO4溶液 + - 阳极 阴极 + - 阳极 阴极 下列装置的电极反应式和总反应化学方程式? 阳极:Cu-2e-=Cu2+ 阴极:2H++2e-=H2↑ Cu+2H2SO4 H2↑+CuSO4 电解 阳极:Cu-2e-=Cu2+ 阴极:Cu2++2e-=Cu CuSO4溶液浓度不变。 电镀池 C Fe NaCl溶液 氯碱工业:电解饱和食盐水制取氯气、烧碱和氢气。 电解槽 Cl2 H2 NaOH 溶液 含少量NaOH 的水 精制食盐水 淡盐水 阳极:2Cl--2e-=Cl2↑ 阴极:2H++2e-=H2 ↑ 2NaCl +2H2O Cl2↑+ H2↑+2NaOH 电解 Cl2 H2 NaOH 溶液 含少量NaOH 的水 精制食盐水 淡盐水 CuSO4溶液 Cu Fe 电镀铜—在铁片上镀铜。 待镀金属:Fe 镀层金属:Cu 电镀液: 阴极: 阳极: 含镀层金属阳离子Cu2+ 电镀池 电极反应式: 阳极:Cu - 2e-=Cu2+ 阴极:Cu2+ + 2e-=Cu CuSO4溶液浓度不变。 CuSO4溶液 粗铜 纯铜 铜的精炼 粗铜中常含有少量的Zn、Fe、Ag等金属杂质。 粗铜 纯铜 电解质溶液: 阳极: 阴极: 电极反应式: 阳极: 阴极:Cu2+ + 2e-=Cu Cu - 2e-=Cu2+ Zn - 2e-=Zn2+ Fe - 2e-=Fe2+ 阳极泥: 金、银等 含Cu2+ CuSO4浓度减小。 电冶金—电解法冶炼活泼金属 2NaCl(熔融 ... ...