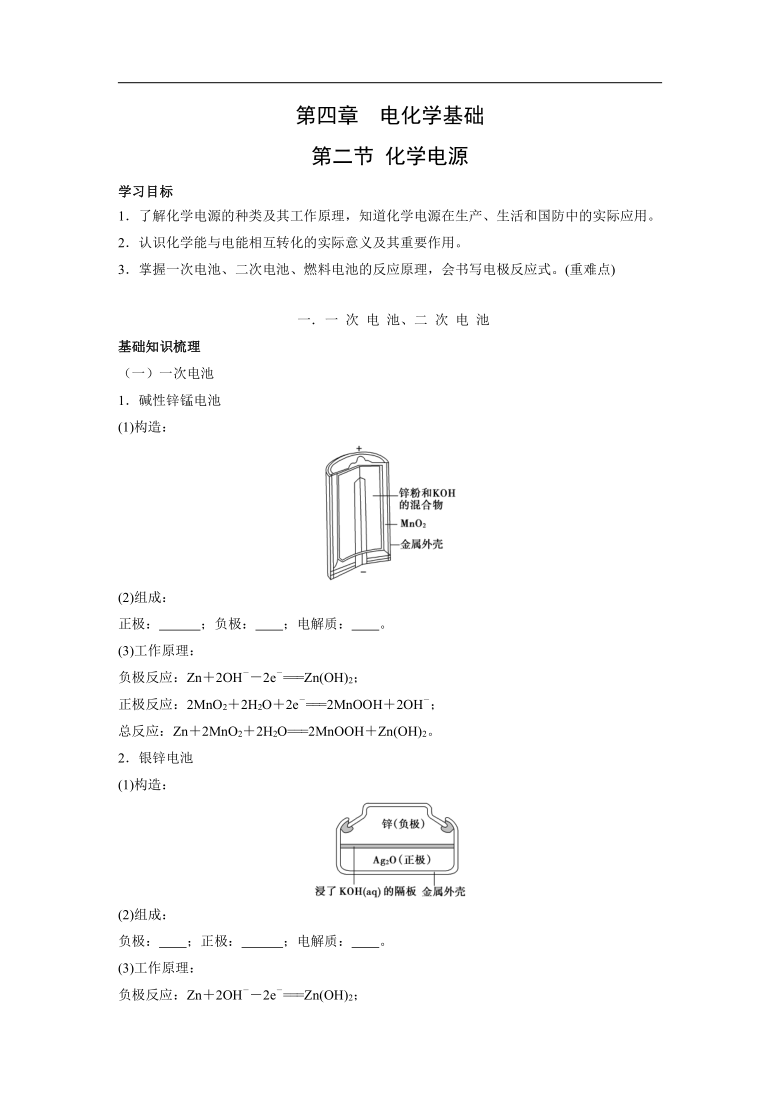
第四章 电化学基础 第二节 化学电源 学习目标 1.了解化学电源的种类及其工作原理,知道化学电源在生产、生活和国防中的实际应用。 2.认识化学能与电能相互转化的实际意义及其重要作用。 3.掌握一次电池、二次电池、燃料电池的反应原理,会书写电极反应式。(重难点) 一.一 次 电 池、二 次 电 池 基础知识梳理 (一)一次电池 1.碱性锌锰电池 (1)构造: (2)组成: 正极: ;负极: ;电解质: 。 (3)工作原理: 负极反应:Zn+2OH--2e-===Zn(OH)2; 正极反应:2MnO2+2H2O+2e-===2MnOOH+2OH-; 总反应:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2。 2.银锌电池 (1)构造: (2)组成: 负极: ;正极: ;电解质: 。 (3)工作原理: 负极反应:Zn+2OH--2e-===Zn(OH)2; 正极反应:Ag2O+H2O+2e-===2Ag+2OH-; (二)二次电池(以铅蓄电池为例) 1.构造 2.组成 负极: ;正极: ;电解质: 。 3.工作原理 (1)放电过程: 负极:Pb(s)+SO(aq)-2e-===PbSO4(s)(氧化反应); 正极:PbO2(s)+4H+(aq)+SO(aq)+2e-===PbSO4(s)+2H2O(l) 总反应:Pb(s)+PbO2(s)+2H2SO4(aq)===2PbSO4(s)+2H2O(l) (2)充电过程: 阴极:PbSO4(s)+2e-===Pb(s)+SO(aq); 阳极:PbSO4(s)+2H2O(l)-2e-===PbO2(s)+4H+(aq)+SO(aq); 总反应:2PbSO4(s)+2H2O(l)===Pb(s)+PbO2(s)+2H2SO4(aq)。 (3)铅蓄电池的充、放电过程: Pb+PbO2+2H2SO42PbSO4+2H2O 互动探究 [思考探究] H2是一种优质燃料,热值高。一种充电电池的原料为H2,其电池反应为H2+2NiO(OH) 2Ni(OH)2,它具有比能量多等优点,常作为卫星的电源。 问题思考: (1)该电池属于一次电池还是二次电池? (2)该电池内电解质溶液呈酸性还是碱性? (3)放电时的电极反应式如何书写? (4)充电时的电极反应式如何书写? (5)电池充电时,外电源的负极连接二次电池的哪个电极? 归纳总结 1.二次电池在充电时,正、负电极上发生的反应正好与放电时阴、阳电极上发生的反应相反,因而充电时,二次电池的正极应与充电电源的正极相连接,电池的负极应与充电电源的负极相连接。 2.充电时发生的电极反应和总反应是放电时发生的反应的逆过程。 即时训练 题组1 一次电池的工作原理 1.人造卫星用到的一种高能电池———银锌电池,其电极反应式为:Zn+2OH--2e-===Zn(OH)2,Ag2O+H2O+2e-===2Ag+2OH-。根据反应式判断氧化银是( ) A.负极 被氧化 B.正极 被还原 C.负极 被还原 D.正极 被氧化 2.在碱性锌锰干电池中,已知氢氧化钾为电解质,发生的电池总反应:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2。下列关于该电池的电极反应,正确的是( ) A.负极反应为Zn-2e-===Zn2+ B.负极反应为Zn+2H2O-2e-===Zn(OH)2+2H+ C.正极反应为2MnO2+2H++2e-===2MnOOH D.正极反应为2MnO2+2H2O+2e-===2MnOOH+2OH- 题组2 二次电池的工作原理 3.一种充电电池放电时的电极反应为 H2+2OH--2e-===2H2O; NiO(OH)+H2O+e-===Ni(OH)2+OH-。 当为电池充电时,与外电源正极连接的电极上发生的反应是( ) A.H2O的还原 B.NiO(OH)的还原 C.H2的氧化 D.Ni(OH)2的氧化 4.关于铅蓄电池的说法中正确的是( ) A.在放电时,正极发生的反应是:Pb(s)+SO(aq)===PbSO4(s)+2e- B.在放电时,该电池的负极材料是铅板 C.在充电时,电池中硫酸的浓度不断变小 D.在充电时,阳极发生的反应是:PbSO4(s)+2e-===Pb(s)+SO(aq) 二.燃 料 电 池 基础知识梳理 氢氧燃料电池 1.构造 2.电池总反应:2H2+O2===2H2O。 3.氢氧燃料电池在不同介质中的电极反应式 介质 负极反应式 正极反应式 酸性 2H2-4e-===4H+ O2+4H++4e- ... ...
~~ 您好,已阅读到文档的结尾了 ~~

