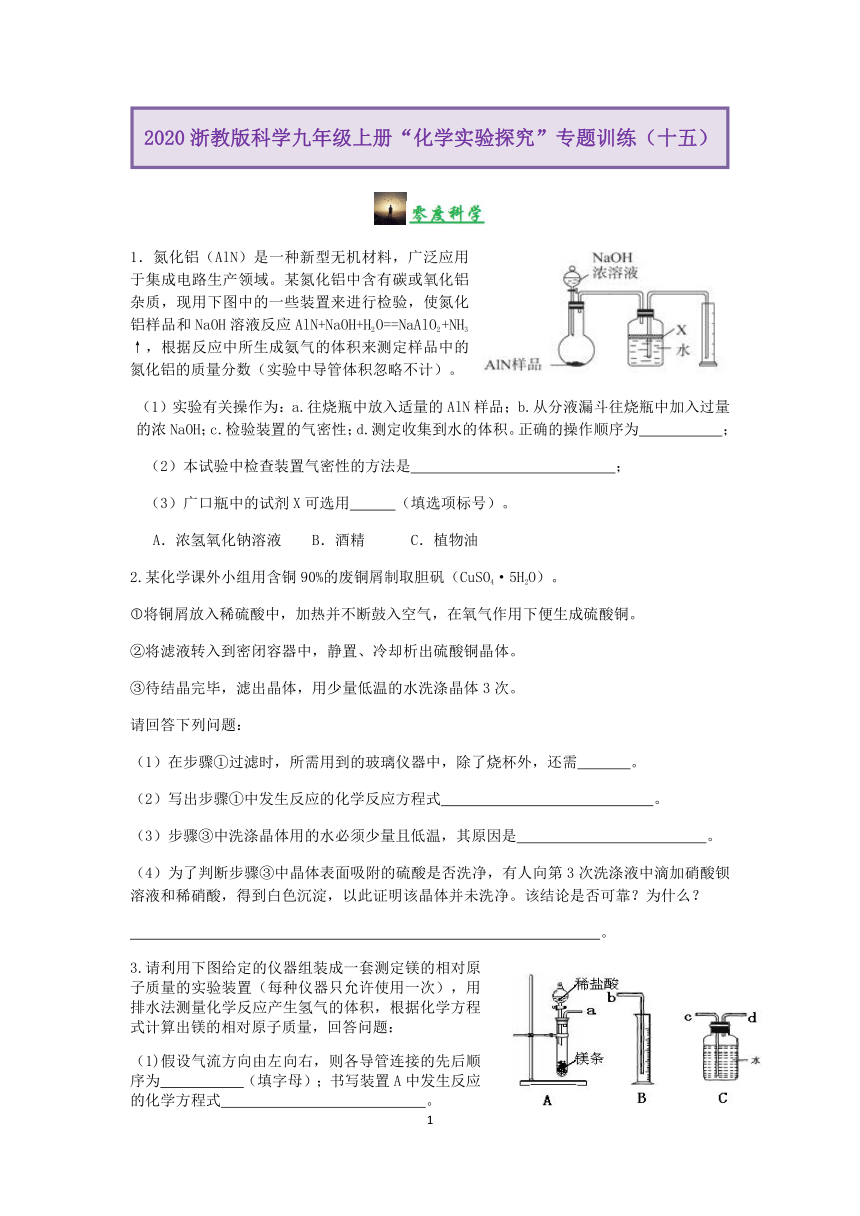
1.氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域。某氮化铝中含有碳或氧化铝杂质,现用下图中的一些装置来进行检验,使氮化铝样品和NaOH溶液反应AlN+NaOH+H2O==NaAlO2+NH3↑,根据反应中所生成氨气的体积来测定样品中的氮化铝的质量分数(实验中导管体积忽略不计)。 (1)实验有关操作为:a.往烧瓶中放入适量的AlN样品;b.从分液漏斗往烧瓶中加入过量的浓NaOH;c.检验装置的气密性;d.测定收集到水的体积。正确的操作顺序为 ; (2)本试验中检查装置气密性的方法是 ; (3)广口瓶中的试剂X可选用 (填选项标号)。 A.浓氢氧化钠溶液 B.酒精 C.植物油 2.某化学课外小组用含铜90%的废铜屑制取胆矾(CuSO4·5H2O)。 将铜屑放入稀硫酸中,加热并不断鼓入空气,在氧气作用下便生成硫酸铜。 ②将滤液转入到密闭容器中,静置、冷却析出硫酸铜晶体。 ③待结晶完毕,滤出晶体,用少量低温的水洗涤晶体3次。 请回答下列问题: (1)在步骤①过滤时,所需用到的玻璃仪器中,除了烧杯外,还需 。 (2)写出步骤①中发生反应的化学反应方程式 。 (3)步骤③中洗涤晶体用的水必须少量且低温,其原因是 。 (4)为了判断步骤③中晶体表面吸附的硫酸是否洗净,有人向第3次洗涤液中滴加硝酸钡溶液和稀硝酸,得到白色沉淀,以此证明该晶体并未洗净。该结论是否可靠?为什么? 。 3.请利用下图给定的仪器组装成一套测定镁的相对原子质量的实验装置(每种仪器只允许使用一次),用排水法测量化学反应产生氢气的体积,根据化学方程式计算出镁的相对原子质量,回答问题: (1)假设气流方向由左向右,则各导管连接的先后顺序为 (填字母);书写装置A中发生反应的化学方程式 。 (2)连接好仪器后,要进行的操作有以下几步:①待仪器A中的物质恢复至室温时,测量量筒B中水的体积。②擦掉镁条表面的氧化膜,将其置于天平上称量后,立即将其投入试管A中。③检查装置的气密性。④旋开仪器A上分液漏斗的活塞,当镁条完全溶解时再关闭活塞。上述几步操作中的先后顺序是 。 (3)分析下列其中一实验步骤出现的状况(其他操作均正确),将会使所测镁的相对原子质量数据偏低的是 (填字母)。 A.装置的气密性不够好 B.装置A的试管中剩余部分产生的氢气 C.若试管A尚未冷却至室温就测量量筒B中水的体积 D.若未擦净镁条表面氧化膜就进行实验 (4)假设在0℃、l01kPa条件下,氢气的密度为0. 0899g/L的条件下进行实验,将质量为M克的镁与足量稀盐酸反应产生氢气,收集并测量产生氢气体积为V毫升,计算镁的相对原子质量为 (填表达式)。 4. 过氧化钙晶体(化学式为CaO2·xH2O,其中x待实验中测定)常温下为白色,能溶于酸,难溶于水、乙醇,且温度越低,其溶解度越小,是一种温和的氧化剂,常用于鱼类长途运输的增氧剂等。 (1)过氧化钙晶体可用下列方法制备: CaCl2+H2O2+NH3+H2O―→CaO2·xH2O↓+NH4Cl。 用如下制取装置可制备过氧化钙晶体: ①装置A中生成的气体应为 ;仪器X的名称为 。 ②反应结束后,经过滤、洗涤、低温烘干可获得CaO2·xH2O。检验晶体已洗涤干净的方法为:取最后一次洗涤液,滴加 ,若 ,则晶体已经洗涤干净。 (2)为确定过氧化钙晶体的组成,某化学兴趣小组查资料发现:过氧化钙晶体受热时会先失去结晶水,然后再发生分解生成氧化钙和氧气,于是他们称取21.6 克过氧化钙晶体用热分析仪对其进行热分解实验,并绘制了固体质量与温度的关系图(如上曲线图),由此计算可得x= 。 5. 化学小组用如图所示装置研究酸碱盐的性质(夹持仪器已省略)。 (1)关闭K2,打开K1和分液漏斗玻璃塞、活塞,向B装置中加入稀盐酸,使其浸没大理石后关闭分液漏斗活塞。B中发生反应的化学方程式为__ ... ...
~~ 您好,已阅读到文档的结尾了 ~~