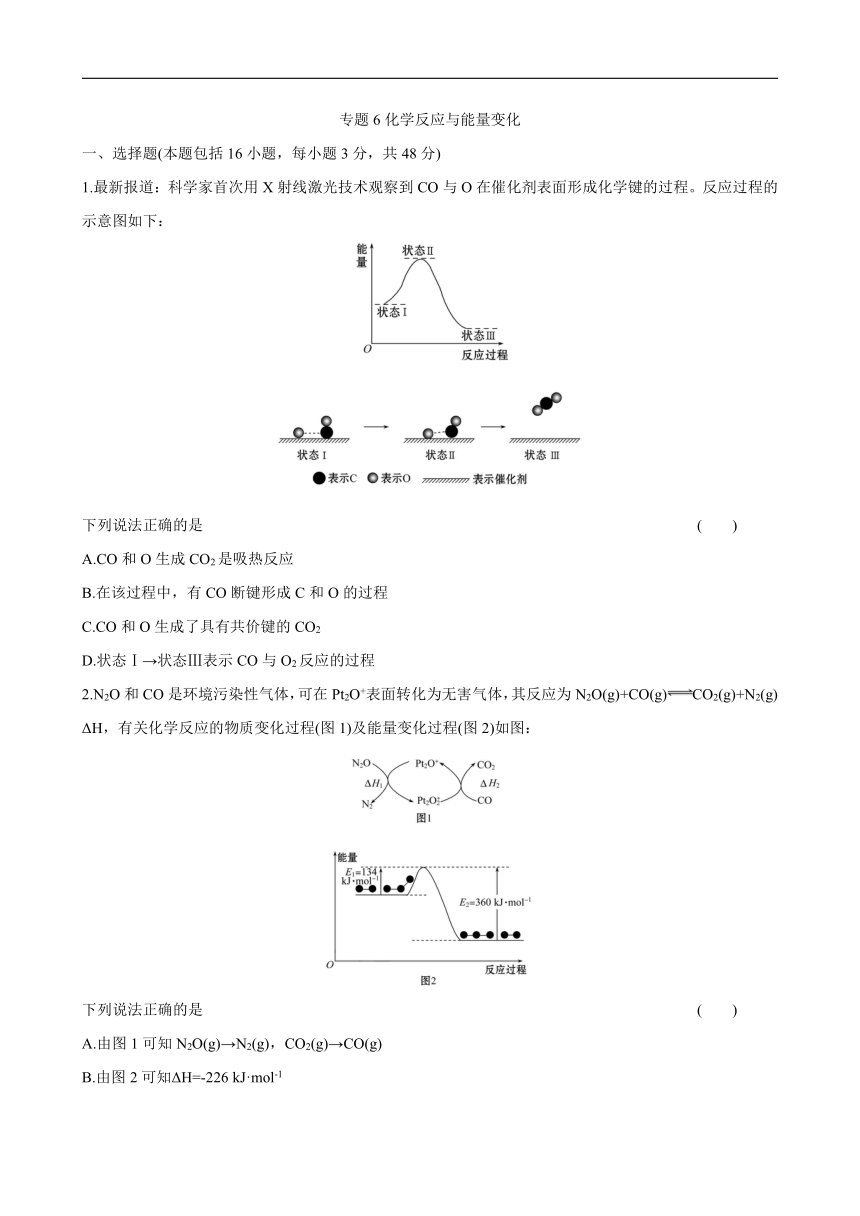
专题6化学反应与能量变化 一、选择题(本题包括16小题,每小题3分,共48分) 1.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下: 下列说法正确的是 ( ) A.CO和O生成CO2是吸热反应 B.在该过程中,有CO断键形成C和O的过程 C.CO和O生成了具有共价键的CO2 D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程 2.N2O和CO是环境污染性气体,可在Pt2O+表面转化为无害气体,其反应为N2O(g)+CO(g)CO2(g)+N2(g) ΔH,有关化学反应的物质变化过程(图1)及能量变化过程(图2)如图: 下列说法正确的是 ( ) A.由图1可知N2O(g)→N2(g),CO2(g)→CO(g) B.由图2可知ΔH=-226 kJ·mol-1 C.为了实现转化需不断向反应器中补充Pt2O+和Pt2 D.由图2可知该反应的逆反应是放热反应 3.氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是 ( ) A.氢氧燃料电池放电时化学能全部转化为电能 B.氢氧燃料电池的负极反应为O2+2H2O+4e-4OH- C.常温常压下,氢氧燃料电池放电过程中消耗11.2 L H2,转移电子的数目为6.02×1023 D.反应2H2(g)+O2(g)2H2O(g)的热量变化可以通过反应中形成新共价键的键能之和与反应中断裂旧共价键的键能之和来计算 4.我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH 的催化反应历程。该历程示意图如下。 下列说法不正确的是 ( ) A.CO2和CH4完全转化CH3COOH B.CH4→CH3COOH 过程中,有C—H 键发生断裂 C.①→②放出能量并形成了C—C键 D.升高温度可减慢该化学反应速率 5.(双选)(2020·济南高一检测)HBr被O2氧化依次由如下Ⅰ、Ⅱ、Ⅲ三步反应组成,1 mol HBr被氧化为Br2放出12.67 kJ热量,其能量与反应过程曲线如图所示。 (Ⅰ)HBr(g)+O2(g)HOOBr(g) (Ⅱ)HOOBr(g)+HBr(g)2HOBr(g) (Ⅲ)HOBr(g)+HBr(g)H2O(g)+Br2(g) 下列说法中正确的是 ( ) A.三步反应均为放热反应 B.步骤(Ⅰ)的反应速率最慢 C.步骤(Ⅰ)中HBr和O2比HOOBr稳定 D.4HBr(g)+O2(g)2H2O(g)+2Br2(g)完全反应放出 12.67 kJ 的能量 6.在反应C(s)+CO2(g)2CO(g)中,可使化学反应速率明显增大的措施是 ( ) ①增大压强 ②升高温度 ③增大CO2的浓度 ④增加炭的量 ⑤降低压强 A.①②③ B.②③④ C.①②③④ D.②③④⑤ 7.反应3X(g)+Y(g)Z(g)+2W(g)在2 L密闭容器中进行,5 min后Y减少了0.1 mol,则此反应的平均速率为 ( ) A.v(X)=0.03 mol·L-1·min-1 B.v(Y)=0.02 mol·L-1·min-1 C.v(Z)=0.10 mol·L-1·min-1 D.v(W)=0.20 mol·L-1·min-1 8.某反应的反应机理、能量与反应进程的关系如图所示,下列说法不正确的是 ( ) A.Fe2+是该反应的催化剂 B.反应的总离子方程式为S2+2I-2S+I2。 C.S2在第一步反应中作氧化剂 D.两步反应都是放热反应 9.(双选)(2020·保山高一检测)中国科学家用墨汁书写后的纸张作为空气电极,设计并组装了轻型、柔性、能折叠的可充电锂—空气电池如图甲,电池的工作原理如图乙。下列有关说法正确的是 ( ) A.放电时,纸张中的石墨作为锂电池的正极 B.开关K闭合给锂电池充电,X为直流电源的正极 C.闭合开关K给锂电池充电,X对应充电电极上的反应为Li++e-Li D.放电时,Li+由正极经过有机电解质溶液移向负极 10.下列对图a和图b的分析合理的是 ( ) A.图a负极上发生的反应是O2+4e-+2H2O4OH- B.图b接通开关后溶液中的H+向正极移动 C.图a中的铁棒发生腐蚀,正极上发生的反应可能是4OH--4e-O2↑+2H2O D.图b接通开关后铜被腐蚀 11.已知X(g)+3Y(g)2W(g)+M(g),1 mol X完全反应放出a kJ热量。一定温度下,在体积恒定的密闭容器中,加入1 mol X(g)与1 mol Y(g),下列说法正确的是 ( ) A.充分反应后,放出热量为a kJ B.当反应达到平衡状态时,X与W的物质的量浓度之比 ... ...
~~ 您好,已阅读到文档的结尾了 ~~