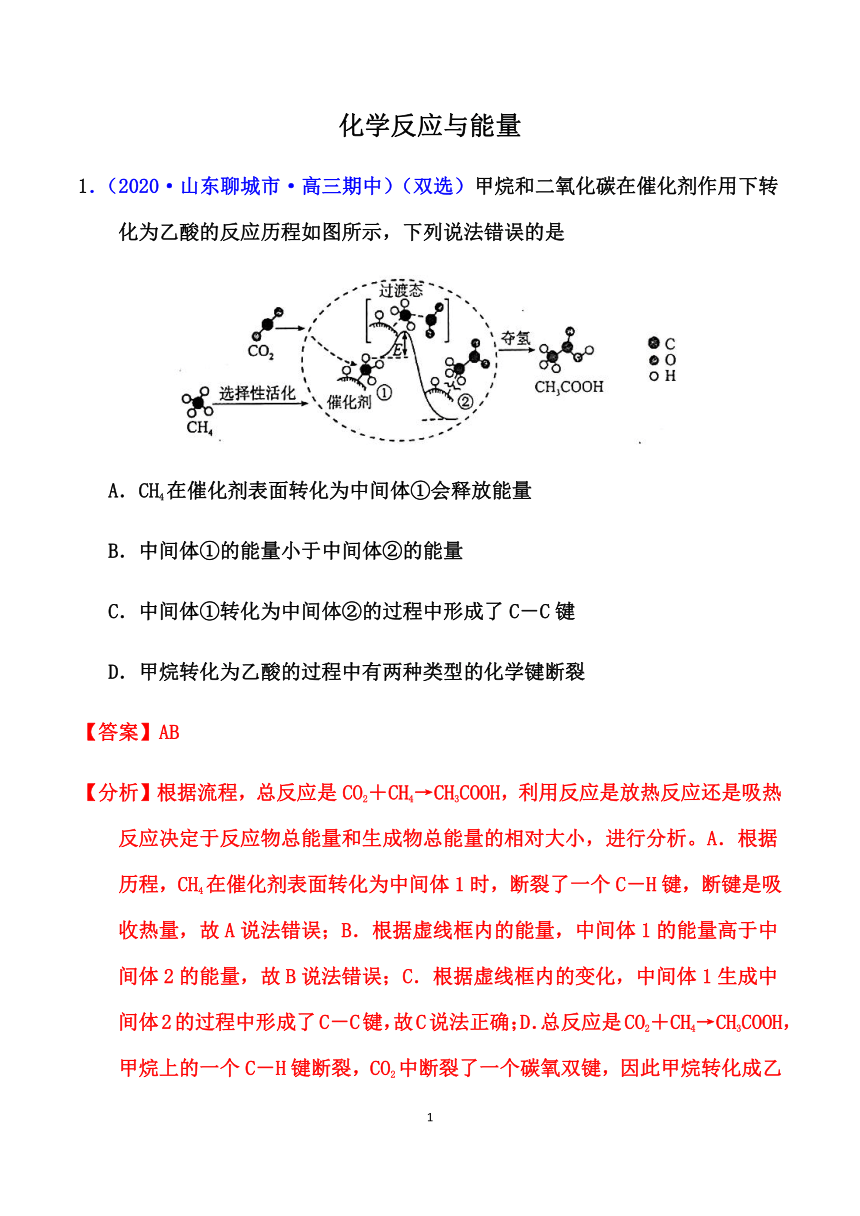
化学反应与能量 1.(2020·山东聊城市·高三期中)(双选)甲烷和二氧化碳在催化剂作用下转化为乙酸的反应历程如图所示,下列说法错误的是 A.CH4在催化剂表面转化为中间体①会释放能量 B.中间体①的能量小于中间体②的能量 C.中间体①转化为中间体②的过程中形成了C-C键 D.甲烷转化为乙酸的过程中有两种类型的化学键断裂 【答案】AB 【分析】根据流程,总反应是CO2+CH4→CH3COOH,利用反应是放热反应还是吸热反应决定于反应物总能量和生成物总能量的相对大小,进行分析。A.根据历程,CH4在催化剂表面转化为中间体1时,断裂了一个C-H键,断键是吸收热量,故A说法错误;B.根据虚线框内的能量,中间体1的能量高于中间体2的能量,故B说法错误;C.根据虚线框内的变化,中间体1生成中间体2的过程中形成了C-C键,故C说法正确;D.总反应是CO2+CH4→CH3COOH,甲烷上的一个C-H键断裂,CO2中断裂了一个碳氧双键,因此甲烷转化成乙酸的过程中有两种类型的化学键断裂,故D说法正确;答案为AB。 2.(2020·陕西榆林市·榆林十二中高三月考)(1)如图表示某反应的能量变化关系,则此反应为____(填“吸热”或“放热”)反应,其中ΔH=____(用含有A.b的关系式表示)。 (2)曾用CuCl2作催化剂,在450 ℃利用空气中的氧气跟氯化氢反应制氯气,反应的化学方程式为____。使用催化剂对反应焓变有无影响_____。 (3)NaBH4(s)与false反应生成false和false。在25℃,101kPa下,已知每消耗falsefalse放热false,该反应的热化学方程式是_____。 (4)甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、false和false)在催化剂作用下合成甲醇,发生的主要反应如下: ①false false ②false false ③false false 已知反应①中相关的化学键键能数据如下(已知CO的化学键为false): 化学键 H-H C-O false H-O C-H false 436 343 1076 465 413 计算false_____false;已知false,则false_____false。 【答案】(1)放热 (a-b) kJ·mol-1 (2)O2+4HClfalse2Cl2+2H2O 无 (3)false false (4) -99 +41 【解析】 (1)反应物的能量高于生成物,因此是放热反应。反应热为反应物断键吸收的能量与生成物成键放出的能量之差,即△H =(a-b)kJfalsemol-1,故答案为:放热;(a-b) kJ·mol-1; (2)用CuCl2作催化剂,在450 ℃利用空气中的氧气跟氯化氢反应制氯气,生成氯气和水,配平书写化学方程式为O2+4HClfalse2Cl2+2H2O。催化剂改变反应的途径,不改变始终态,则催化剂降低反应所需的活化能,但对反应热无影响。故答案为:O2+4HClfalse2Cl2+2H2O;无; (3)3.8gNaBH4的物质的量为0.1mol,在25℃,101kPa下,每消耗3.8gNaBH4(s)放热21.6kJ,则消耗1molNaBH4(s)放热216kJ,则该反应的热化学方程式是falsefalse,答案为:falsefalse; (4)反应热=反应物总键能-生成物总键能,故△H1=1076kJfalsemol-1+2false436kJfalsemol-1-(3false413+343+465)kJfalsemol-1=-99kJfalsemol-1; 反应②-反应①得反应③,根据盖斯定律△H3=△H2-△H1=-58kJfalsemol-1-(-99kJfalsemol-1)=+41kJfalsemol-1,故答案为:-99;+41。 3.(2020·重庆复旦中学高三月考)CO、SO2、NO均为大气污染物,通过下列反应可以实现可持续发展。已知: ①2CO(g)+SO2(g)=S(g)+2CO2(g) △H=+8.0 kJ?mol?1 ②2H2(g)+SO2(g)=S(g)+2H2O(g) △H=+90.4 kJ?mol?1 ③2NO(g)+2CO(g)=N2(g)+2CO2(g) △H=-746.5kJ?mol?1 请回答: (1)反应①属于___(填“吸热”或“放热”)反应。 (2)反应②生成0.5molS(g)时,△H=___kJ?mol?1。 (3)反应③消耗30gNO(g)时,△H=___kJ?mol?1。 (4)反应CO(g)+H2O(g)=CO2(g)+H2(g),△H=___kJ?mol?1。 (5)已知乙醇燃烧热是1366.8 kJ?mol?1,写 ... ...
~~ 您好,已阅读到文档的结尾了 ~~

