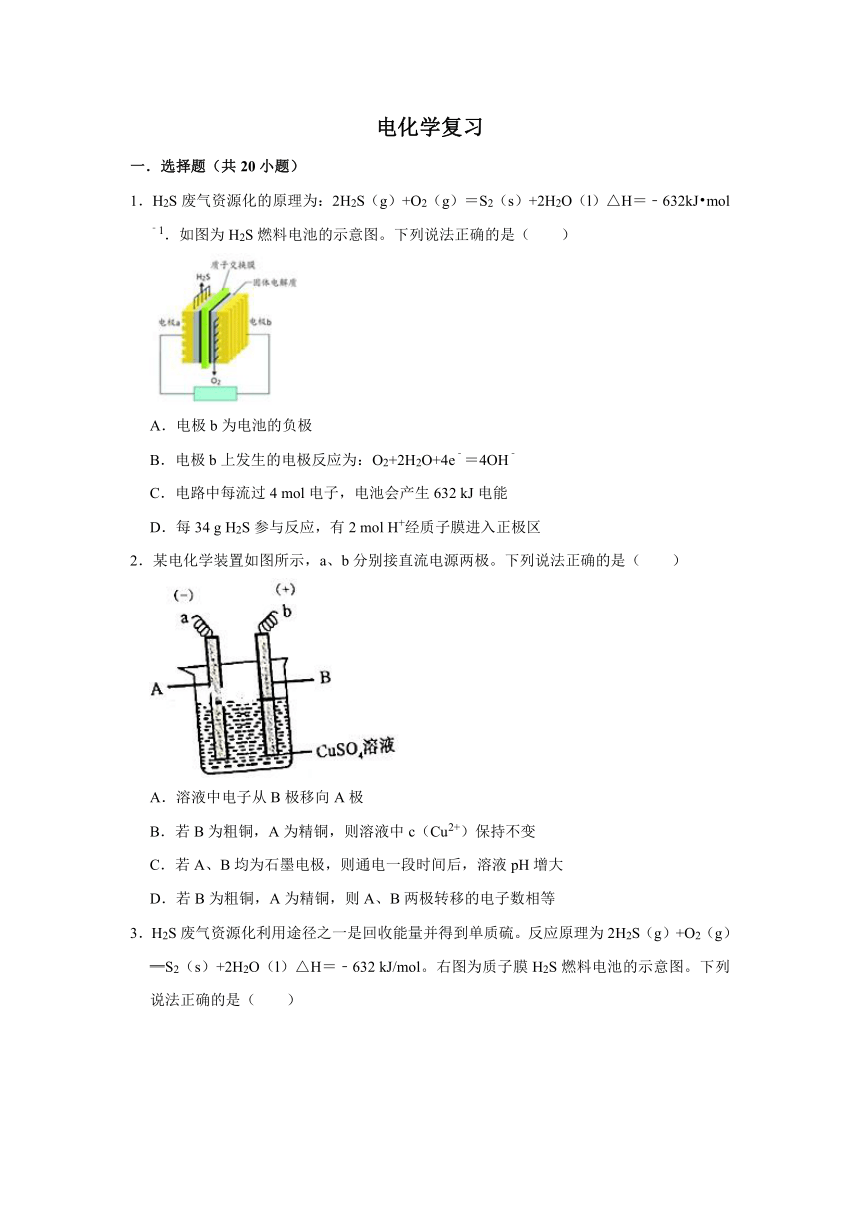
电化学复习 一.选择题(共20小题) 1.H2S废气资源化的原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=﹣632kJ?mol﹣1.如图为H2S燃料电池的示意图。下列说法正确的是( ) A.电极b为电池的负极 B.电极b上发生的电极反应为:O2+2H2O+4e﹣=4OH﹣ C.电路中每流过4 mol电子,电池会产生632 kJ电能 D.每34 g H2S参与反应,有2 mol H+经质子膜进入正极区 2.某电化学装置如图所示,a、b分别接直流电源两极。下列说法正确的是( ) A.溶液中电子从B极移向A极 B.若B为粗铜,A为精铜,则溶液中c(Cu2+)保持不变 C.若A、B均为石墨电极,则通电一段时间后,溶液pH增大 D.若B为粗铜,A为精铜,则A、B两极转移的电子数相等 3.H2S废气资源化利用途径之一是回收能量并得到单质硫。反应原理为2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=﹣632 kJ/mol。右图为质子膜H2S燃料电池的示意图。下列说法正确的是( ) A.电极a为电池的正极 B.电极b上发生的电极反应为:O2+4H++4e﹣=2H2O C.电路中每流过4mol电子,电池会产生632kJ热能 D.22.4LH2S参与反应时,2molH+经质子交换膜进入正极区 4.下列关于如图所示装置的说法,正确的是( ) A.①装置中阴极处产生的气体能够使湿润KI淀粉试纸变蓝 B.②装置中待镀铁制品应与电源正极相连 C.③装置中电子由b极流向a极 D.④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 5.某课题组以纳米Fe2O3、金属钾和碳的复合材料(碳作为金属锂的载体)作为两极的电极材料制备锂离子电池(电解质为一种能传导Li+的高分子材料),通过在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控。如图,下列说法不正确的是( ) A.该电池不可以用NaOH溶液作为电解质溶液 B.放电时电池正极的电极反应式为Fe2O3+6e﹣=3O2﹣+2Fe C.放电时电池的总反应为Fe2O3+6Li=3Li2O+2Fe D.在放电过程中,通过电极材料Fe2O3转化为Fe,实现对磁铁的吸引 6.关于下列装置的说法,正确的是( ) A.装置①中盐桥内K+的移向ZnSO4溶液 B.装置①将电能转变为化学能 C.若装置②用于铁棒镀铜,则N极为铜棒,电镀过程中溶液中的浓度基本保持不变 D.若装置②用于电解精炼铜,精炼过程溶液中Cu2+的浓度基本保持不变 7.钠离子电池开始成为下一轮电池研究的重点,下图是一种可充电钠离子电池(电解质溶液Na2SO3溶液)工作示意图。下列说法正确的是( ) A.电池放电时,Na+从a极区移动到b极区 B.电池放电时,b极区发生的反应是Na2NiFeⅡ(CN)6═NaNiFeⅢ(CN)6+e﹣+Na+ C.金属钠可以作为该电池的负极材料 D.离子交换膜也可以改成阴离子交换膜 8.一种碳纳米管能够吸附氢气,用这种材料制备的电池其原理如图所示,该电池的电解质为6 mol?L﹣1KOH溶液。下列说法中不正确的是( ) A.放电时电池负极的电极反应为H2﹣2e﹣+2OH﹣═2H2O B.放电时K+移向正极 C.放电时镍电极的电极反应为Ni(OH)2+OH﹣﹣e﹣═NiO(OH)+H2O D.该反应过程中KOH溶液的浓度基本保持不变 9.锂离子电池已经成为应用最广泛的可充电电池。某种锂离子电池的结构示意图如图所示,其中两极区间的隔膜只允许Li+通过。电池放电时的总反应方程式为:Li2CoO2+xLi=LiCoO2.关于该电池的推论错误的是( ) A.放电时,Li+主要从负极区通过隔膜移向正板区 B.放电时,负极反应为:xLi﹣xe﹣=xLi+ C.为增强溶液的导电性,使用硫酸为电解质溶液 D.充电时,负极(C)上锂元素被还原 10.有一种银锌电池,其电极分别为Ag2O和Zn,电解质溶液为NaOH,其中Ag2O极电极反应式为Ag2O+H2O+2e﹣═2Ag+2OH﹣,根据上述反应式,下列说法正确的是( ) A.使用过程中,电子由Ag2O极经外路流向Zn极 B.使用 ... ...
~~ 您好,已阅读到文档的结尾了 ~~