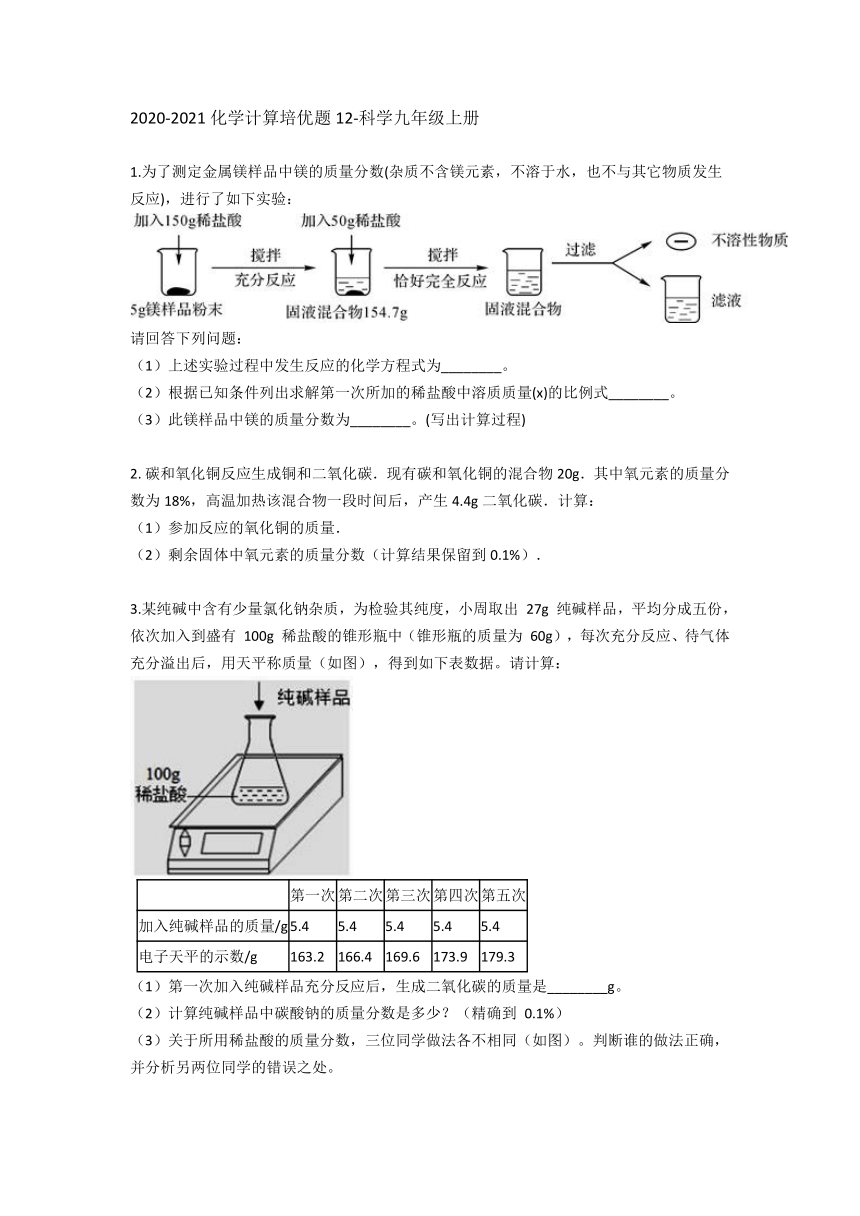
2020-2021化学计算培优题12-科学九年级上册 1.为了测定金属镁样品中镁的质量分数(杂质不含镁元素,不溶于水,也不与其它物质发生反应),进行了如下实验: 请回答下列问题: (1)上述实验过程中发生反应的化学方程式为_____。 (2)根据已知条件列出求解第一次所加的稀盐酸中溶质质量(x)的比例式_____。 (3)此镁样品中镁的质量分数为_____。(写出计算过程) 2.?碳和氧化铜反应生成铜和二氧化碳.现有碳和氧化铜的混合物20g.其中氧元素的质量分数为18%,高温加热该混合物一段时间后,产生4.4g二氧化碳.计算: (1)参加反应的氧化铜的质量. (2)剩余固体中氧元素的质量分数(计算结果保留到0.1%). 3.某纯碱中含有少量氯化钠杂质,为检验其纯度,小周取出 27g 纯碱样品,平均分成五份,依次加入到盛有 100g 稀盐酸的锥形瓶中(锥形瓶的质量为 60g),每次充分反应、待气体充分溢出后,用天平称质量(如图),得到如下表数据。请计算: 第一次 第二次 第三次 第四次 第五次 加入纯碱样品的质量/g 5.4 5.4 5.4 5.4 5.4 电子天平的示数/g 163.2 166.4 169.6 173.9 179.3 (1)第一次加入纯碱样品充分反应后,生成二氧化碳的质量是_____g。 (2)计算纯碱样品中碳酸钠的质量分数是多少?(精确到 0.1%) (3)关于所用稀盐酸的质量分数,三位同学做法各不相同(如图)。判断谁的做法正确,并分析另两位同学的错误之处。 芳芳的解法: 明 明的解法: 秀秀的解法: 4.实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na2CO3的质量分数,小明进行了如下实验。 ①取质量、大小相同的3个烧杯,分别加入一定质量分数的稀盐酸100克; ②向上述3个烧杯中分别加入3份质量不同的样品; ③充分反应后,再用电子天平称量烧杯及烧杯内物质的总质量(假设产生的气体完全逸出)。 实验数据记录如下: 实验一 实验二 实验三 反应前稀盐酸+烧杯质量(克) 150 150 150 反应前固体样品质量(克) 4 8 12 反应后烧杯内物质+烧杯质量(克) m 155.8 158.7 已知实验中发生的化学反应: NaOH+HCl=NaCl+H2O;Na2CO3+2HCl=2NaCl+H2O+CO2↑ (1)表中的m值为_____。 (2)根据实验二的数据计算样品中Na2CO3的质量分数。 5.取氯酸钾和二氧化锰的混合物13g,加热至混合物固体质量不再减少为止,冷却后称得剩余固体质量为8.2g,将剩余固体加入一定量的水中,充分搅拌后过滤,滤液是10%的氯化钾溶液(假设溶液无损失),计算: (1)生成氧气的质量? (2)参加反应的氯酸钾的质量?(写出计算过程) (3)氯化钾溶液的质量?(写出计算过程) 6.小明想测定部分变质的熟石灰样品中Ca(OH)2的质量分数,他称取 0.5g该样品,加足量水使之充分溶解,搅拌过滤后,在滤液中加入10%盐酸溶液,加入盐酸溶液的质量和溶液的pH见表。 加入盐酸溶液的质量/g 0 2.5 3.65 6 溶液的pH 12 11 7 2 (1)当pH=2时,溶液中所含的溶质是_____(写化学式)。 (2)求样品中Ca(OH)2的质量分数。(写出计算过程) 7.小科同学为了测定黄铜屑(由锌和铜制形成的合金)样品组成,取四份样品分别加和硫酸反应,其实验数据记录如下表。 样品 第1 份 第2份 第3份 第4份 取样品质量(g) 40.0 40.0 40.0 40.0 取稀硫酸质量(g) 40.0 80.0 120.0 160.0 产生气体质量(g) 0.3 0.6 0.8 0.8 试计算: (1)经分析,在第_____份样品测得的数据中,锌完全反应了。 (2)列式计算黄铜屑样品中的锌的质量分数和所用稀硫酸中溶质的质量分数。 (3)请在图中画出在60.0g样品中加稀硫酸的质量与产生气体质量变化关系的示意图。 8.?如图是某胃药标签的部分内容.小明同学测定该药品中NaHCO3含量的过程如下:取10粒该药剂研碎后放入烧杯中,加入50克水后充分搅拌,再向其中滴 ... ...
~~ 您好,已阅读到文档的结尾了 ~~

