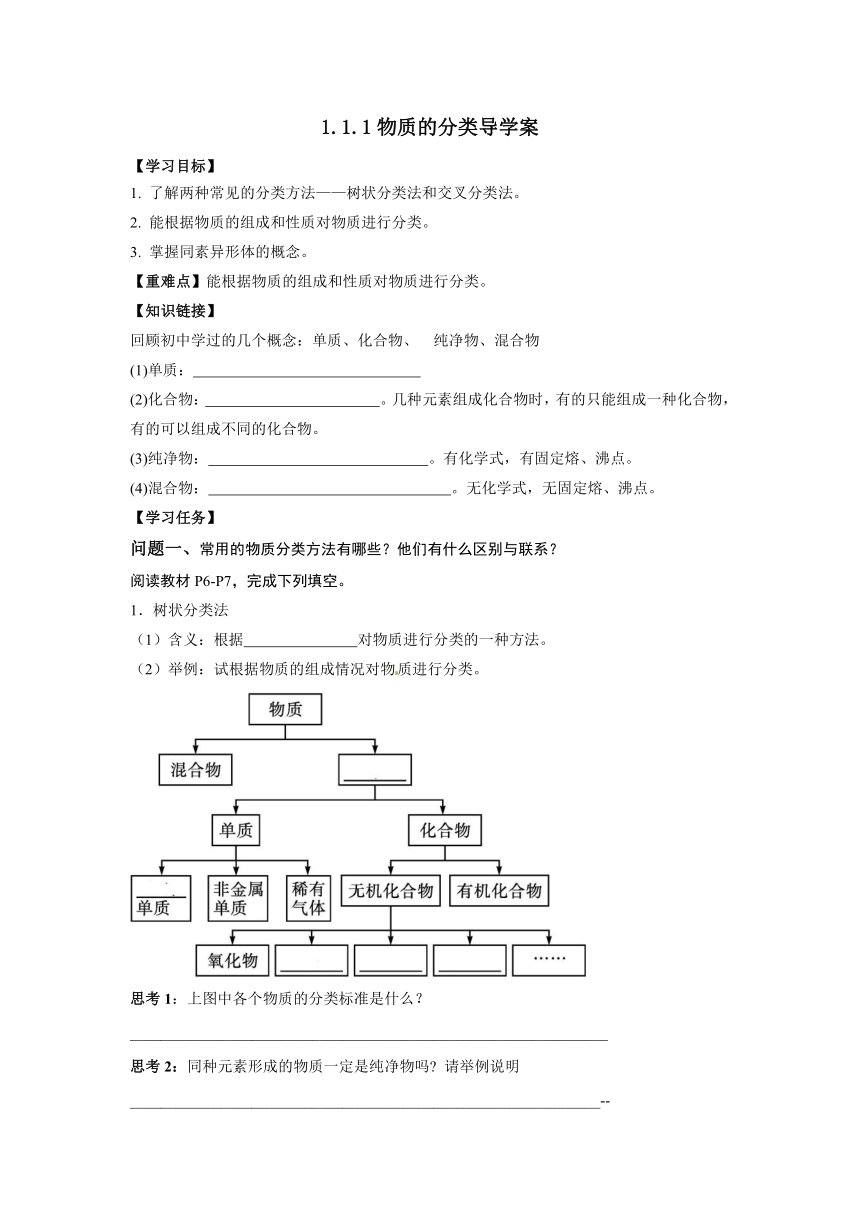
1.1.1物质的分类导学案 【学习目标】 了解两种常见的分类方法———树状分类法和交叉分类法。 能根据物质的组成和性质对物质进行分类。 掌握同素异形体的概念。 【重难点】能根据物质的组成和性质对物质进行分类。 【知识链接】 回顾初中学过的几个概念:单质、化合物、 纯净物、混合物 (1)单质: (2)化合物: 。几种元素组成化合物时,有的只能组成一种化合物,有的可以组成不同的化合物。 (3)纯净物: 。有化学式,有固定熔、沸点。 (4)混合物: 。无化学式,无固定熔、沸点。 【学习任务】 问题一、常用的物质分类方法有哪些?他们有什么区别与联系? 阅读教材P6-P7,完成下列填空。 1.树状分类法 (1)含义:根据 对物质进行分类的一种方法。 (2)举例:试根据物质的组成情况对物质进行分类。 思考1:上图中各个物质的分类标准是什么? _____ 思考2:同种元素形成的物质一定是纯净物吗 请举例说明 _____-- 【重要概念】 同素异形体: 。 如:碳元素常见的同素异性体: 氧元素的同素异形体: 磷元素的同素异形体:白磷(P4)、红磷(P) 2.交叉分类法 (1)含义:根据不同的分类标准,对同一事物进行多种分类的一种分类方法 (2)举例:试从不同的角度对下列各组物质进行分类,将其类别名称分别填在相应的空格内。 问题二、什么叫酸、碱、盐和氧化物? ( 两性氧化物 不成盐氧化物 )根据组成和性质对酸、碱、盐和氧化物进行再分类(★★★) ( )氧化物 根据组成元素分 根据性质分 ①酸性氧化物:能与碱反应只生成 的氧化物。 ②碱性氧化物:能与酸反应只生成 的氧化物。 思考1:非金属氧化物一定是酸性氧化物吗?金属氧化物一定是碱性氧化物吗? ( 【知识点总结】 碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物 。 如 Mn 2 O 7 、 CrO 3 为酸性氧化物, Al 2 O 3 为两性氧化物, Na 2 O 2 为过氧化物。 ② 酸性氧化物不一定是非金属氧化物,非金属氧化物也不一定是酸性氧化物 。 如: Mn 2 O 7 、 CrO 3 是酸性氧化物, CO 、 NO 都是不成盐氧化物。 酸性氧化物、碱性氧化物不一定都能与水反应 。 如 SiO 2 、 Fe 2 O 3 都不与水反应。 )_____ 酸: 阳离子全部是氢离子(H+)的化合物 (1)按是否含氧分为: (如H2SO4、HNO3 H3PO4)和 (如HCl 、H2S) (2)按酸性强弱分为: (如HCl、H2SO4、HNO3)和 (如H3PO4、H2CO3) (3)按电离产生的氢离子数目分为: (如HNO3、HCl )、 (如H2SO4 、H2S)和 (如H3PO4) 碱:阴离子全部是氢氧根离子( OH- )的化合物 (1)按碱性强弱分为: (如NaOH KOH Ba(OH)2 Ca(OH)2)和 (如Cu(OH)2 Fe(OH)3 NH3·H2O) (2)按电离产生的氢氧根离子数目分为: (如NaOH KOH NH3·H2O )、 (如Ba(OH)2 Fe(OH) 2)和 (如Fe(OH)3) (3)按溶解性分为: (如NaOH KOH Ba(OH)2 )、 (如Cu(OH)2 Fe(OH)3)和 (如Ca(OH)2) 盐:由金属阳离子(或NH4+)和酸根离子构成的化合物 (1)按溶解性分为: (如NaCl、AgNO3、CuSO4、NH4Cl)和 (如CaCO3、 BaCO3 、BaSO4) (2)按组成离子分为:钠盐、钾盐、硫酸盐、硝酸盐、铵盐等等 (3)按组成分为: (如NaCl、NH4Cl、BaSO4)、 (如NaHSO4、 NaHSO3)和 (如碱式碳酸铜Cu2(OH)2CO3) 【重要概念】 正盐:酸跟碱完全中和生成的盐,不会有酸中的H+,也不会有碱中的OH- 酸式盐:在水溶液中能电离出H+的盐 碱式盐:在电离时生成的阴离子除了酸根离子外还有OH-的盐 课堂达标练 1.下列各组属于同素异形体的是( ) A. 16O和18O B. O2和O3 C. S2-和S D. H2O和H2S 2.某气体经过检验只含有一种元素,则该气体是( ) A.一种单质 B.一种化合物 C.单质与化合物的混合物 D.可能是一种单质,也可能是几种单质的混合物 3.将下列各组物质 ... ...
~~ 您好,已阅读到文档的结尾了 ~~