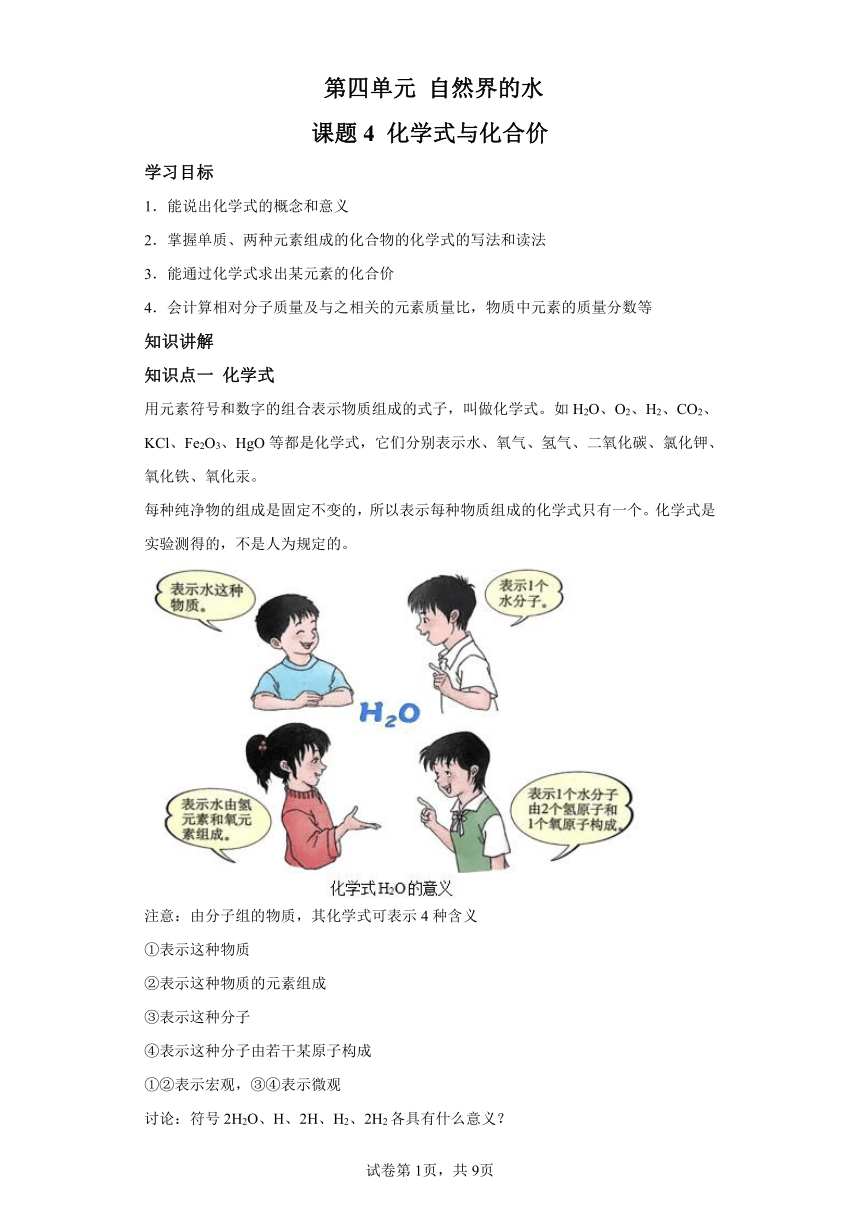
第四单元 自然界的水 课题4 化学式与化合价 学习目标 1.能说出化学式的概念和意义 2.掌握单质、两种元素组成的化合物的化学式的写法和读法 3.能通过化学式求出某元素的化合价 4.会计算相对分子质量及与之相关的元素质量比,物质中元素的质量分数等 知识讲解 知识点一 化学式 用元素符号和数字的组合表示物质组成的式子,叫做化学式。如H2O、O2、H2、CO2、KCl、Fe2O3、HgO等都是化学式,它们分别表示水、氧气、氢气、二氧化碳、氯化钾、氧化铁、氧化汞。 每种纯净物的组成是固定不变的,所以表示每种物质组成的化学式只有一个。化学式是实验测得的,不是人为规定的。 注意:由分子组的物质,其化学式可表示4种含义 ①表示这种物质 ②表示这种物质的元素组成 ③表示这种分子 ④表示这种分子由若干某原子构成 ①②表示宏观,③④表示微观 讨论:符号2H2O、H、2H、H2、2H2各具有什么意义? 总结:元素符号或化学式前有数字或字母,则只表示微观含义,如aFe表示a个铁原子,3O2表示3个氧分子。 书写化学式的注意事项: ①当某组成元素原子个数比是1时,1可省略; ②氧化物化学式的书写,一般吧氧的元素符号写在右方,另一种元素的符号写在左方,如CO2; ③由金属元素与非金属元素组成的化合物,书写其化学式时,一般把金属元素符号写在左方,非金属元素符号写在右方,如NaCl。 由两种元素组成的化合物的名称,一般读作某化某,例如,NaCl读作氯化钠。有时还要读出化学式中各元素的原子个数,例如CO2读作二氧化碳,Fe3O4读作四氧化三铁。 知识点二 化合价 化合物有固定的组成,即形成化合物的元素有固定的原子个数比,如HCl为1:1,H2O为2:1,我们如何确定原子的个数比呢? 一般我们可以通过“化合价”来认识其中的规律,化合价有正有负,在化合物里正、负化合价的代数和为零。如,在化合物里O通常为-2价,H通常为+1价,Cl通常为-1价,当氢气与氧气反应时,2个氢原子与1个氧原子结合成H2O;当氢气与氯气反应时,1个氢原子与1个氯原子结合成HCl。 有些物质如Ca(OH)2、CaCO3等,它们中的一些带电的原子团,如、常作为一个整体参加反应,这样的原子团,又叫做根。根也有化合价,中学化学常见的根有、、、、。 常见元素化合价口诀:一价氢氯钾钠银,其中氯为-1,其余为+1 二价氧钙钡镁锌,其中氧为-2,其余为+2 三铝,四硅,五价磷 二三铁,二四碳 二四六硫都齐全,硫为-2、+4、+6 铜汞二价最常见 莫忘单质都为零,单质的化合价都是0价 在确定元素的化合价时,需要注意以下几点: 1.金属元素与非金属化合时,金属元素显正价,非金属元素显负价 2.一些元素在不同物质中可显示不同的化合价 思考:化合价表示原子之间相互化合时原子得失电子的数目,那么化合价与元素原子的最外层电子数有什么关系呢?离子中的某元素的化合价怎么计算? 知道了元素的化合价,可以根据“化合中正负化合价代数和为零”求出元素原子的个数比,从而写出化合物的化学式。 知识点三 有关相对分子质量的计算 化学式中各原子的相对原子质量的总和,就是相对分子质量(符号为Mr)。根据化学式可进行以下各种计算。 1.计算相对分子质量 如,H2O的相对分子质量=1×2+16=18 2.计算物质组成元素的质量比 如,二氧化碳(CO2)中碳元素和氧元素的质量比等于12:(16×2)=3:8 3.计算物质中某元素的质量分数 物质中某元素的质量分数,就是该元素的质量与组成物质的元素总质量之比。如,计算硝酸铵(NH4NO3)中氮元素的质量分数,可先根据化学式计算出NH4NO3的相对分子质量: NH4NO3的相对分子质量=14+1×4+14+16×3=80 再计算氮元素的质量分数: 注意:药品、食品等商品的标签或说明书上常常用质量分数来表示物质的成分或纯度。 考法一:化学式的意义、读法、写法(详 ... ...
~~ 您好,已阅读到文档的结尾了 ~~