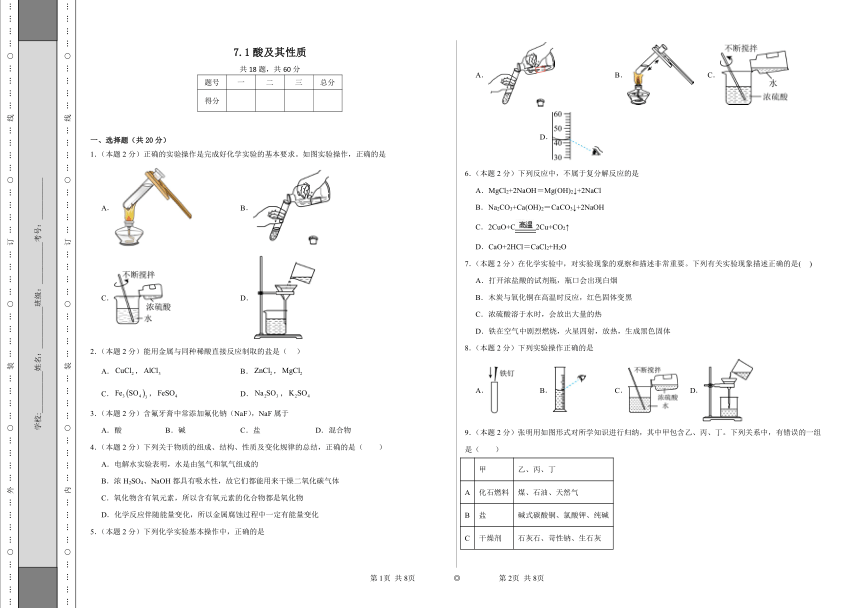
7.1酸及其性质 共18题,共60分 题号 一 二 三 总分 得分 一、选择题(共20分) 1.(本题2分)正确的实验操作是完成好化学实验的基本要求。如图实验操作,正确的是 A. B. C. D. 2.(本题2分)能用金属与同种稀酸直接反应制取的盐是( ) A., B., C., D., 3.(本题2分)含氟牙膏中常添加氟化钠(NaF),NaF属于 A.酸 B.碱 C.盐 D.混合物 4.(本题2分)下列关于物质的组成、结构、性质及变化规律的总结,正确的是( ) A.电解水实验表明,水是由氢气和氧气组成的 B.浓H2SO4、NaOH都具有吸水性,故它们都能用来干燥二氧化碳气体 C.氧化物含有氧元素,所以含有氧元素的化合物都是氧化物 D.化学反应伴随能量变化,所以金属腐蚀过程中一定有能量变化 5.(本题2分)下列化学实验基本操作中,正确的是 A. B. C. D. 6.(本题2分)下列反应中,不属于复分解反应的是 A.MgCl2+2NaOH=Mg(OH)2↓+2NaCl B.Na2CO3+Ca(OH)2=CaCO3↓+2NaOH C.2CuO+C2Cu+CO2↑ D.CaO+2HCl=CaCl2+H2O 7.(本题2分)在化学实验中,对实验现象的观察和描述非常重要。下列有关实验现象描述正确的是( ) A.打开浓盐酸的试剂瓶,瓶口会出现白烟 B.木炭与氧化铜在高温时反应,红色固体变黑 C.浓硫酸溶于水时,会放出大量的热 D.铁在空气中剧烈燃烧,火星四射,放热,生成黑色固体 8.(本题2分)下列实验操作正确的是 A. B. C. D. 9.(本题2分)张明用如图形式对所学知识进行归纳,其中甲包含乙、丙、丁。下列关系中,有错误的一组是( ) 甲 乙、丙、丁 A 化石燃料 煤、石油、天然气 B 盐 碱式碳酸铜、氯酸钾、纯碱 C 干燥剂 石灰石、苛性钠、生石灰 D 溶液 碘酒、糖水、生理盐水 A.A B.B C.C D.D 10.(本题2分)下列物质中属于酸的是 A.H2CO3 B.NaHCO3 C.P2O5 D.Ba(OH)2 二、判断题(共10分) 11.(本题2分)复分解反应中元素的化合价不变。( ) 12.(本题2分)浓硫酸使白纸变黑,是由于浓硫酸具有吸水性( ) 13.(本题2分)将水滴入稀硫酸中会出现液体沸腾,液滴飞溅的现象( ) 14.(本题2分)稀释浓硫酸时玻璃棒的主要作用是搅拌,加速散热( ) 15.(本题2分)打开浓盐酸试剂瓶瓶塞,瓶口冒白烟( ) 三、综合应用题(共30分) 16.(本题10分)银白色的镁条表面常有一层灰黑色的“外衣”,某小组同学进行了如下探究。已知镁条变黑是因为生成了碱式碳酸镁【】。 (1)根据碱式碳酸镁含有H元素,推测镁条变黑与空气中的 有关。 (2)为确认镁条变黑是否与O2有关,乙同学设计了如下实验 同学们讨论得出:只要完成实验 (选填序)就可达到探究目的。 同学们继续探究碱式碳酸镁【 】的化学式,已知碱式碳酸镁受热分解生成三种氧化物,称量1.42g碱式碳酸镁进行如下实验(假设每步吸收均完全)。 部分实验步骤如下: Ⅰ.打开弹簧夹K,通入一段时间的空气; Ⅱ.关闭弹簧夹K,给碱式碳酸镁加热; Ⅲ.当样品完全反应,停止加热,继续通空气直到玻璃管冷却; Ⅳ.称量C装置增重0.18g,D装置增重0.44g。 (3)装置C中盛放的试剂是 。 (4)实验过程中,当关闭K后,加热B装置,判断碱式碳酸镁完全分解的方法 ,证明其已完全分解。 (5)通过计算确定该碱式碳酸镁中x:y的最简整数比= 。 (6)若没有A装置,则测定得到的x:y的比值 (填“偏大”、“偏小”、“无影响”)。 (7)工业上碱式碳酸镁可作阻燃剂,其可能的原因是 (选填序号)。 a.分解时吸热,降低可燃物的着火点 b.生成的固体覆盖燃烧物,隔绝氧气 c.生成的气体稀释了可燃物周围的氧气浓度 17.(本题10分)探究从身边的物质开始 过氧化氢,是一种无机化合物,化学式为H2O2。纯过氧化氢是淡蓝色的黏稠液体,可任意比例与水混溶,是一种强氧化剂,水溶液俗称双氧水,为 ... ...
~~ 您好,已阅读到文档的结尾了 ~~