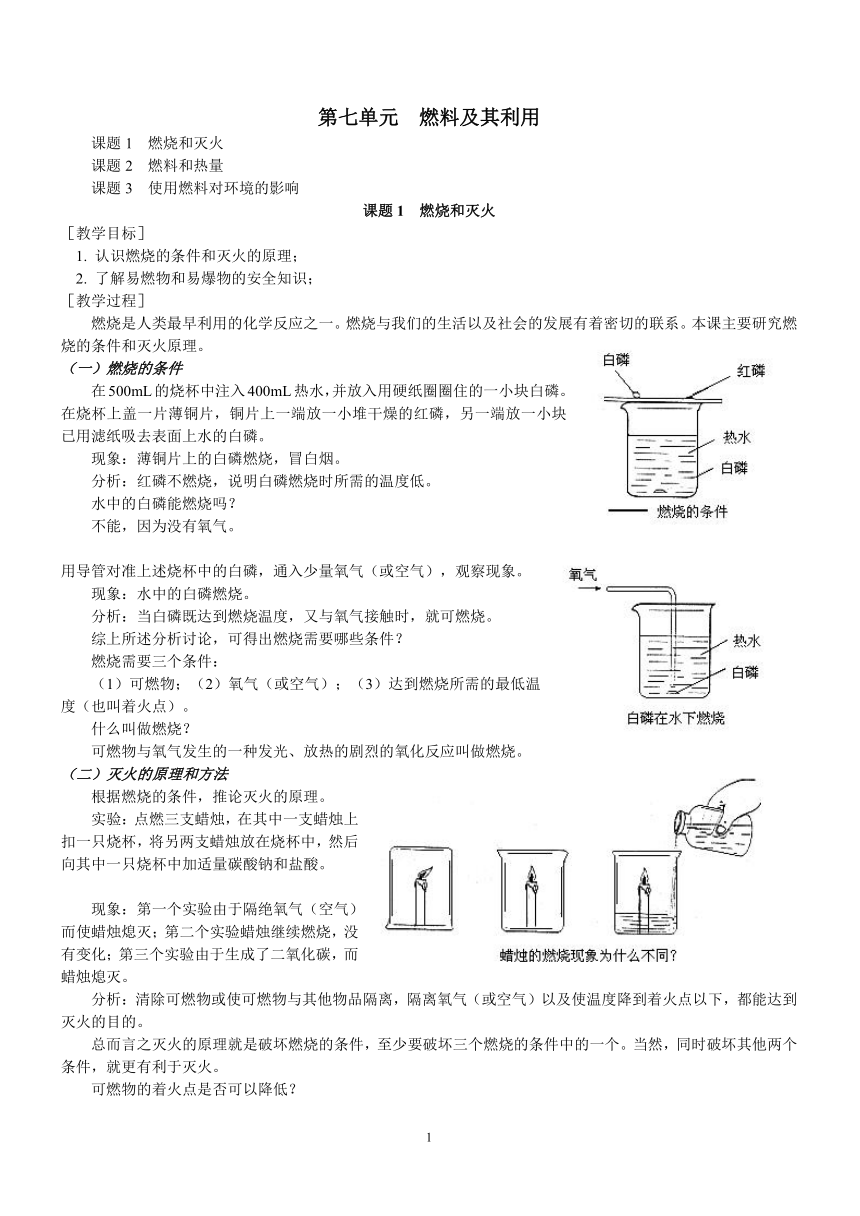
第七单元 燃料及其利用 课题1 燃烧和灭火 课题2 燃料和热量 课题3 使用燃料对环境的影响 课题1 燃烧和灭火 [教学目标] 1. 认识燃烧的条件和灭火的原理; 2. 了解易燃物和易爆物的安全知识; [教学过程] 燃烧是人类最早利用的化学反应之一。燃烧与我们的生活以及社会的发展有着密切的联系。本课主要研究燃烧的条件和灭火原理。 (一)燃烧的条件 在500mL的烧杯中注入400mL热水,并放入用硬纸圈圈住的一小块白磷。在烧杯上盖一片薄铜片,铜片上一端放一小堆干燥的红磷,另一端放一小块已用滤纸吸去表面上水的白磷。 现象:薄铜片上的白磷燃烧,冒白烟。 分析:红磷不燃烧,说明白磷燃烧时所需的温度低。 水中的白磷能燃烧吗? 不能,因为没有氧气。 用导管对准上述烧杯中的白磷,通入少量氧气(或空气),观察现象。 现象:水中的白磷燃烧。 分析:当白磷既达到燃烧温度,又与氧气接触时,就可燃烧。 综上所述分析讨论,可得出燃烧需要哪些条件? 燃烧需要三个条件: (1)可燃物;(2)氧气(或空气);(3)达到燃烧所需的最低温度(也叫着火点)。 什么叫做燃烧? 可燃物与氧气发生的一种发光、放热的剧烈的氧化反应叫做燃烧。 (二)灭火的原理和方法 根据燃烧的条件,推论灭火的原理。 实验:点燃三支蜡烛,在其中一支蜡烛上扣一只烧杯,将另两支蜡烛放在烧杯中,然后向其中一只烧杯中加适量碳酸钠和盐酸。 现象:第一个实验由于隔绝氧气(空气)而使蜡烛熄灭;第二个实验蜡烛继续燃烧,没有变化;第三个实验由于生成了二氧化碳,而蜡烛熄灭。 分析:清除可燃物或使可燃物与其他物品隔离,隔离氧气(或空气)以及使温度降到着火点以下,都能达到灭火的目的。 总而言之灭火的原理就是破坏燃烧的条件,至少要破坏三个燃烧的条件中的一个。当然,同时破坏其他两个条件,就更有利于灭火。 可燃物的着火点是否可以降低? 不可以。因为着火点是可燃物燃烧时所需的最低温度,不可以改变。 下面我们列举一些生活中灭火的实例,分析其灭火的原理。 (1)炒菜时油锅中的油不慎着火,可用锅盖盖灭。 原理:隔绝氧气(空气) (2)堆放杂质的纸箱着火时,可用水扑灭。 原理:隔绝空气,降低温度。 (3)扑灭森林火灾的有效方法之一是:将大火蔓延线路前的一片树木砍掉。 原理:隔离可燃物。 (4)酒精在桌上燃烧,用湿沫布盖灭。 原理:隔绝空气,使可燃物的温度低于着火点。 (5)将沙土铺在燃烧的化学药品上。 原理:隔绝空气。 (三)易燃物和易爆物的安全知识 1. 什么是爆炸现象呢? 可燃物在有限的空间内,急剧地燃烧,短时间内聚积大量的热,使气体的体积迅速膨胀,而引起爆炸。 2. 可能发生爆炸的物质:可燃性气体、粉尘。(面粉、煤粉) 实验:金属罐和小塑料瓶的底侧各打一个比橡皮管外径略小的小孔。连接好装置,在小塑料瓶中放入面粉,点燃蜡烛,用塑料盖盖住罐(如图I、II所示)。从橡皮管一端鼓入大量的空气(人距离该装置远一些),使面粉充满罐,观察现象并分析原因。 现象:面粉被空气鼓起成粉尘,充满金属罐,面粉尘被点燃的烛焰点燃,发生爆炸,塑料盖被弹起。 分析:可燃物与氧气接触面积越大,燃烧就愈剧烈。所以油库、面粉加工厂、纺织厂、矿井等地方的空气中常混有可燃性的气体或粉尘,它们接触到明火,就有发生爆炸的危险。 3. 在生产、运输、使用和贮存易燃物和易爆物时,必须严格遵守有关规定,绝不允许违章操作。 课题2 燃料和热量 [教学目标] 1. 了解几种化石燃料的主要成分。合理开采和节约使用化石燃料的重要性。 2. 了解化学反应中的能量变化。 [教学过程] 许多物质都能发生燃烧反应,从最早使用的柴草、到煤、石油和天然气发展至今的许多新型燃料,燃料的燃烧在人类社会的发展过程中起着相当重 ... ...
~~ 您好,已阅读到文档的结尾了 ~~