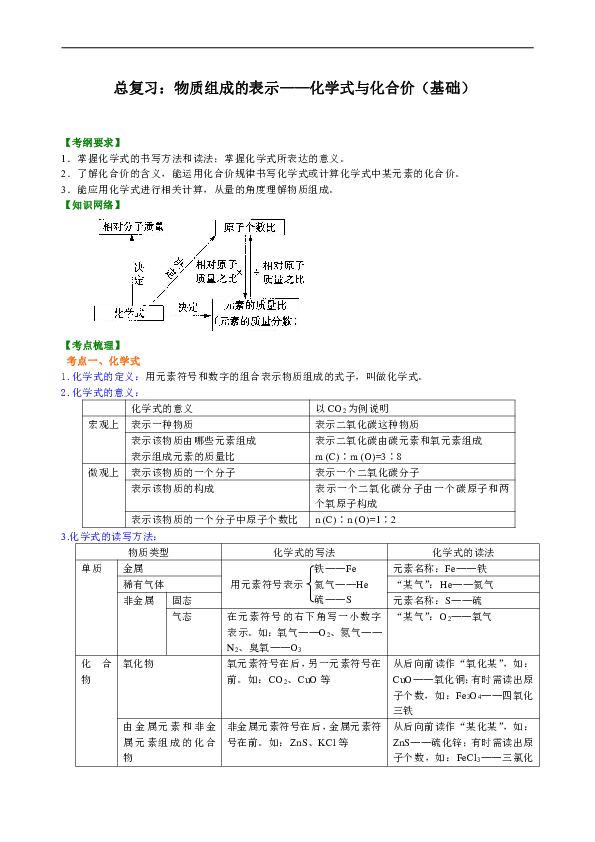
总复习:物质组成的表示———化学式与化合价(基础) 【考纲要求】 1.掌握化学式的书写方法和读法;掌握化学式所表达的意义。 2.了解化合价的含义,能运用化合价规律书写化学式或计算化学式中某元素的化合价。 3.能应用化学式进行相关计算,从量的角度理解物质组成。 【知识网络】 / 【考点梳理】 考点一、化学式 1.化学式的定义:用元素符号和数字的组合表示物质组成的式子,叫做化学式。 2.化学式的意义: 化学式的意义 以CO2为例说明 宏观上 表示一种物质 表示二氧化碳这种物质 表示该物质由哪些元素组成 表示组成元素的质量比 表示二氧化碳由碳元素和氧元素组成 m (C)∶m (O)=3∶8 微观上 表示该物质的一个分子 表示一个二氧化碳分子 表示该物质的构成 表示一个二氧化碳分子由一个碳原子和两个氧原子构成 表示该物质的一个分子中原子个数比 n (C)∶n (O)=1∶2 3.化学式的读写方法: 物质类型 化学式的写法 化学式的读法 单质 金属 元素名称:Fe———铁 稀有气体 “某气”:He———氦气 非金属 固态 元素名称:S———硫 气态 在元素符号的右下角写一小数字表示。如:氧�———O2、氮�———N2、臭氧———O3 “某气”:O2———氧气 化合物 氧化物 氧元素符号在后,另一元素符号在前。如:CO2、CuO等 从后向前读作“氧化某”,如:CuO———氧化铜;有时需读出原子个数,如:Fe3O4———四氧化三铁 由金属元素和非金属元素组成的化合物 非金属元素符号在后,金属元素符号在前。如:ZnS、KCl等 从后向前读作“某化某”,如:ZnS———硫化锌;有时需读出原子个数,如:FeCl3———三氯化铁 【要点诠释】 1.当表述物质组成和构成时要“宏观对宏观”“微观对微观”“个数对个数”。如CO2由碳元素和氧元素组成,1个CO2分子由1个碳原子和2个氧原子构成。也可简单记忆为“见分子用原子,不见分子用元素”。 2.化学式书写规则:书写步骤可概括为:正左、负右、标价、化简、交叉、检查。 (1)一般正价元素在前,负价元素在后(CH4和NH3例外),每种元素的原子数写在符号右下角。 (2)化学式中原子(原子团)个数比一般是最简整数比,元素正负化合价代数和为零。 (3)化学式中原子团个数不为1时,原子团必须加括号。如Ca(OH)2、Mg(NO3)2等。 考点二、化合价 1.元素化合价的表示方法:标化合价时,先写“+”或“-”号,再写化合价的数值,标在元素符号的正上方。如:、、。 2.化合价规则: (1)在化合物中各元素化合价代数和为零。如:。 (+1)+(+7)+(-2)×4=0。 (2)单质中元素的化合价为零。如、。 (3)在原子团形成的离子中,各元素的化合价代数和等于离子所带电荷数。如:SO42-。 (+6)+(-2)×4=-2。 3.常见元素的化合价: (1)氢元素通常显+1价,氧元素显-2价。例如:,,。 (2)金属元素一般显正价。例如:,,。 (3)非金属与氢或金属化合时,非金属显负价;非金属与氧元素化合时,非金属显正价。例如:在、、中,硫、氯、磷三种元素的化合价分别为-2、-1和+5。 (4)许多元素具有可变化合价。例如:Fe有0、+2、+3价;Cl有-1、0、+1、+3、+5、+7价;硫有-2、0、+4、+6价。 (5)Fe3O4可看成。 4.化合价的应用: (1)根据化合价求化合物的化学式。 (2)根据化学式求元素的化合价。 化合物中正负化合价的代数和为零是解答此类问题的基础,一般是跟据无多价元素的化合价求有多价元素的化合价。例如计算KClO3中氯元素的化合价,方法为:设氯元素的化合价为X,依据K、O在化合物中分别为+1价和-2价,各元素正负价的代数和为零列出代数式:(+1)+X+(-2) ×3==0 解得X==+5,所以KClO3中氯元素显+5价。 【要点诠释】 1.元素化合价记忆法: (1)化合价、化学式联系记忆法。如记住了SO2和SO3就记住了硫元素有+4价和+6价。 ... ...
~~ 您好,已阅读到文档的结尾了 ~~

