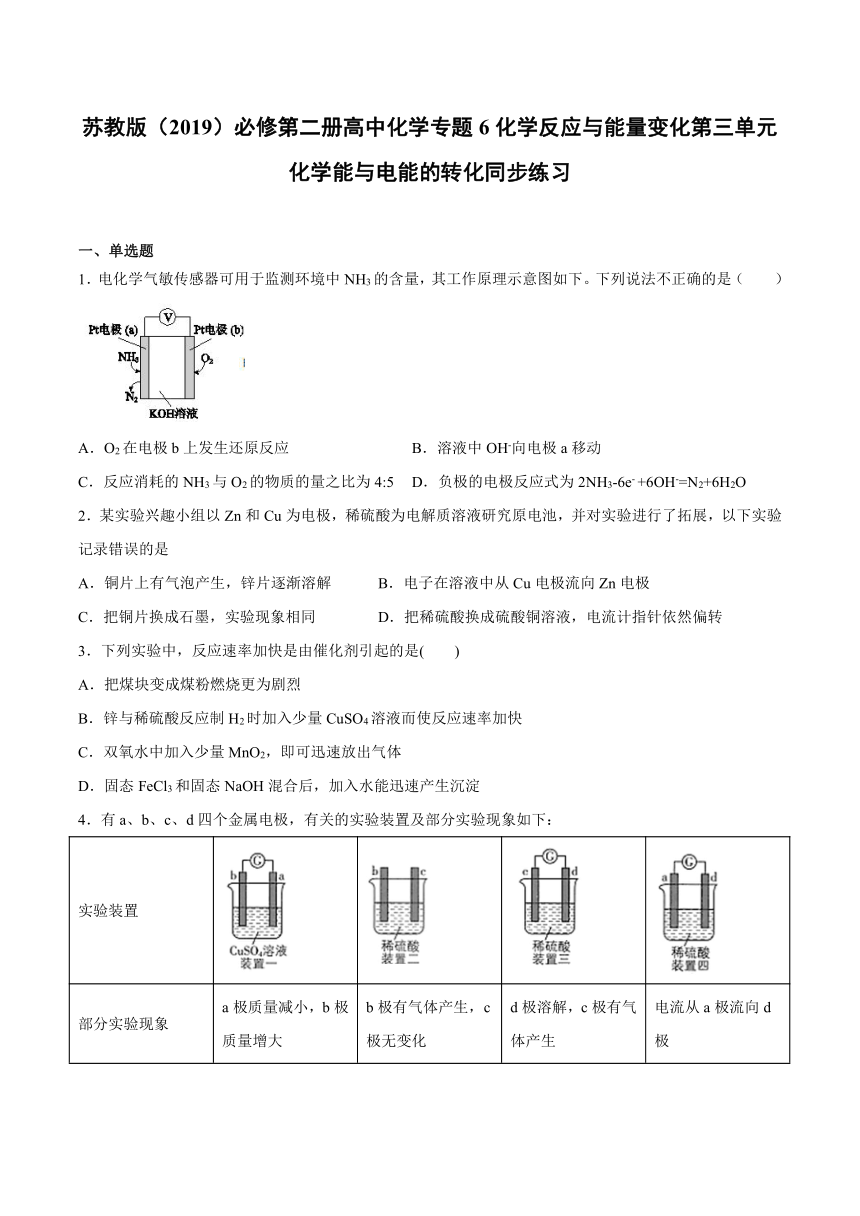
苏教版(2019)必修第二册高中化学专题6化学反应与能量变化第三单元化学能与电能的转化同步练习 一、单选题 1.电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法不正确的是( ) A.O2在电极b上发生还原反应 B.溶液中OH-向电极a移动 C.反应消耗的NH3与O2的物质的量之比为4:5 D.负极的电极反应式为2NH3-6e- +6OH-=N2+6H2O 2.某实验兴趣小组以Zn和Cu为电极,稀硫酸为电解质溶液研究原电池,并对实验进行了拓展,以下实验记录错误的是 A.铜片上有气泡产生,锌片逐渐溶解 B.电子在溶液中从Cu电极流向Zn电极 C.把铜片换成石墨,实验现象相同 D.把稀硫酸换成硫酸铜溶液,电流计指针依然偏转 3.下列实验中,反应速率加快是由催化剂引起的是( ) A.把煤块变成煤粉燃烧更为剧烈 B.锌与稀硫酸反应制H2时加入少量CuSO4溶液而使反应速率加快 C.双氧水中加入少量MnO2,即可迅速放出气体 D.固态FeCl3和固态NaOH混合后,加入水能迅速产生沉淀 4.有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下: 实验装置 部分实验现象 a极质量减小,b极质量增大 b极有气体产生,c极无变化 d极溶解,c极有气体产生 电流从a极流向d极 由此可判断这四种金属的活动性顺序是( ) A. B. C. D. 5.有关电化学知识的描述正确的是 A.由于CaO+H2OCa(OH)2,可以放出大量的热,故可把该反应设计成原电池 B.当马口铁(镀锡铁)的镀层破损后,马口铁腐蚀会加快 C.原电池的电极附近溶液pH的变化可以用电池总反应式来判断 D.铅蓄电池放电时的正极反应式为PbO2 +4H+ +2e-Pb2+ +2H2O 6.近两年,我县电动汽车(标志为“”)逐渐增多,为保护环境做出了积极贡献。下列说法错误的是 A.电动汽车使用时涉及化学能与电能的转换 B.燃油汽车与电动汽车的动力能量转换完全一致 C.电动汽车充电、放电过程均有电子转移 D.电动汽车的使用有助于减少氮氧化物的排放 7.对于敞口容器中的化学反应:Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g),下列叙述中不正确的是( ) A.Zn和H2SO4的总能量大于ZnSO4和H2的总能量 B.反应过程中能量关系可用上图表示 C.若将该反应设计成原电池,则Zn为负极 D.若将该反应设计成原电池,当有32.5g锌溶解时正极放出22.4 L气体 8.将纯锌片和纯铜片按图所示插入相同浓度的稀硫酸中,以下有关叙述正确的是( ) A.甲装置中电能转化为化学能 B.乙装置中电能转化为化学能 C.甲装置中铜片表面有气泡产生 D.乙装置中铜片表面有气泡生成 9.银锌纽扣电池,其电池的电池反应式为:Zn + Ag2O + H2O =Zn(OH)2 + 2Ag 下列说法不正确的是 A.锌作负极 B.正极发生还原反应 C.电池工作时,电流从Ag2O经导线流向Zn D.负极的电极方程式为:Zn-2e- = Zn2+ 10.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3?)以达到消除污染的目的。其工作原理的示意图如下: 下列说法不正确的是 A.Ir的表面发生反应:H2 + N2O=N2 + H2O B.导电基体上的负极反应:H2-2e?=2H+ C.若导电基体上只有单原子铜,也能消除含氮污染物 D.若导电基体上的Pt颗粒增多,不利于降低溶液中的含氮量 11.电子表和电子计算器的电源通常用微型银-锌电池,其电极分别为 Ag2O 和Zn, 电解质为 KOH 溶液,电极总反应为:Ag2O + H2O + Zn = Zn(OH)2 + 2Ag。 下列叙述正确的是 A.Zn是正极 B.Ag2O 电极上发生氧化反应 C.工作时正极区溶液的pH增大 D.工作时电子由 Ag2O 极经外电路流向Zn极 12.一定量的盐酸和过量的铁粉反应时,为了增大反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的 A.NaOH(s) B.NaCl(s) C.CuSO4 (s) D.H2O 13.A、B、C都是金属,A和C分别放入同浓度的稀硫酸中 ... ...
~~ 您好,已阅读到文档的结尾了 ~~