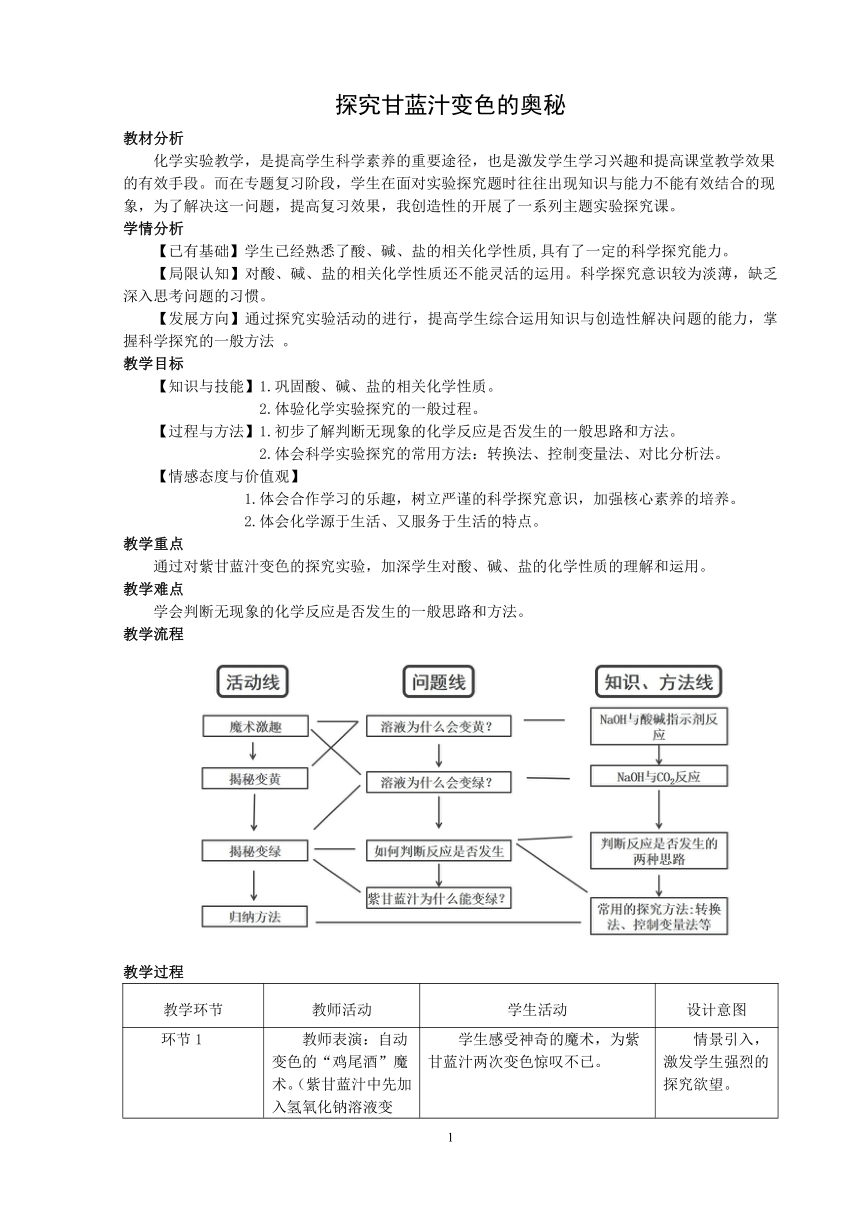
探究甘蓝汁变色的奥秘 教材分析 化学实验教学,是提高学生科学素养的重要途径,也是激发学生学习兴趣和提高课堂教学效果的有效手段。而在专题复习阶段,学生在面对实验探究题时往往出现知识与能力不能有效结合的现象,为了解决这一问题,提高复习效果,我创造性的开展了一系列主题实验探究课。 学情分析 【已有基础】学生已经熟悉了酸、碱、盐的相关化学性质,具有了一定的科学探究能力。 【局限认知】对酸、碱、盐的相关化学性质还不能灵活的运用。科学探究意识较为淡薄,缺乏深入思考问题的习惯。 【发展方向】通过探究实验活动的进行,提高学生综合运用知识与创造性解决问题的能力,掌握科学探究的一般方法 。 教学目标 【知识与技能】1.巩固酸、碱、盐的相关化学性质。 2.体验化学实验探究的一般过程。 【过程与方法】1.初步了解判断无现象的化学反应是否发生的一般思路和方法。 2.体会科学实验探究的常用方法:转换法、控制变量法、对比分析法。 【情感态度与价值观】 1.体会合作学习的乐趣,树立严谨的科学探究意识,加强核心素养的培养。 2.体会化学源于生活、又服务于生活的特点。 教学重点 通过对紫甘蓝汁变色的探究实验,加深学生对酸、碱、盐的化学性质的理解和运用。 教学难点 学会判断无现象的化学反应是否发生的一般思路和方法。 教学流程 教学过程 教学环节 教师活动 学生活动 设计意图 环节1 魔术激趣 教师表演:自动变色的“鸡尾酒”魔术。(紫甘蓝汁中先加入氢氧化钠溶液变黄,再加入干冰,溶液又由黄色变为绿色。)为什么紫甘蓝汁会现两次变色呢? 学生感受神奇的魔术,为紫甘蓝汁两次变色惊叹不已。 情景引入,激发学生强烈的探究欲望。 环节2 揭秘变黄 紫甘蓝汁由紫色变黄,秘密在哪? 学生根据 “紫甘蓝汁是酸碱指示剂” 这一在“自制酸碱指示剂”所学到的旧有知识,很快判断出变黄的原因,是利用氢氧化钠能与酸碱指示剂反应的性质。 从学生的“最近发展区”出发,便于学生进行有效的分析与判断。 环节3 揭秘变绿 变黄的紫甘蓝汁在放入干冰后为什么又会变绿呢? 你能设计实验方案验证是否是CO2与水反应生成的H2CO3使紫甘蓝汁变绿? 有什么方法能验证是CO2与NaOH反应导致溶液变绿呢? 教师提供信息: “氢氧化钠易溶于酒精,碳酸钠微溶于酒精”并请学生根据所给信息及已有知识,利用本组所给定的实验仪器和用品,设计实验进行验证,并用文字或图画的形式将方案、现象及得出的结论记录在实验单上。 教师及时提供仪器, 教师适时追问,酚酞在碳酸钠溶液中显现什么颜色? 教师展示网络资料:紫甘蓝汁在不同PH的溶液中可以表现不同的颜色。 生活中我们在食用凉拌紫甘蓝菜时常会加入少许的醋,不仅能使其口味更加丰富,也使其色彩更加诱人;我们的生活中除紫甘蓝外还有很多蔬菜和花朵当遇到不同PH的溶液也会显现不同的颜色。 学生根据溶液中存在的三种物质,经过小组讨论对液体变绿进行了合理的猜想: ( 猜想 )①CO2与水反应生成的H2CO3使溶液变绿 ②CO2与NaOH反应导致溶液变绿 学生分组实验:向紫甘蓝汁吹气。 观察现象:溶液变红 得出结论:紫甘蓝汁变绿不是CO2与水反应生成的H2CO3导致的。排除猜想1。 学生向NaOH溶液中吹气, 没有观察到任何现象,从而引发了学生思考,如何判断两者发生了反应? 学生分组讨论,在老师的指导下总结出: 对于没有现象的反应判断其是否发生,有两个思路: ①证明反应物减少, ②证明生成了新的物质。 学生以小组为单位进行实验验证。 证明有新物质生成的方案中,学生设计出如下方案: ①根据资料的提示,向氢氧化钠的酒精溶液中吹气,由于碳酸钠微溶于酒精,溶液会变浑浊,从而证明有碳酸钠生成,猜想二成立。 ②向CO2与NaOH反应后的溶液中滴入稀盐酸,观察是否有气泡产生。 ③ ... ...
~~ 您好,已阅读到文档的结尾了 ~~