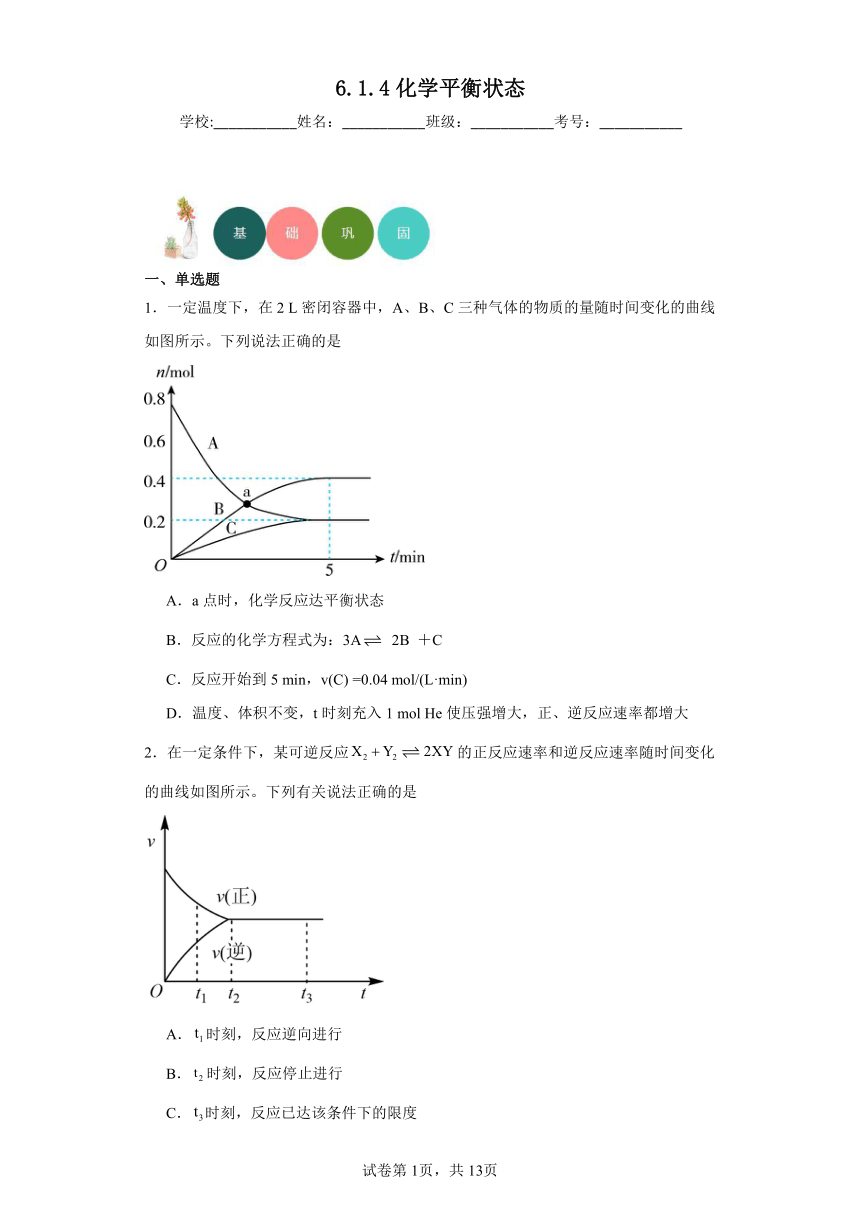
6.1.4化学平衡状态 学校:_____姓名:_____班级:_____考号:_____ 一、单选题 1.一定温度下,在2 L密闭容器中,A、B、C三种气体的物质的量随时间变化的曲线如图所示。下列说法正确的是 A.a点时,化学反应达平衡状态 B.反应的化学方程式为:3A 2B +C C.反应开始到5 min,v(C) =0.04 mol/(L·min) D.温度、体积不变,t时刻充入1 mol He使压强增大,正、逆反应速率都增大 2.在一定条件下,某可逆反应的正反应速率和逆反应速率随时间变化的曲线如图所示。下列有关说法正确的是 A.时刻,反应逆向进行 B.时刻,反应停止进行 C.时刻,反应已达该条件下的限度 D.时刻,反应物的量逐渐增多 3.工业合成氨是重要的人工固氮的方式,在一个恒容容器中充入N2(g)和H2(g),一定条件下发生反应N2(g)+3H2(g)2NH3(g),若温度保持不变,下列说法正确的是 A.当充入足够N2(g)后,H2(g)会全部转化 B.升温可以加快化学反应速率故工业合成氨时温度越高越好 C.正、逆反应速率相等时,N2与H2浓度比一定是1:3 D.通过调控反应条件,可以提高该反应进行的程度 4.一定条件下,向某恒温恒容密闭容器中通入一定量的氢气和溴蒸气,发生反应,下列说法错误的是 A.反应达到化学平衡状态前,正反应速率逐渐减小 B.向容器中充入气体,压强增大,反应速率加快 C.容器内的气体颜色不变时,说明反应达到平衡状态 D.容器内的气体的密度和压强始终保持不变 5.设NA为阿伏加德罗常数的值。下列说法正确的是 A.标准状况下22.4LCHCl3含有C-Cl键的数目为3NA B.25℃时pH=1的盐酸含有H+总数为0.1NA C.1molPCl3和1molCl2在密闭容器中充分反应,生成物中P-Cl键的数目为5NA D.100g质量分数为46%的乙醇溶液含有的氧原子总数为4NA 6.对于可逆反应M + 3N2Q达到平衡时,下列说法正确的是 A.反应已经停止 B.M、N全部变成了Q C.反应混合物各组分的浓度不再变化 D.M、N、Q三种物质的浓度一定相等 7.合成氨是工业上的重要反应:N2(g)+3H2(g)2NH3(g),下列说法不正确的是( ) A.反应达平衡状态后,各物质浓度不再改变 B.反应达平衡状态后,单位时间内生成1molN2的同时消耗3molH2 C.若改用新型高效催化剂,N2有可能100%转化为NH3 D.使用催化剂是为了加快反应速率,提高生产效率 8.一定温度下在一容积不变的密闭容器中发生可逆反应2X(g) Y(g)+Z(s),下列叙述不能说明该反应达到化学平衡状态的是 A.v正 (X) = 2 v逆 (Y) B.X的分解速率与Y的消耗速率相等 C.反应容器中Y的质量分数不变 D.单位时间内生成1 mol Y的同时生成2 mol X 9.汽车尾气系统中的催化转化器,可有效降低尾气中的CO、NO和NO2等向大气的排放。在催化转化器的前半部发生的反应为2CO(g)+2NO(g)2CO2(g)+N2(g)。下列有关叙述正确的是 A.反应达平衡时,正、逆反应速率均为零 B.使用合适的催化剂,反应速率会加快 C.升高温度,反应速率可能减慢 D.反应达平衡时,尾气中CO2、N2的浓度之比为2:1 10.下列说法错误的是 A.水的生成与电解是可逆反应 B.温度升高,正、逆反应速率都增大 C.化学反应的速率和限度均可通过改变化学反应条件来改变 D.化学反应达到平衡状态时,正反应速率与逆反应速率相等 二、填空题 11.在密闭容器中进行反应2SO2(g)+O2(g)2SO3(g),当SO2、O2、SO3的浓度之比为2∶1∶2时,能否说明该反应达到化学平衡状态 12.现代社会中,人类的一切活动都离不开能量。化学反应中,不仅有新物质的生成,而且伴随着能量的变化,同时,化学电池也成为人类生产和生活的重要能量来源之一。回答下列问题: (1)已知:键能是在标准状况下,将气态分子解离为气态原子所需的能量。请从断键和成键的角度分析下列反应中能量的变化。部分化学键的键能如表所示: 化学键 键能 436 496 46 ... ...
~~ 您好,已阅读到文档的结尾了 ~~