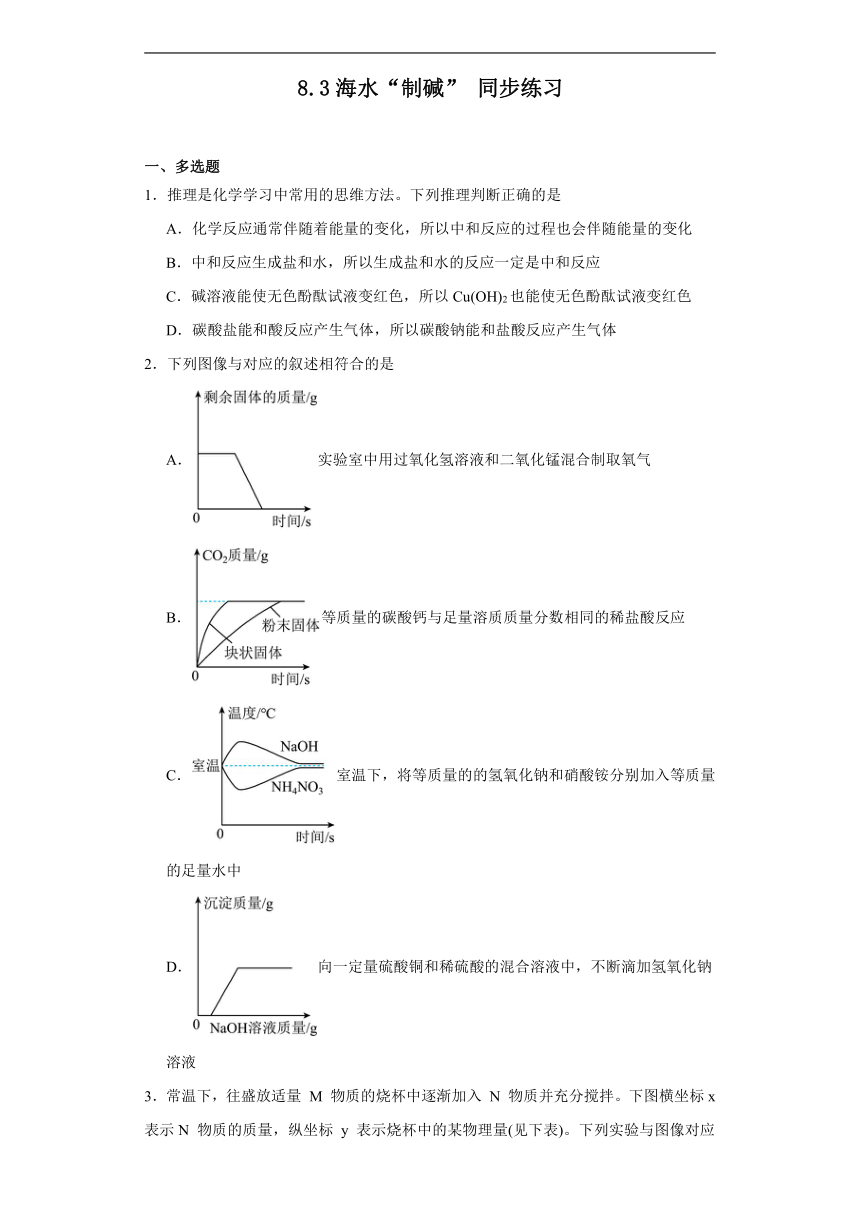
8.3海水“制碱” 同步练习 一、多选题 1.推理是化学学习中常用的思维方法。下列推理判断正确的是 A.化学反应通常伴随着能量的变化,所以中和反应的过程也会伴随能量的变化 B.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 C.碱溶液能使无色酚酞试液变红色,所以Cu(OH)2也能使无色酚酞试液变红色 D.碳酸盐能和酸反应产生气体,所以碳酸钠能和盐酸反应产生气体 2.下列图像与对应的叙述相符合的是 A.实验室中用过氧化氢溶液和二氧化锰混合制取氧气 B.等质量的碳酸钙与足量溶质质量分数相同的稀盐酸反应 C.室温下,将等质量的的氢氧化钠和硝酸铵分别加入等质量的足量水中 D.向一定量硫酸铜和稀硫酸的混合溶液中,不断滴加氢氧化钠溶液 3.常温下,往盛放适量 M 物质的烧杯中逐渐加入 N 物质并充分搅拌。下图横坐标x表示N 物质的质量,纵坐标 y 表示烧杯中的某物理量(见下表)。下列实验与图像对应关系合理的是 M N(x) y A 水 氧化钙 溶液的质量 B 水 氢氧化钠 溶液的温度 C 饱和石灰水 氧化钙 溶液中溶质的质量 D 饱和硫酸铜溶液 无水硫酸铜 溶液的质量 A.A B.B C.C D.D 4.实验室内有一瓶没有标签的白色粉末,为探究该药品的成分,某实验小组将该药品分别加入四种实验试剂中进行实验,根据实验现象,该样品的成分可能是: 实验试剂 实验现象 水 白色粉末溶解 稀盐酸 有气泡产生 氢氧化钡溶液 有白色沉淀产生 氯化钙溶液 有白色沉淀产生 A.碳酸钠 B.碳酸钙 C.氯化镁 D.碳酸钾 5.现有一包粉末,可能含有NaC1、Na2CO3、K2CO3、FeCl3、CaC12中的一种或几种物质。小明同学对这包粉末的成分进行了如下探究: (1)取少量该粉末,加水溶解后得到无色透明溶液。 (2)向(1)所得溶液中加入过量Ba(NO3)2溶液后,产生白色沉淀,加入足量稀硝酸,沉淀全部溶解并产生大量气泡。 (3)取13.8g该粉末加入足量的稀盐酸,充分反应后产生4.4g二氧化碳。 根据上述操作和现象,下列说法中一定正确的是 A.该粉末中一定不含FeCl3 B.(2)实验结束后所得溶液中只含有和Na+ C.该粉末中一定含有K2CO3 D.该粉末的组成最多有三种情况 二、选择题 6.下列物质能在pH=12的无色溶液中大量共存的是 A.KNO3、FeCl3、NaCl B.HCl、AgNO3、K2SO4 C.BaCl2、NH4Cl、ZnCl2 D.NaNO3、Na2CO3、NaOH 7.下列物质之间不能发生反应的是( ) A.H2SO4与NaOH B.HCl与Na2SO4 C.K2CO3与CaCl2 D.NaCl与AgNO3 8.下列各组物质的名称、俗称、化学式均表示同一种物质的是( ) A.硫酸铜晶体,胆矾,CuSO4 5H2O B.氯化钠,苏打,NaCl C.氢氧化钠,纯碱,NaOH D.碳酸钙,生石灰,Ca(OH)2 9.除去下列物质中的少量杂质,所用试剂及方法正确的是 选项 混合物(括号内为杂质) 试剂及方法 A CaO(CaCl2) 加水溶解、过滤、洗涤、干燥 B O2(H2O) 通入浓硫酸干燥 C Na2SO4溶液(Na2CO3) 加入过量稀硫酸 D CO2(CO) 通入澄清石灰水 A.A B.B C.C D.D 10.碳酸钠是重要的化工原料。早期曾以食盐、浓硫酸、木炭和石灰石为原料制取碳酸 钠,具体工艺流程如下图所示。我国化学工程专家侯德榜先生改进了原有的制碱方法,发明了将制碱与制氨结合起来的“侯氏制碱法”,大大提高了原料的利用率。 根据以上信息及工艺流程图判断,以下说法错误的是( ) A.反应①属于复分解反应 B.该流程中产生的有害气体 CO 和HCl,可用水加以吸收处理 C.步骤③中“水浸”时需要搅拌,目的是加快碳酸钠的溶解速率 D.侯氏制碱法更符合“绿色化学” 11.下列各组物质的溶液,不加试剂能鉴别出来的是 A.NaOH、NaCl、KNO3 B.Na2CO3、BaCl2、Na2SO4 C.FeCl3、NaOH、NH4Cl D.Ca(NO3)2、K2CO3、NaNO3 12.在pH=2的溶液中,下列离子能大量共存的是 A.Ba2+ ... ...
~~ 您好,已阅读到文档的结尾了 ~~