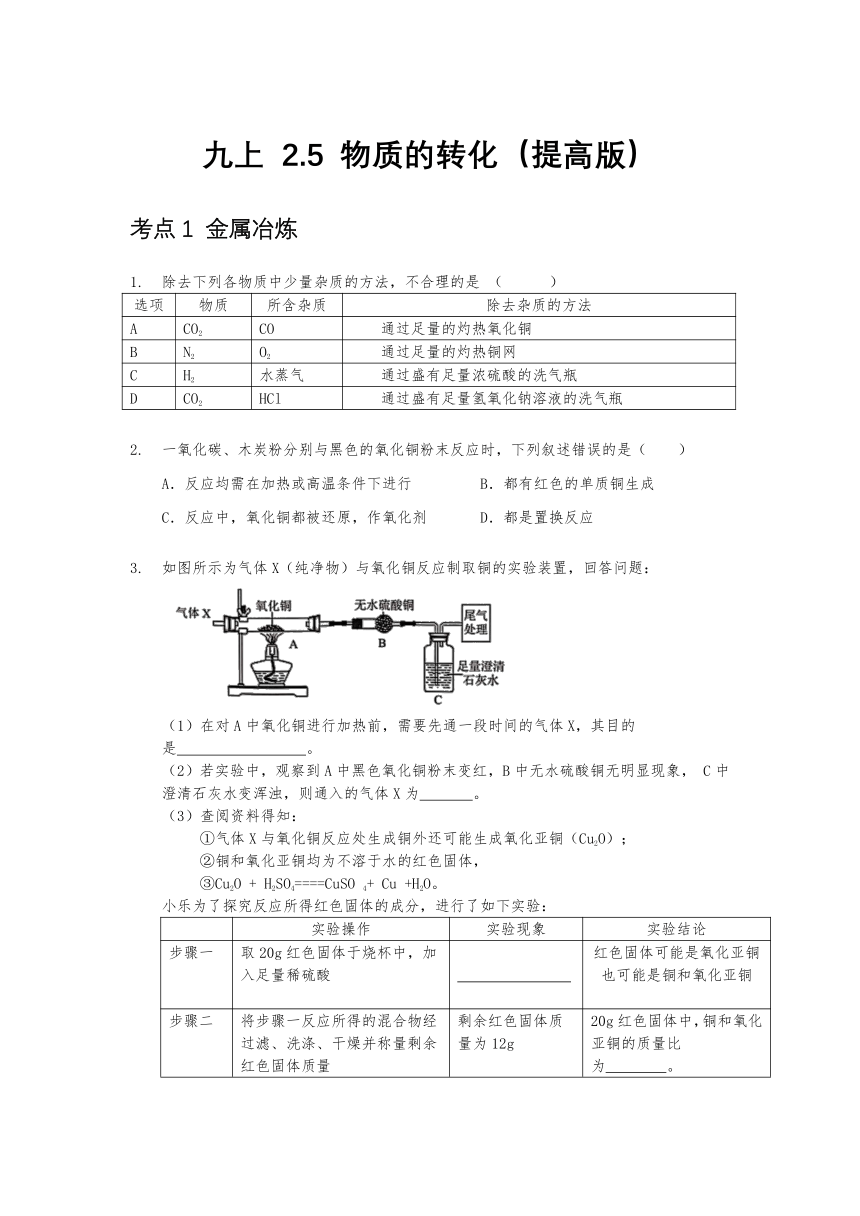
九上 2.5 物质的转化(提高版) 考点1 金属冶炼 除去下列各物质中少量杂质的方法,不合理的是 ( ) 选项 物质 所含杂质 除去杂质的方法 A CO2 CO 通过足量的灼热氧化铜 B N2 O2 通过足量的灼热铜网 C H2 水蒸气 通过盛有足量浓硫酸的洗气瓶 D CO2 HCl 通过盛有足量氢氧化钠溶液的洗气瓶 一氧化碳、木炭粉分别与黑色的氧化铜粉末反应时,下列叙述错误的是( ) A.反应均需在加热或高温条件下进行 B.都有红色的单质铜生成 C.反应中,氧化铜都被还原,作氧化剂 D.都是置换反应 如图所示为气体X(纯净物)与氧化铜反应制取铜的实验装置,回答问题: (1)在对A中氧化铜进行加热前,需要先通一段时间的气体X,其目的是 。 (2)若实验中,观察到A中黑色氧化铜粉末变红,B中无水硫酸铜无明显现象, C中澄清石灰水变浑浊,则通入的气体X为 。 (3)查阅资料得知: ①气体X与氧化铜反应处生成铜外还可能生成氧化亚铜(Cu2O); ②铜和氧化亚铜均为不溶于水的红色固体, ③Cu2O + H2SO4====CuSO 4+ Cu +H2O。 小乐为了探究反应所得红色固体的成分,进行了如下实验: 实验操作 实验现象 实验结论 步骤一 取20g红色固体于烧杯中,加入足量稀硫酸 红色固体可能是氧化亚铜也可能是铜和氧化亚铜 步骤二 将步骤一反应所得的混合物经过滤、洗涤、干燥并称量剩余红色固体质量 剩余红色固体质量为12g 20g红色固体中,铜和氧化亚铜的质量比为 。 某化学兴趣小组同学利用图中所示装置模拟炼铁: (1)为了避免玻璃管a在加热时可能发生爆炸,加热前应 . (2)a管中氧化铁发生反应的化学方程式为 . (3)B装置可用来吸收二氧化碳气体,写出该反应的化学方程式 ;B装置 (填“能”或“不能”)用来收集CO. (4)若a管中氧化铁全部还原成铁,冷却后称量铁的质量比反应前氧化铁的质量减少了2.4g,则加入a管中氧化铁的质量是 g. 已知某混合气体由H2、CO和CO2三种气体组成。为验证该混合气体成分,科学研究小组的同学经过讨论,设计了如图1所示的实验方案。 根据方案回答下列问题: (1)装置C在实验中的作用是_____。 (2)仅根据D装置中黑色粉末变红这一现象,能否证明混合气体中一定存在CO?请判断并说明理由_____。 (3)小丁根据装置E中出现白色硫酸铜粉末变成蓝色的实验现象,得出该混合气体中有氢气存在的结论。你认为结论是否可靠?若可靠,请说明理由;若不可靠,请对图1实验装置提出改进意见。_____。 (4)图1方案中B装置可用来吸收CO2但没有现象。为证明CO2和NaOH能发生反应,小丁又设计了图2所示的方案。则图2方案中所加试剂X应该是_____。 考点2物质的转化 如图是小科同学绘制的单质铜及其化合物的转化模型图,其中能转化的环节有( ) A.①② B.③④ C.①③ D.②④ Ca与水可以发生剧烈反应并产生一种气体。单质Ca的一种转化路线为:Ca→CaO→Ca(OH)2→CaCO3,有关说法错误的是( ) A.Ca与水反应产生的气体是氢气 B.CaO也可直接转化为CaCO3 C.CaO和Ca(OH)2均可用于吸收SO2 D.Na与Cu也可以发生上述转化 如图表示元素的化合价与物质类别的关系,“→”表示物质之间可以转化,甲、乙、丙、丁、戊是初中化学常见物质,它们均含有X元素。下列有关说法正确的是( ) A.戊代表的物质均易溶于水 B.由X元素形成的不同单质具有相同的性质 C.“甲→乙→丙”的转化都只能通过与O2反应来实现 D.加热丁和紫色石蕊的混合液,溶液颜色由红色变紫色 下列物质的转化都能一步实现: Fe2O3→FeCl3 ②Fe(OH)3→FeCl3 ③Fe2(SO4)3→FeCl3 下列相关说法不正确的是( ) A.三个反应中铁元素的化合价均不变 B.三个反应均可用于制备氯化铁溶液 C.三个反应中均有明显现象产生 D.三个反应都可通过加入盐酸 ... ...
~~ 您好,已阅读到文档的结尾了 ~~

