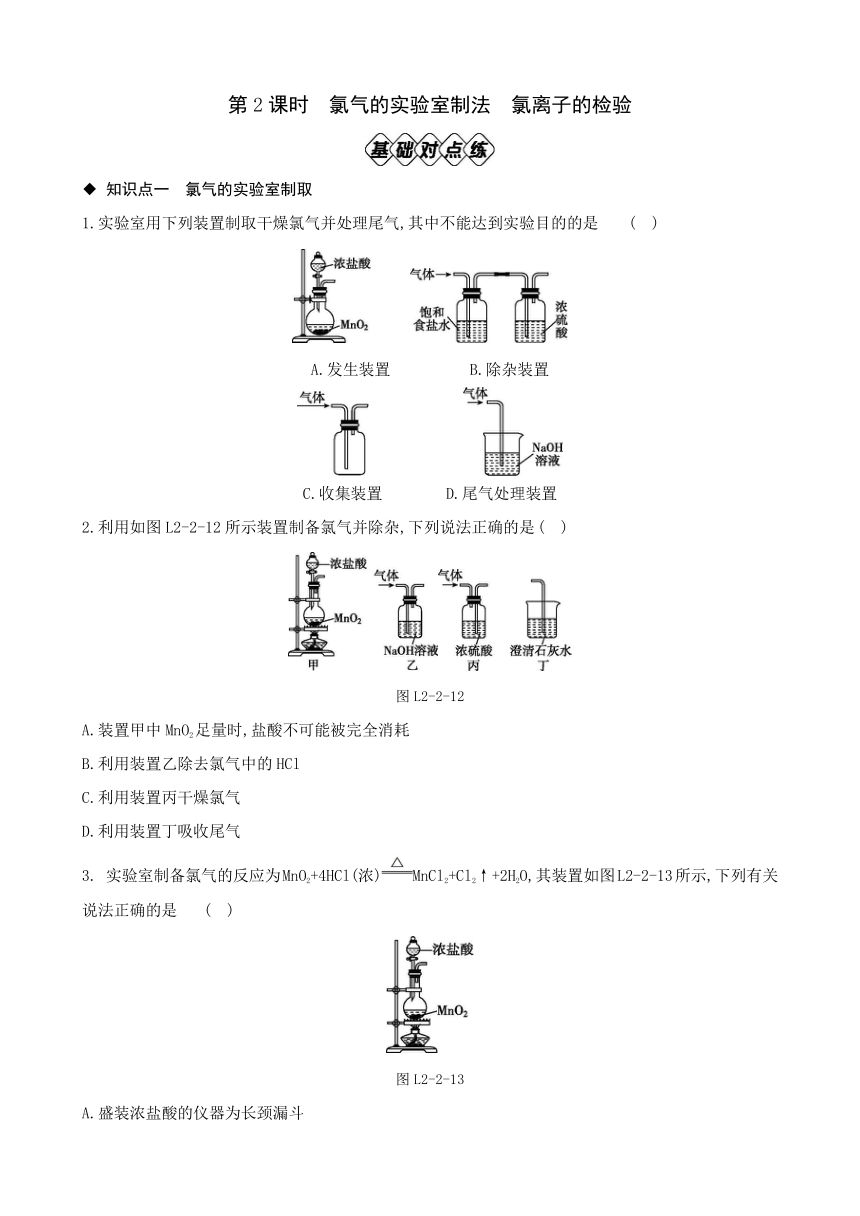
第2课时 氯气的实验室制法 氯离子的检验 ◆ 知识点一 氯气的实验室制取 1.实验室用下列装置制取干燥氯气并处理尾气,其中不能达到实验目的的是 ( ) A.发生装置 B.除杂装置 C.收集装置 D.尾气处理装置 2.利用如图L2-2-12所示装置制备氯气并除杂,下列说法正确的是 ( ) 图L2-2-12 A.装置甲中MnO2足量时,盐酸不可能被完全消耗 B.利用装置乙除去氯气中的HCl C.利用装置丙干燥氯气 D.利用装置丁吸收尾气 3. 实验室制备氯气的反应为MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,其装置如图L2-2-13所示,下列有关说法正确的是 ( ) 图L2-2-13 A.盛装浓盐酸的仪器为长颈漏斗 B.可用向下排空气法收集氯气 C.制取的氯气中会混有HCl和水蒸气 D.可用该制备氯气的装置来制备氢气 4. 实验室可用高锰酸钾和浓盐酸反应制取氯气,其反应原理为2KMnO4+16HCl(浓)2KCl+2MnCl2+5Cl2↑+8H2O,实验室用如图L2-2-14所示装置制取少量Cl2,其中能达到相应实验目的的是 ( ) 图L2-2-14 A.用装置甲生成Cl2 B.用装置乙除去Cl2中的HCl C.用装置丙收集Cl2 D.用装置丁吸收Cl2尾气 5. 某同学用以下装置制备并检验Cl2的性质。下列说法正确的是( ) 图L2-2-15 A.图Ⅰ:制备并收集纯净的氯气 B.图Ⅱ:只证明新制氯水具有酸性 C.图Ⅲ:产生了棕黄色的雾 D.图Ⅳ:湿润的有色布条褪色 6. 钠元素在自然界分布很广,储量极为丰富,都以化合态存在。19世纪初,英国化学家戴维在实验室中电解熔融氯化钠,首次获得了金属钠,为深入探究钠的性质提供了可能。钠和含钠的化合物(如NaCl、Na2O2、Na2CO3、NaHCO3等)在生产生活中被广泛应用。例如高压钠灯可用于道路和广场照明,还可以用Na来制取钛(Ti)、锆(Zr)、铌(Nb)等稀有金属等。化学研究性学习小组设计了如下装置制备少量氯化钠,无法达到实验目的的是 ( ) 图L2-2-16 A.用装置甲制取氯气 B.用装置乙净化、干燥氯气 C.用装置丙制备氯化钠 D.用装置丁吸收尾气 ◆ 知识点二 氯离子(Cl-)的检验 7.检验某溶液中是否含有Cl-,正确的操作是 ( ) A.取样,滴加AgNO3溶液,看是否有白色沉淀生成 B.取样,先加足量的稀硝酸酸化,再加入AgNO3溶液,若有白色沉淀生成,则证明溶液中含有Cl- C.取样,先加入AgNO3溶液,有白色沉淀生成,再加稀盐酸,沉淀不溶解,则证明溶液中含有Cl- D.取样,先加稀盐酸酸化,再加AgNO3溶液,有白色沉淀,则证明溶液中含有Cl- 8. 下列是对“某溶液”进行离子检测的方法和结论,其中说法正确的是( ) A.加入稀盐酸,产生能使澄清石灰水变浑浊的无色气体,则“某溶液”中一定含有C B.先加入稀盐酸,再加入AgNO3溶液,有白色沉淀产生,则“某溶液”中一定含有Cl- C.加入BaCl2溶液,有白色沉淀产生,则“某溶液”中一定含有S D.加入HNO3酸化后,再加入AgNO3溶液,有白色沉淀产生,则“某溶液”中一定含有Cl- 9. 下列溶液中离子检验正确的是 ( ) A.向某溶液中滴加氯化钡溶液,有白色沉淀,证明含S B.某无色溶液中滴入无色酚酞溶液显红色,证明该溶液一定显碱性 C.某无色溶液滴入稀盐酸,产生气泡,证明该溶液一定含有C D.向某种溶液中加入稀盐酸酸化的硝酸银溶液,有白色沉淀生成,证明含Cl- 10. 图L2-2-17是实验室制备氯气,并通过干燥的蓝色石蕊试纸和湿润的蓝色石蕊试纸探究氯气是否有漂白性的装置(部分夹持装置略)。 图L2-2-17 下列说法正确的是 ( ) A.装置B中盛有饱和食盐水,实验结束时关闭K,可储存多余氯气 B.装置C和D中的试剂可以互换 C.Ⅰ和Ⅱ分别为干燥的蓝色石蕊试纸和湿润的蓝色石蕊试纸 D.实验中湿润的蓝色石蕊试纸直接变为无色 11. 实验室用如图L2-2-18所示装置制取氯气,并用氯气进行实验,D中为红色湿布条,E中为蘸有NaBr溶液的棉花团。已知溴水为橙黄色,实验中观察到E中棉花团变黄色,F中棉花团变蓝色。下列说法错误的是( ) 图L2-2-18 A.装 ... ...
~~ 您好,已阅读到文档的结尾了 ~~

