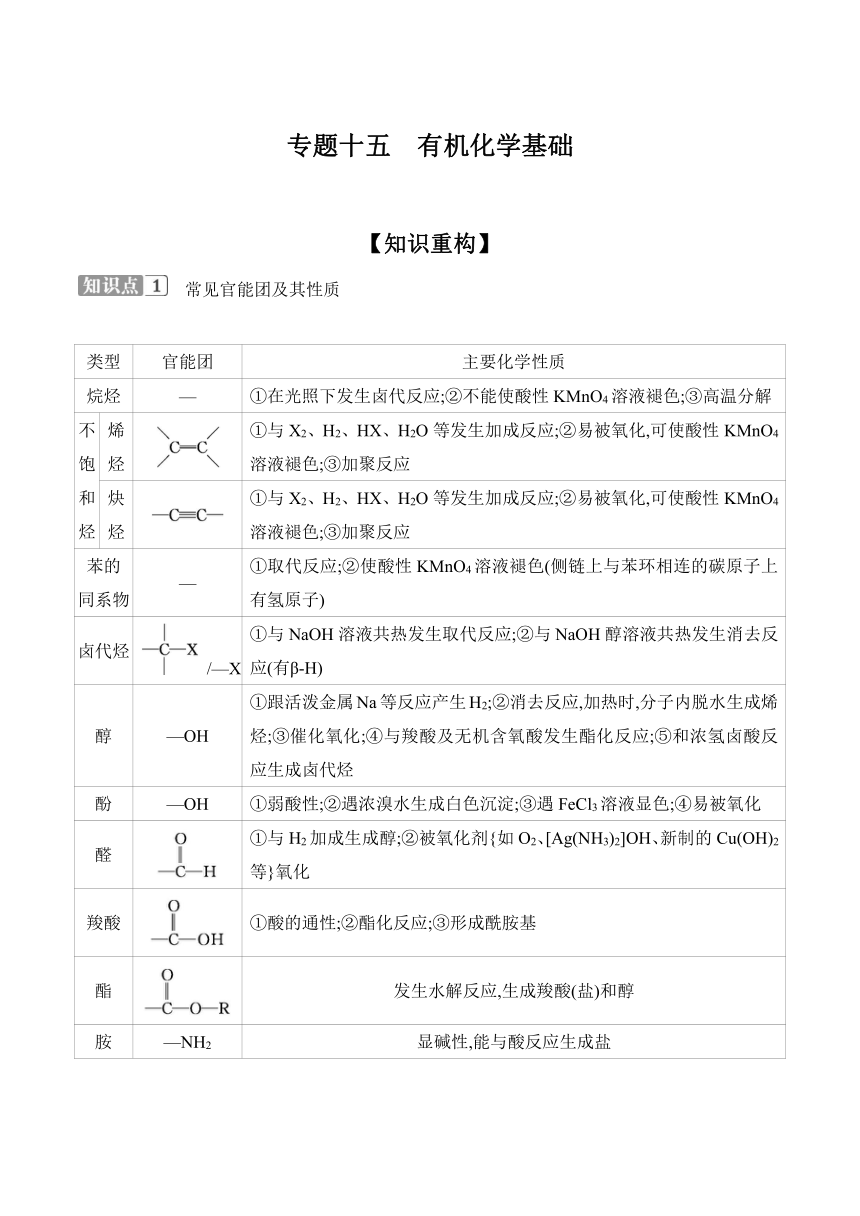
专题十五 有机化学基础 【知识重构】 常见官能团及其性质 类型 官能团 主要化学性质 烷烃 — ①在光照下发生卤代反应;②不能使酸性KMnO4溶液褪色;③高温分解 不饱和烃 烯烃 ①与X2、H2、HX、H2O等发生加成反应;②易被氧化,可使酸性KMnO4溶液褪色;③加聚反应 炔烃 ①与X2、H2、HX、H2O等发生加成反应;②易被氧化,可使酸性KMnO4溶液褪色;③加聚反应 苯的 同系物 — ①取代反应;②使酸性KMnO4溶液褪色(侧链上与苯环相连的碳原子上有氢原子) 卤代烃 /—X ①与NaOH溶液共热发生取代反应;②与NaOH醇溶液共热发生消去反应(有β-H) 醇 —OH ①跟活泼金属Na等反应产生H2;②消去反应,加热时,分子内脱水生成烯烃;③催化氧化;④与羧酸及无机含氧酸发生酯化反应;⑤和浓氢卤酸反应生成卤代烃 酚 —OH ①弱酸性;②遇浓溴水生成白色沉淀;③遇FeCl3溶液显色;④易被氧化 醛 ①与H2加成生成醇;②被氧化剂{如O2、[Ag(NH3)2]OH、新制的Cu(OH)2等}氧化 羧酸 ①酸的通性;②酯化反应;③形成酰胺基 酯 发生水解反应,生成羧酸(盐)和醇 胺 —NH2 显碱性,能与酸反应生成盐 酰胺 / 能在酸性或碱性条件下发生水解反应 确定官能团的方法 1.根据试剂或特征现象推知官能团的种类 ①使溴水褪色,则表示该物质中可能含有“”或“”结构 ②使KMnO4(H+)溶液褪色,则该物质中可能含有“”“”“—CH2OH”或“—CHO”等结构或为苯的同系物 ③遇FeCl3溶液显色,或加入溴水出现白色沉淀,则该物质中含有酚羟基 ④遇浓硝酸变黄,则表明该物质是含有苯环结构的蛋白质 ⑤遇I2变蓝,则该物质为淀粉 ⑥加入新制的Cu(OH)2,加热煮沸有红色沉淀生成;加入银氨溶液,水浴加热有银镜生成,表示含有—CHO ⑦加入Na放出H2,表示含有—OH或—COOH ⑧加入NaHCO3溶液产生气体,表示含有—COOH 2.根据数据确定官能团的数目 ① ②2—OH(醇、酚)H2 ③2—COOHH2,2—COOHCO2,—COOHCO2 ④, —C≡C—(或二烯、烯醛)—CH2CH2— ⑤某有机物与醋酸反应,相对分子质量增加42,则含有1个—OH;增加84,则含有2个—OH。即—OH转变为—OOCCH3 ⑥由—CHO转变为—COOH,相对分子质量增加16;若增加32,则含2个—CHO 2.根据数据确定官能团的数目 ⑦当醇被氧化成醛或酮后,相对分子质量减少2,则含有1个能被氧化的—OH;若相对分子质量减少4,则含有2个能被氧化的—OH 3.根据性质确定官能团的位置 ①若醇能氧化为醛或羧酸,则醇分子中应含有结构“—CH2OH”;若能氧化成酮,则醇分子中应含有结构“—CHOH———� ②由消去反应的产物可确定“—OH”或“—X”的位置 ③由一卤代物的种类可确定碳骨架 ④由加氢后的碳架结构,可确定“”或“—C≡C———�的位置 有机反应类型的判断 1.有机化学反应类型判断的基本思路 2.根据反应条件推断反应类型 ①在NaOH的水溶液中发生水解反应,可能是酯、酰胺的水解反应或卤代烃的水解反应 ②在NaOH的乙醇溶液中加热,发生卤代烃的消去反应 ③在浓硫酸存在的条件下加热,可能发生醇的消去反应、酯化反应、成醚反应,硝化反应等 ④能与溴水或溴的CCl4溶液反应,可能为烯烃、炔烃的加成反应 ⑤能与H2在Ni作用下发生反应,则为烯烃、炔烃、芳香烃、酮、醛的加成反应或还原反应 ⑥在O2、Cu(或Ag)、加热(或CuO、加热)条件下,发生醇的催化氧化反应 ⑦与O2或新制的Cu(OH)2或银氨溶液反应,则该物质发生的是—CHO的氧化反应。(如果连续两次出现O2,则为醇醛羧酸的过程) ⑧在稀硫酸加热条件下发生酯、酰胺、低聚糖、多糖等的水解反应 ⑨在光照、X2(表示卤素单质)条件下发生烷基上的取代反应;在Fe粉、X2条件下发生苯环上的取代反应 有机合成 1.原则 基础原料要价廉、易得、低毒性、低污染;产品易于分离、产率较高;合成线路简捷,操作简便,能耗低,易于实现 2.官能 团的 引入 引入官能团 有关反应 羟基(—OH) ... ...
~~ 您好,已阅读到文档的结尾了 ~~

