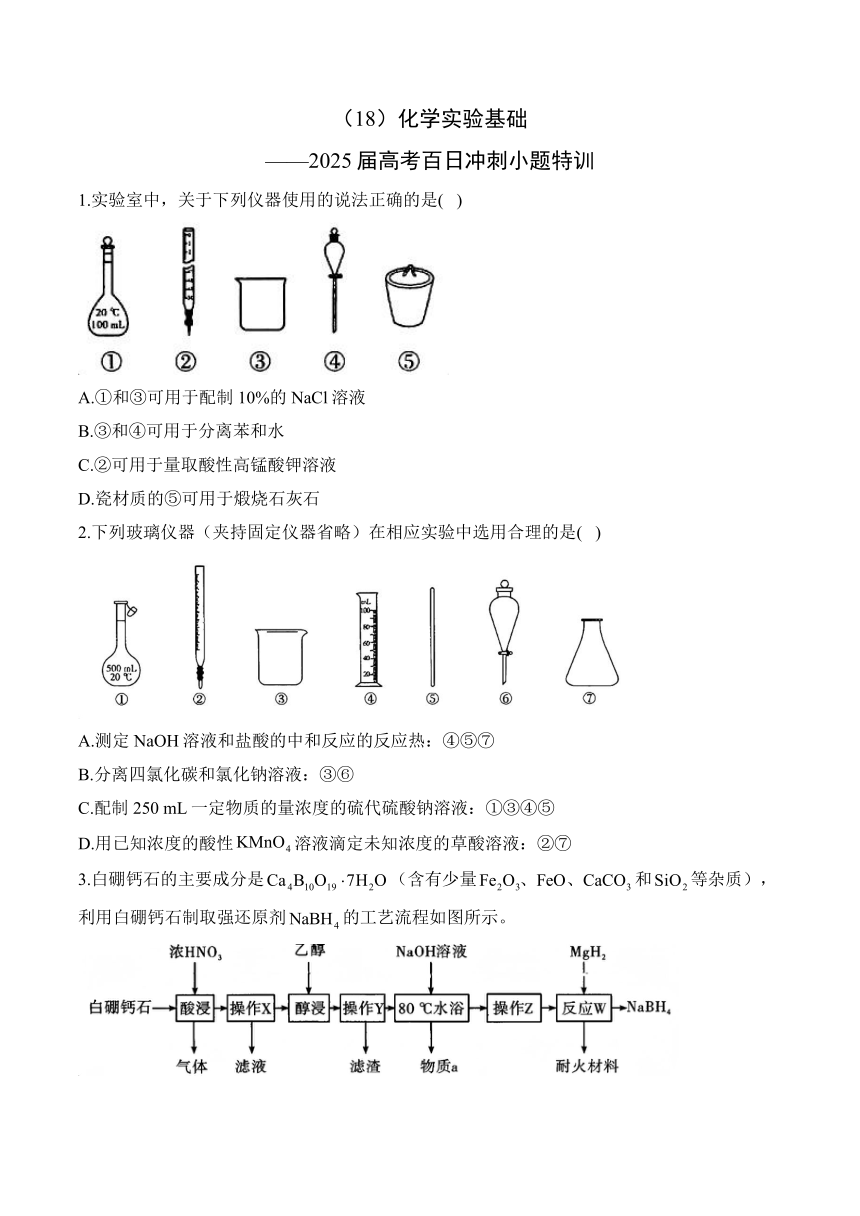
(18)化学实验基础 ———2025届高考百日冲刺小题特训 1.实验室中,关于下列仪器使用的说法正确的是( ) A.①和③可用于配制10%的NaCl溶液 B.③和④可用于分离苯和水 C.②可用于量取酸性高锰酸钾溶液 D.瓷材质的⑤可用于煅烧石灰石 2.下列玻璃仪器(夹持固定仪器省略)在相应实验中选用合理的是( ) A.测定NaOH溶液和盐酸的中和反应的反应热:④⑤⑦ B.分离四氯化碳和氯化钠溶液:③⑥ C.配制250 mL一定物质的量浓度的硫代硫酸钠溶液:①③④⑤ D.用已知浓度的酸性溶液滴定未知浓度的草酸溶液:②⑦ 3.白硼钙石的主要成分是(含有少量和等杂质),利用白硼钙石制取强还原剂的工艺流程如图所示。 已知微溶于水,易溶于乙醇;偏硼酸钠易溶于水,溶解度随温度升高而增大,难溶于乙醇,碱性条件下稳定。下列说法错误的是( ) A.“气体”中可能有 B.该流程用到两步过滤操作 C.物质a可循环利用 D.“反应W”为非氧化还原反应 4.某污水处理厂用“沉淀法”处理含铬废水(主要含以及少量、)的工艺流程如图所示: 已知:①金属离子、、沉淀完全时()pH分别为6.7、5.6、2.8。 ②。 下列说法错误的是( ) A.“氧化”时生成的离子方程式为 B.“沉降”过程中加入NaOH溶液,调节溶液pH>6.7 C.加入生成,说明 D.“沉铬”过程中,增大溶液的pH,沉铬率提高 5.提纯粗品(含少量的和)得到纯品的方案如下,所用试剂为溶液、溶液、盐酸和溶液。 下列说法不正确的是( ) A.用过量的溶液除去 B.通过生成沉淀后过滤除去 C.4种试剂的使用顺序为溶液、溶液、盐酸、溶液 D.调后的滤液蒸发至大量固体析出,趁热过滤、洗涤、干燥后即得纯品 6.将溴水分别与四氯化碳、己烷、己烯、酒精四种试剂混合,充分振荡后静置,下列现象与所加试剂不相吻合的是( ) 选项 A B C D 与溴水混合的试剂 四氧化碳 己烷 己烯 酒精 现象 A.A B.B C.C D.D 7.下列实验装置可以用于制备相应物质的是( ) A.装置甲可用于制备 B.装置乙可用于制备 C.装置丙可用于制备溴苯 D.装置丁可用于制备乙烯 8.是重要的化工原料,下列流程涉及的制备与用途。有关说法正确的是( ) A.过程Ⅰ中,实验室制氨可用氢氧化钠代替熟石灰 B.过程Ⅱ中,物质A是一种高效氮肥 C.过程Ⅲ中,参加反应的氧化剂与还原剂的物质的量之比为2:1 D.过程Ⅳ中,反应的离子方程式为 9.固体粉末X中可能含有、、中的若干种。为确定该固体粉末的成分,取适量X进行以下实验,实验过程及现象如图所示。下列说法不正确的是( ) A.气体1一定不含有 B.沉淀4一定是纯净物 C.固体X中至少含有两种物质 D.若沉淀3为白色沉淀且在空气中久置不变色,则X中一定含有 10.一包由三种物质组成的混合物,它们是、和Al中的三种。为了确定其组成进行如下实验,该混合物的成分可能是( ) 序号 操作及现象 Ⅰ 取少量粉末溶于水,产生沉淀,放出无色气体。在该气体中点燃镁条,镁条能燃烧,只产生白色粉末 Ⅱ 过滤,得到固体和透明滤液 Ⅲ 取Ⅱ中固体,加入足量NaOH溶液,固体部分溶解,得到红褐色固体 A.和 B.和 C.和 D.和 11.镓被称为“电子工业脊梁”,与铝性质相似。以砷化镓废料(主要成分为GaAs,含少量等杂质)为原料生产Ga,工艺流程如图。已知砷化镓废料“溶解”后砷以形式存在。下列说法错误的是( ) A.砷化镓“溶解”反应的还原剂与氧化剂物质的量之比为1:4 B.“滤渣2”的主要成分为、 C.实验室“结晶”时用到的硅酸盐仪器有酒精灯、烧杯、坩埚、玻璃棒 D.电解溶液的阴极电极反应式为 12.下列实验操作、现象和结论均正确的是( ) 编号 实验操作 现象 结论 A 用坩埚钳夹持一片未打磨的薄铝片,在酒精灯火焰上加热,轻轻晃动铝片 铝片表面呈灰白色,熔化而不滴落 铝的熔点很高 B 把加入碘水中,振荡、静置、分液,从上口倒出有机层 有机层呈现紫红色 能 ... ...
~~ 您好,已阅读到文档的结尾了 ~~