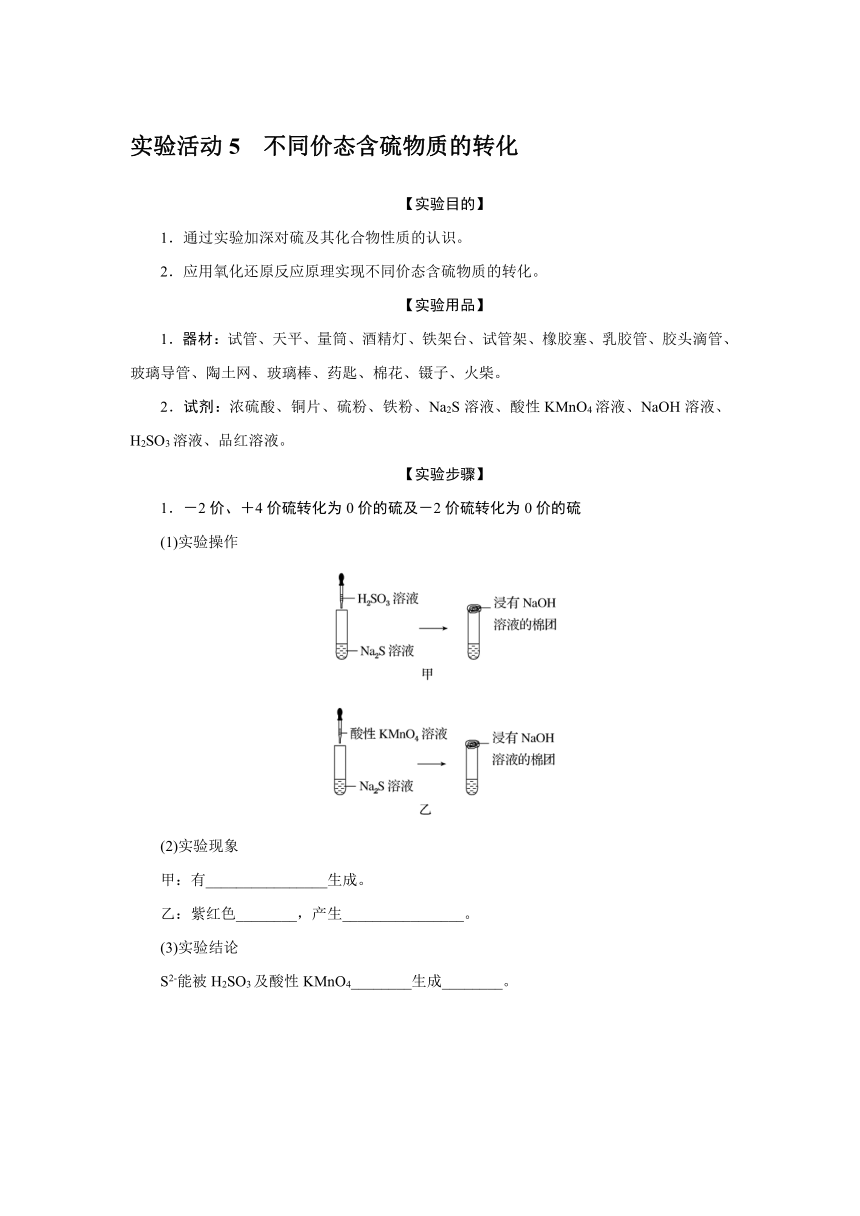
实验活动5 不同价态含硫物质的转化 【实验目的】 1.通过实验加深对硫及其化合物性质的认识。 2.应用氧化还原反应原理实现不同价态含硫物质的转化。 【实验用品】 1.器材:试管、天平、量筒、酒精灯、铁架台、试管架、橡胶塞、乳胶管、胶头滴管、玻璃导管、陶土网、玻璃棒、药匙、棉花、镊子、火柴。 2.试剂:浓硫酸、铜片、硫粉、铁粉、Na2S溶液、酸性KMnO4溶液、NaOH溶液、H2SO3溶液、品红溶液。 【实验步骤】 1.-2价、+4价硫转化为0价的硫及-2价硫转化为0价的硫 (1)实验操作 (2)实验现象 甲:有_____生成。 乙:紫红色_____,产生_____。 (3)实验结论 S2-能被H2SO3及酸性KMnO4_____生成_____。 2.+6价的硫转化为+4价的硫 实验装置 实验现象 加热有_____生成,品红溶液逐渐变为_____ 实验结论 浓硫酸和Cu反应的化学方程式: 2H2SO4(浓)+Cu 3.0价的硫转化为-2价的硫 (1)实验装置及操作 (2)实验现象:混合物继续保持_____,最后生成_____固体。 (3)硫粉和铁粉反应的方程式:Fe+SFeS。 【问题探究】 1.在上述实验中,含硫物质中硫元素的价态发生了怎样的变化? 2.实验1中用浸有NaOH溶液的棉团塞住试管口的作用是什么? 3.SO2具有还原性,浓硫酸具有强氧化性,能否用浓硫酸干燥SO2气体? 4.铁粉和硫粉在空气中混合燃烧时,可能发生哪些化学反应? 即学即练 1.实验室研究不同价态元素的转化,对于物质的制备和应用至关重要。实验室可以用如图所示装置研究S(+6价)→S(+4价)。 (1)装置C的作用是_____。 (2)装置B、D盛放的试剂应分别为_____、_____(填字母)。 a.BaCl2溶液 b.KI淀粉溶液 c.FeSO4溶液 d.NaOH溶液 e.品红溶液 (3)实验结束后,发现装置A中溶液几乎为无色,且试管中有较多的白色固体。试管中溶液显无色,体现了浓硫酸的_____性。 (4)实验结束后,若要证明装置A中白色固体为无水CuSO4,需要采取的操作是_____。 2.亚硫酸钠是一种无机物,化学式为Na2SO3,是常见的亚硫酸盐,是白色、单斜晶体或粉末。对眼睛、皮肤、黏膜有刺激作用,可污染水源。受高热分解产生有毒的硫化物烟气。工业上主要用于制亚硫酸纤维素酯、硫代硫酸钠、有机化学药品、漂白织物等,还用作还原剂、防腐剂、去氯剂等。 请回答: (1)亚硫酸钠分解的化学方程式为4Na2SO3Na2S+3Na2SO4,从氧化还原反应的角度分析亚硫酸钠具有_____性质。 (2)现有试剂:溴水、硫化钠溶液、亚硫酸钠溶液、稀硫酸、氢氧化钠溶液、亚硫酸溶液。 ①要证明亚硫酸溶液具有还原性,应选用_____试剂;会观察到现象为_____,写出反应的离子方程式:_____。 ②要证明亚硫酸钠溶液具有氧化性,应选用_____试剂;会观察到现象为_____,写出反应的离子方程式:_____。 3.[2024·北京西城区高一期末]亚硫酸钠(Na2SO3)是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究 Na2SO3 的性质,进行了如下实验。 [性质预测] (1)Na2SO3 中硫元素的化合价是_____价,属于 S 元素的中间价态,既具有氧化性,又具有还原性。 [实验验证] 资料:酸性条件下,KMnO4 被还原为无色的 Mn2+。 [分析解释] (2)实验ⅰ中,反应的离子方程式是_____。 (3)实验ⅱ中,能说明 Na2S 在酸性条件下被氧化的实验现象是_____。 [继续探究] (4)甲同学认为实验ⅱ 的现象不能直接得出“Na2SO3具有氧化性”。 ①对淡黄色浑浊产生的原因作出如下假设: 假设a:酸性溶液中的具有氧化性,可产生S; 假设b:空气中存在O2,在酸性条件下,由于_____(用离子方程式表示),可产生S; 假设c:酸性溶液中的具有氧化性,可产生S。 ②设计实验ⅲ证实了假设a和b不是产生S的主要原因。 实验ⅲ:向Na2S溶液中加入_____(填试剂名称),产生有臭鸡蛋气味的气体,溶液未变浑浊。 (5)结合实验ⅱ和ⅲ,用离子方 ... ...
~~ 您好,已阅读到文档的结尾了 ~~