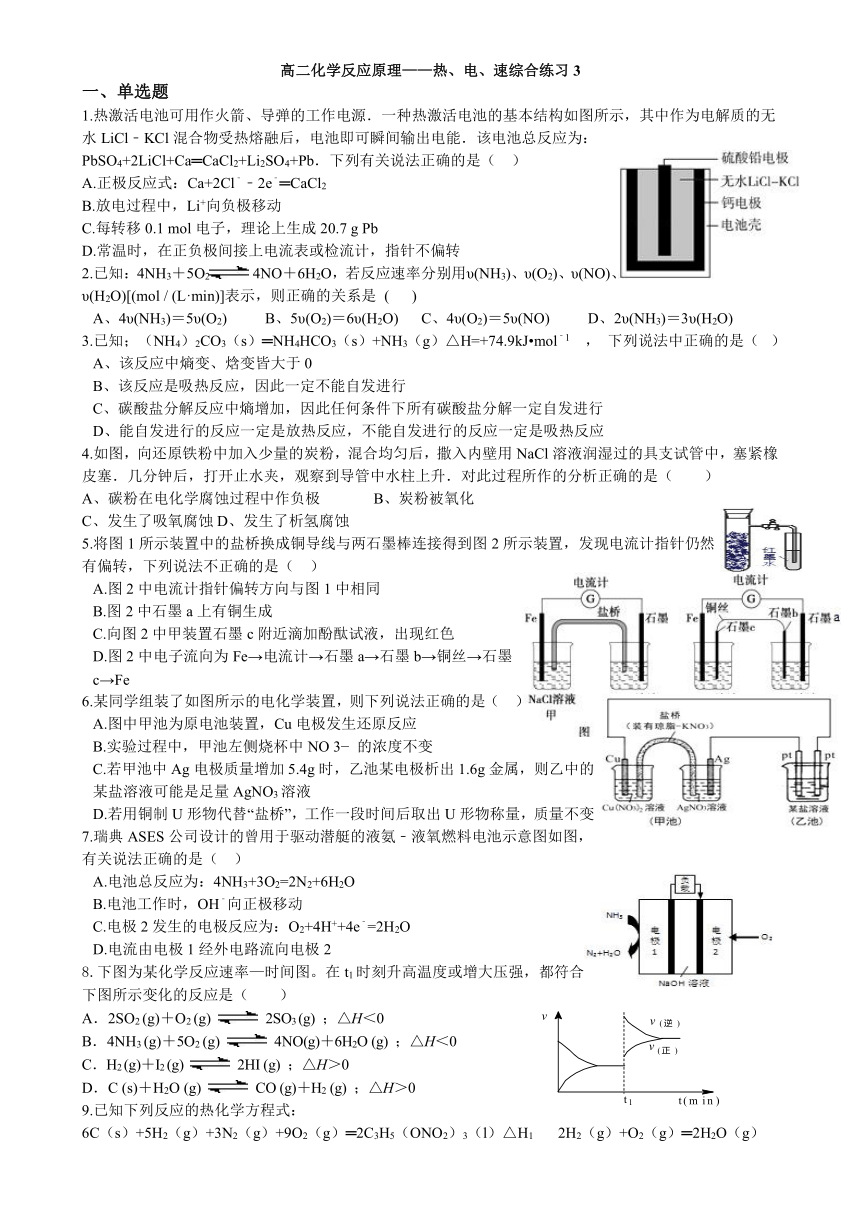
高二化学反应原理———热、电、速综合练习3 一、单选题 1.热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl﹣KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为:PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( ) A.正极反应式:Ca+2Cl﹣﹣2e﹣═CaCl2 B.放电过程中,Li+向负极移动 C.每转移0.1 mol电子,理论上生成20.7 g Pb D.常温时,在正负极间接上电流表或检流计,指针不偏转 2.已知:4NH3+5O2 4NO+6H2O,若反应速率分别用υ(NH3)、υ(O2)、υ(NO)、υ(H2O)[(mol / (L·min)]表示,则正确的关系是 ( ) A、4υ(NH3)=5υ(O2) B、5υ(O2)=6υ(H2O) C、4υ(O2)=5υ(NO) D、2υ(NH3)=3υ(H2O) 3.已知;(NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9kJ mol﹣1 , 下列说法中正确的是( ) A、该反应中熵变、焓变皆大于0 B、该反应是吸热反应,因此一定不能自发进行 C、碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行 D、能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 4.如图,向还原铁粉中加入少量的炭粉,混合均匀后,撒入内壁用NaCl溶液润湿过的具支试管中,塞紧橡皮塞.几分钟后,打开止水夹,观察到导管中水柱上升.对此过程所作的分析正确的是( ) A、碳粉在电化学腐蚀过程中作负极 B、炭粉被氧化 C、发生了吸氧腐蚀D、发生了析氢腐蚀 5.将图1所示装置中的盐桥换成铜导线与两石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转,下列说法不正确的是( ) A.图2中电流计指针偏转方向与图1中相同 B.图2中石墨a上有铜生成 C.向图2中甲装置石墨c附近滴加酚酞试液,出现红色 D.图2中电子流向为Fe→电流计→石墨a→石墨b→铜丝→石墨c→Fe 6.某同学组装了如图所示的电化学装置,则下列说法正确的是( ) A.图中甲池为原电池装置,Cu电极发生还原反应 B.实验过程中,甲池左侧烧杯中NO 3 的浓度不变 C.若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某盐溶液可能是足量AgNO3溶液 D.若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量不变 7.瑞典ASES公司设计的曾用于驱动潜艇的液氨﹣液氧燃料电池示意图如图,有关说法正确的是( ) A.电池总反应为:4NH3+3O2=2N2+6H2O B.电池工作时,OH﹣向正极移动 C.电极2发生的电极反应为:O2+4H++4e﹣=2H2O D.电流由电极1经外电路流向电极2 8.下图为某化学反应速率—时间图。在t1时刻升高温度或增大压强,都符合下图所示变化的反应是( ) A.2SO2 (g)+O2 (g) 2SO3 (g) ;△H<0 B.4NH3 (g)+5O2 (g) 4NO(g)+6H2O (g) ;△H<0 C.H2 (g)+I2 (g) 2HI (g) ;△H>0 D.C (s)+H2O (g) CO (g)+H2 (g) ;△H>0 9.已知下列反应的热化学方程式: 6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1 2H2(g)+O2(g)═2H2O(g)△H2 C(s)+O2(g)═CO2(g)△H3 则反应4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为( ) A.12△H3+5△H2﹣2△H1 B.2△H1﹣5△H2﹣12△H3 C.12△H3﹣5△H2﹣2△H1 D.△H1﹣5△H2﹣12△H3 10.100mL 4mol/L 稀硫酸与2g锌粒反应,在一定温度下为了减缓反应的速率,但又不影响生成氢气的总量,可向反应物中加入( ) A.硫酸钠固体 B.硫酸铜固体 C.硝酸钾溶液 D.氯化钠溶液 11.甲醇﹣空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如图.下列有关叙述正确的是( ) A.H+从正极区通过交换膜移向负极区 B.负极的电极反应式为:CH3OH(l)+H2O(l)﹣6e﹣=CO2(g)+6H+ C.d导出的是CO2 D.图中b、c分别是O2、甲醇 12.某种氢氧燃料电池的电 ... ...
~~ 您好,已阅读到文档的结尾了 ~~

