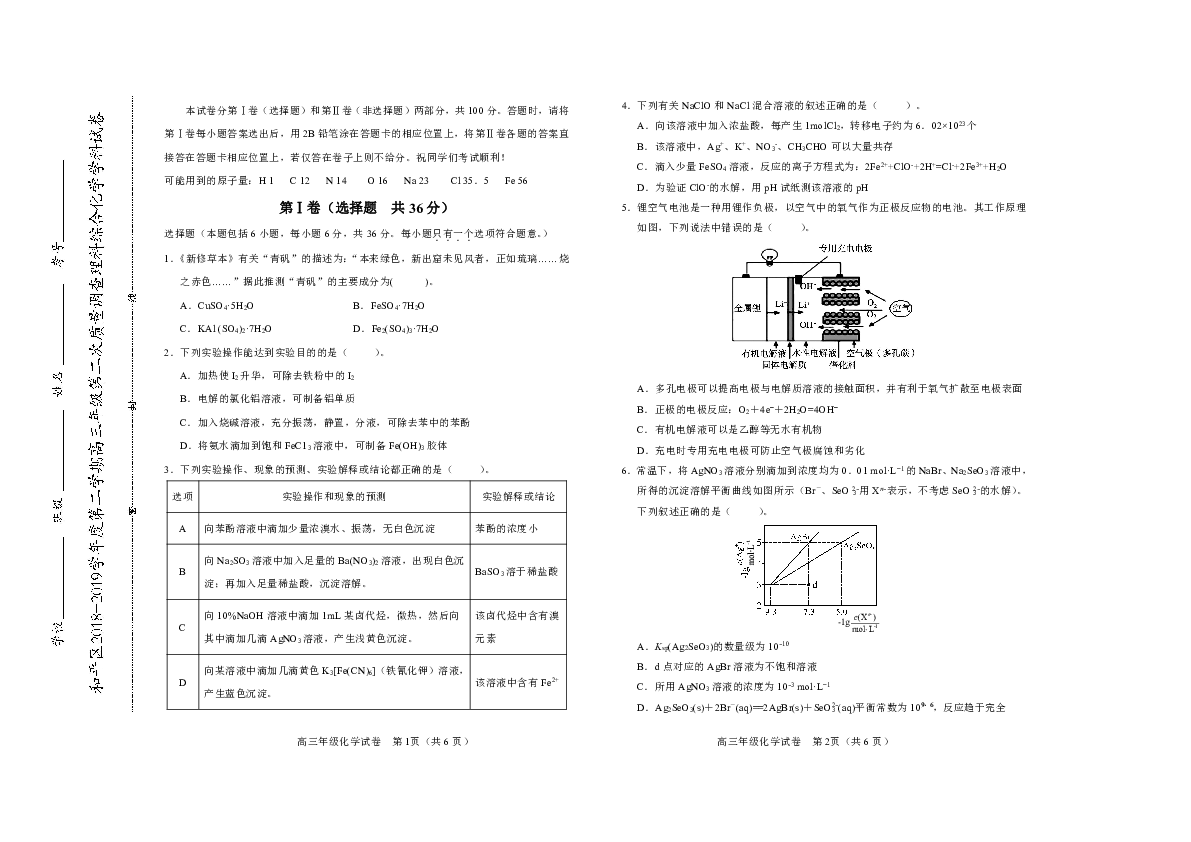
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分。答题时,请将第Ⅰ卷每小题答案选出后,用2B铅笔涂在答题卡的相应位置上,将第Ⅱ卷各题的答案直接答在答题卡相应位置上,若仅答在卷子上则不给分。祝同学们考试顺利! 可能用到的原子量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5 Fe 56 第Ⅰ卷(选择题 共36分) 选择题(本题包括6小题,每小题6分,共36分。每小题只有一个选项符合题意。) 1.《新修草本》有关“青矾”的描述为:“本来绿色,新出窟未见风者,正如琉璃……烧之赤色……”据此推测“青矾”的主要成分为( )。 A.CuSO4·5H2O B.FeSO4·7H2O C.KAl (SO4)2·7H2O D.Fe2(SO4)3·7H2O 2.下列实验操作能达到实验目的的是( )。 A.加热使I2升华,可除去铁粉中的I2 B.电解的氯化铝溶液,可制备铝单质 C.加入烧碱溶液,充分振荡,静置,分液,可除去苯中的苯酚 D.将氨水滴加到饱和FeC13溶液中,可制备Fe(OH)3胶体 3.下列实验操作、现象的预测、实验解释或结论都正确的是( )。 选项 实验操作和现象的预测 实验解释或结论 A 向苯酚溶液中滴加少量浓溴水、振荡,无白色沉淀 苯酚的浓度小 B 向Na2SO3溶液中加入足量的Ba(NO3)2溶液,出现白色沉淀;再加入足量稀盐酸,沉淀溶解。 BaSO3溶于稀盐酸 C 向10%NaOH溶液中滴加1mL某卤代烃,微热,然后向其中滴加几滴AgNO3溶液,产生浅黄色沉淀。 该卤代烃中含有溴元素 D 向某溶液中滴加几滴黄色K3[Fe(CN)6](铁氰化钾)溶液,产生蓝色沉淀。 该溶液中含有Fe2+ 4.下列有关NaClO和NaCl混合溶液的叙述正确的是( )。 A.向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 B.该溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存 C.滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+=Cl-+2Fe3++H2O D.为验证ClO-的水解,用pH试纸测该溶液的pH 5.锂空气电池是一种用锂作负极,以空气中的氧气作为正极反应物的电池。其工作原理如图,下列说法中错误的是( )。 A.多孔电极可以提髙电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面 B.正极的电极反应:O2+4e ̄+2H2O=4OH ̄ C.有机电解液可以是乙醇等无水有机物 D.充电时专用充电电极可防止空气极腐蚀和劣化 6.常温下,将AgNO3溶液分别滴加到浓度均为0.01?mol·L?1的NaBr、Na2SeO3溶液中,所得的沉淀溶解平衡曲线如图所示(Br-、SeO�用Xn-表示,不考虑SeO�的水解)。下列叙述正确的是( )。 A.Ksp(Ag2SeO3)的数量级为10-10 B.d点对应的AgBr溶液为不饱和溶液 C.所用AgNO3溶液的浓度为10-3 mol·L?1 D.Ag2SeO3(s)+2Br-(aq)==2AgBr(s)+SeO�(aq)平衡常数为109.6,反应趋于完全 第Ⅱ卷(非选择题 共64分) 注意事项: 1.用黑色墨水的钢笔或或签字笔将答案写在试卷上。 2.本卷共4题,共64分。 7.(14分)锂在有机合成、电池等领城中有重要的作用。 Ⅰ.LiAlH4的制备和应用如下图所示。 (1)锂元素在元素周期表中的位置 。 (2)写出A的电子式 。 (3)LiAlH4是有机合成中常用的还原剂,试写出反应③的化学方程式 。 Ⅱ.磷酸亚铁锂(LiFePO4)是新型锂离子电池的首选电极材料,是以铁棒为阳极,石墨为阴极,电解磷酸二氢铵、氯化锂混合溶液,析出磷酸亚铁锂沉淀,在800℃左右、惰性气体氛围中煅烧制得。在锂离子电池中,需要一种有机聚合物作为正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如下: CH2=C—C—OCH2CH2O—C—OCH3 请回答下列问题: (1)制备磷酸亚铁锂必须在惰性气体氛围中进行,其原因是_____。 (2)阳极生成磷酸亚铁锂的电极反应式为_____。 (3)写出M与足量氢氧化钠溶液反应的化学方程式_____。 (4)该电池充电时阳极的磷酸 ... ...
~~ 您好,已阅读到文档的结尾了 ~~